Современные подходы к диагностике и лечению тикозных гиперкинезов у детей | Зыков В.П., Каширина Э.А., Наугольных Ю.В., Комарова И.Б., Новикова Е.Б.
В статье представлены современные подходы к диагностике и лечению тикозных гиперкинезов у детей.
Введение
Тикозные расстройства представляют собой актуальную проблему в связи с высокой частотой встречаемости, достигающей 1–6% в детской популяции, коморбидностью с синдромом дефицита внимания, стереотипиями, тревожностью, трудностями обучения, перепадами настроения и нарушениями сна [1, 2].
Тик представляет собой стереотипный гиперкинез, включающий различные группы мышц, напоминает произвольные движения или звуки, усиливается при эмоциональных и физических нагрузках, исчезает во сне [3]. В последней версии Международной классификации болезней (МКБ-11) [4], которая представлена для обсуждения, тикозные расстройства и синдром Туретта (СТ) из раздела психических заболеваний переведены в раздел болезней нервной системы. Проект МКБ-11 будет утвержден Генеральной Ассамблеей ВОЗ в мае 2019 г. Планируется полный переход на новую версию с 2022 г. Надо отметить, что данное нововведение оправданно, т. к. родители обращаются в первую очередь к детскому неврологу при появлении тикозных гиперкинезов, а не к психиатру.
Проект МКБ-11 будет утвержден Генеральной Ассамблеей ВОЗ в мае 2019 г. Планируется полный переход на новую версию с 2022 г. Надо отметить, что данное нововведение оправданно, т. к. родители обращаются в первую очередь к детскому неврологу при появлении тикозных гиперкинезов, а не к психиатру.
Классификация тикоподобных расстройств по МКБ-11
09 Болезни нервной системы / Двигательные нарушения
8A05.0 Первичные тики или тиковые расстройства
8A05.00 Синдром Туретта
8A05.01 Хронический моторный синдром
8A05.02 Хроническое звуковое расстройство
8A05.0Y Другие уточненные первичные тики или тиковые расстройства
8A05.0Z Первичные тики или тиковые расстройства, неуточненные
8A05.1 Вторичные тики
8A05.10 Инфекционные или постинфекционные тики
8A05.11 Тики, связанные с нарушениями развития
8A05. 1Y Другие уточненные вторичные тики
1Y Другие уточненные вторичные тики
8A05.1Z Вторичные тики, неуточненные
8A05.Y Другие уточненные тиковые расстройства
Первичные тики
Под первичными тиками подразумевают наследственные, с клинических позиций целесообразно составление родословных, поиск родственников, у которых были тики в детском возрасте или наблюдаются в настоящее время. В ряде случаев ретроспектива гиперкинезов родственников пробанда позволяет представить индивидуальный прогноз для больного. СТ рассматривают как множественные генерализованные моторные тики, один или более вокальные, возникающие в течение 12 мес. с ремиссией не более 3 мес. Гиперкинезы значительно ухудшают профессиональную деятельность (у взрослых) или обучение в школе и колледже (у детей). Имеются сложности дифференциальной диагностики между СТ и хроническими моторными и вокальными тиками, в связи с чем изучают генетические, нейрофизиологические маркеры заболевания и данные нейровизуализации.
Семиотика тиков и топография гиперкинезов имеют следующую особенность перехода хронических тиков в СТ, а именно генерализацию моторных тиков с включением верхних и нижних конечностей, мышц-разгибателей спины и живота.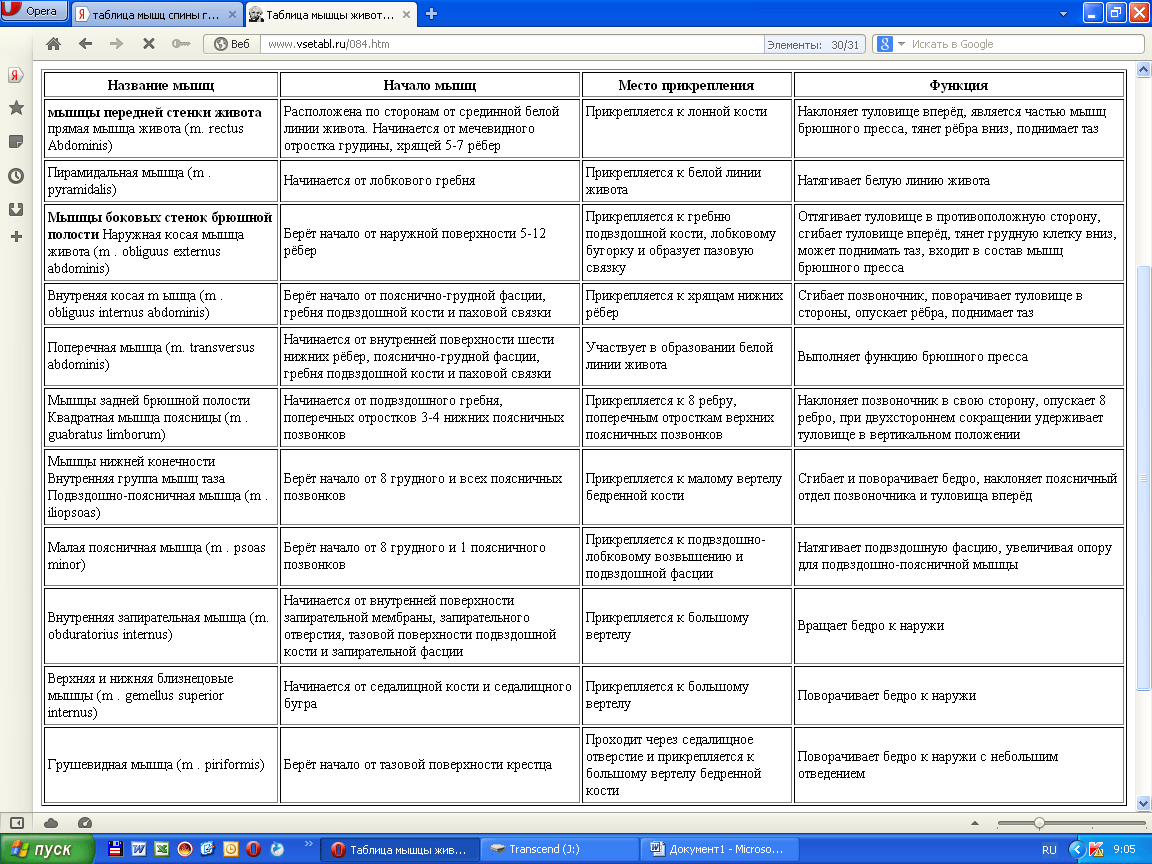 Хронические тики отличаются от СТ тяжестью гиперкинезов по Йельской шкале оценки тяжести тиков
Хронические тики отличаются от СТ тяжестью гиперкинезов по Йельской шкале оценки тяжести тиков
YGTSS [7], длительностью периодов обострения, трудностями социальной адаптации. В МКБ-11 присутствует нозология «хронический моторный и вокальный тик», только для детского возраста имеется сочетание хронических моторных и вокальных тиков, но по выраженности проявлений они не достигают СТ. В семиотике гиперкинезов мы выделяем клонические и дистонические тики (табл. 1).
Вторичные тики
Вторичные тики: постинфекционные, в рамках последствий стрептококковой инфекции, педиатрический аутоиммунный синдром, вызванный стрептококком, и педиатрический иммунный синдром, вызванный любой инфекцией. По нашим данным, до 17% больных после респираторных инфекций имели антитела к хвостатому ядру. Клиническими критериями инфекционных тиков являются дебют гиперкинезов и обострение после респираторных инфекций, незначительный эффект от антитикозных препаратов — нейролептиков.
Решающими факторами для определения нозологической формы являются семиотика и количество серий тиков за 20 мин. Как видно из таблицы 1, СТ отличается от хронических тиков полиморфизмом моторных гиперкинезов, включая тики верхних и нижних конечностей, наличие сложных вокализмов.
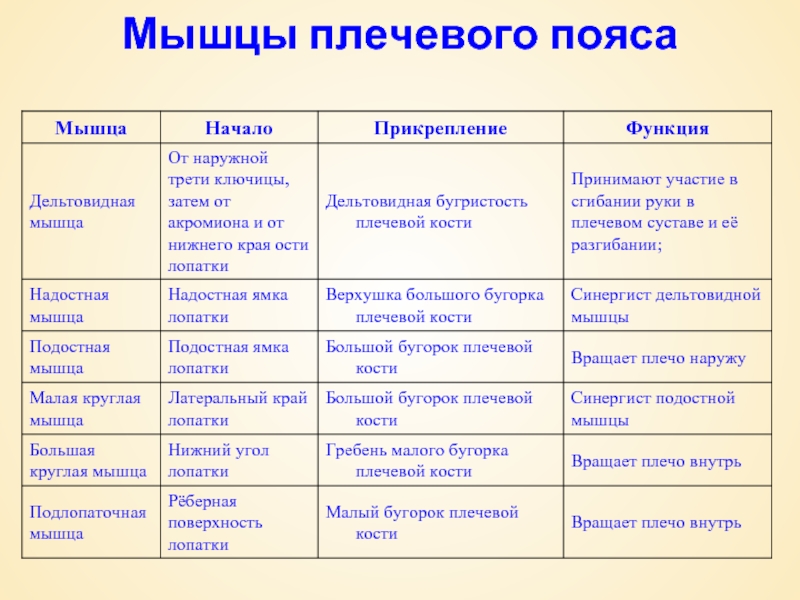 Обострения заболевания протекают с высокой частотой тиков за 20 мин до 100 и более и высоким уровнем баллов по Йельской шкале оценки тяжести тиков. Гиперкинезы приводят к нарушению адаптации и обучения в школе. D. Martino et al. (2015) [10] считают, что синдром дефицита внимания, обсессивно-компульсивный синдром и сенсорные симптомы (предчувствие тика) являются основными критериями СТ.
Обострения заболевания протекают с высокой частотой тиков за 20 мин до 100 и более и высоким уровнем баллов по Йельской шкале оценки тяжести тиков. Гиперкинезы приводят к нарушению адаптации и обучения в школе. D. Martino et al. (2015) [10] считают, что синдром дефицита внимания, обсессивно-компульсивный синдром и сенсорные симптомы (предчувствие тика) являются основными критериями СТ.
Клиническое наблюдение
Мы обследовали 130 больных с тикозными расстройствами в возрасте 6–14 лет, средний возраст составил 10±4 года. В таблице 1 представлены семиотика и топография гиперкинезов, оценка тяжести методом подсчета за 20 мин и по шкале тяжести тиков YGSST.
Обращает на себя внимание тот факт, что отличие СТ от хронических моторно-вокальных тикозных расстройств состояло в генерализации гиперкинезов на верхние и нижние конечности, наличии 3 и более различных вариантов моторных тиков, статусных вокализмов и появлении эхо-копролалии. Результаты подсчета тиков за 20 мин соответствовали результатам балльной оценки по шкале YGTSS. Максимальное количество моторных и вокальных тиков при подсчете за 20 мин было выявлено у больных СТ, как и балльная оценка суммарной и совокупной тяжести тиков. Достоверные различия наблюдались только между группами больных с изолированными моторными симптомами и СТ. С целью поиска нейрофизиологических паттернов для дифференциального диагноза СТ от хронических моторно-вокальных тиков проведена электромиография (ЭМГ).
Результаты подсчета тиков за 20 мин соответствовали результатам балльной оценки по шкале YGTSS. Максимальное количество моторных и вокальных тиков при подсчете за 20 мин было выявлено у больных СТ, как и балльная оценка суммарной и совокупной тяжести тиков. Достоверные различия наблюдались только между группами больных с изолированными моторными симптомами и СТ. С целью поиска нейрофизиологических паттернов для дифференциального диагноза СТ от хронических моторно-вокальных тиков проведена электромиография (ЭМГ).
В таблице 2 представлена клинико-электромиографическая верификация гиперкинезов. У больных 1-й группы при проведении исследования в интерференционном режиме ЭМГ кластерная залповая активность (КЗА) не выявлялась.

Амплитуда биоэлектрической активности (БЭА) лобной мышцы (при записи слева), мышц плечевого пояса (трапециевидной, надостной мышц при записи справа) у больных моторными тиками (1-я группа) не отличалась от таковой в группе контроля. Обнаруживалось значимое увеличение амплитуды БЭА мышц лица (лобная мышца при записи справа, круговая мышца глаза, круговая мышца рта), плечевого пояса (трапециевидной мышцы, надостной мышцы при записи слева), мышц верхних конечностей без регистрации КЗА, эти параметры достоверно превышали соответствующие показатели в контрольной группе (p<0,01).
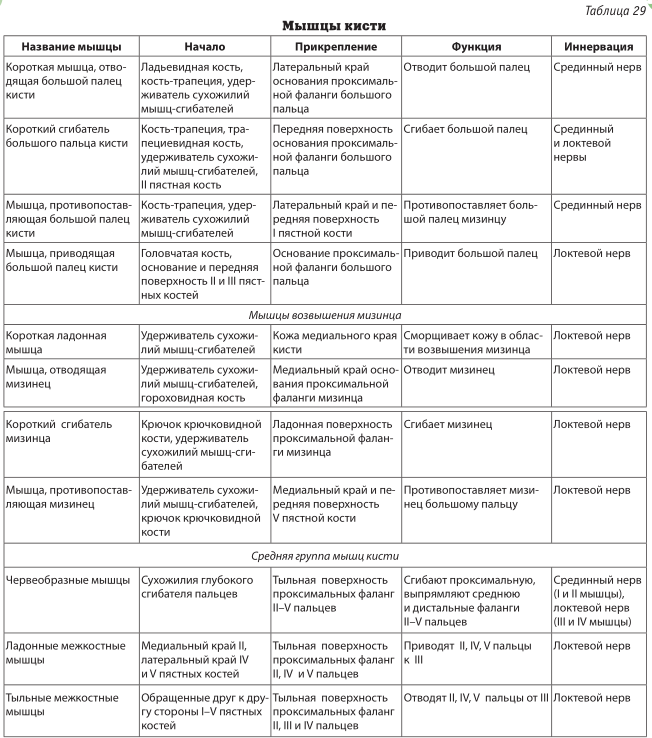
У пациентов 2-й группы амплитуда БЭА лобной мышцы (при записи справа) не отличалась от таковой в группе контроля (табл. 2). Было обнаружено достоверное увеличение амплитуды БЭА лобной мышцы при записи слева по сравнению с таковой в группе контроля (p<0,01), круговой мышцы рта (p<0,01), надостной мышцы при записи справа (p<0,01). КЗА была зафиксирована в мышцах лица — в круговой мышце глаза, в мышцах плечевого пояса — трапециевидных мышцах, надостной мышце при записи слева, мышцах верхних конечностей с амплитудой залпов 350,33+356,63 мкВ длительностью до 100 мс.
У больных СТ (3-й группы) БЭА лобной мышцы была достоверно выше, чем в контрольной группе (p<0,01). КЗА обнаруживалась во всех исследуемых мышцах — лица (круговая мышца глаза, круговая мышца рта), плечевого пояса, верхних конечностей с амплитудой ЗА 380,24+512,55 мкВ длительностью осцилляции в пределах 100 мс. У пациентов 3-й группы отмечалось значимое преобладание БЭА лобной мышцы при записи слева по сравнению с больными 1-й (p<0,01) и 2-й групп (p<0,05).

Таким образом, только по данным ЭМГ обнаружены четкие различия между группами больных моторными, моторно-вокальными тиками и СТ по параметрам исходного фона БЭА мышц, количеству серийных (кластерных) залпов и их амплитуды, получена прямая корреляция с тяжестью гиперкинезов по шкале YGSST.
Патогенетические концепции, которые рассматриваются в современной литературе, касаются дисфункции нейромедиаторных систем дофамина, норадреналина, ГАМК, серотонина и глутамата в кортико-стриато-амигдало-таламо-кортикальной системе [10–12]. Последние исследования с использованием функциональной МРТ показали связь эмоциональных факторов со зрительной корой, инсулярной областью и стриарной системой у больных СТ по сравнению со здоровыми обследуемыми [13].
 Данное исследование позволило объяснить роль психоэмоционального фактора, провоцирующего тик, зону дебюта гиперкинеза рассматривать как дополнительную моторную кору. МРТ с режимом анизотропии определила связь тяжести тиков, нарушений плотности связей и нейронов в корковых отделах сенсомоторной коры левого полушария, что было расценено как врожденные или приобретенные изменения, которые объясняют длительное течение заболевания и продолжение его у взрослых [14].
Данное исследование позволило объяснить роль психоэмоционального фактора, провоцирующего тик, зону дебюта гиперкинеза рассматривать как дополнительную моторную кору. МРТ с режимом анизотропии определила связь тяжести тиков, нарушений плотности связей и нейронов в корковых отделах сенсомоторной коры левого полушария, что было расценено как врожденные или приобретенные изменения, которые объясняют длительное течение заболевания и продолжение его у взрослых [14].
Лечение тиков
Лечение тиков представляет собой длительную программу — от 4–6 мес. до нескольких лет. В период обострения рекомендуется ограничить просмотр телепрограмм и занятия на персональном компьютере. В режим ввести длительные пешие прогулки. Лечение коморбидных синдромов рекомендуется проводить после стабилизации тикозных гиперкинезов. В стадии дебюта в дошкольном и младшем школьном возрасте рекомендуется назначение гопантеновой или аминофенилмасляной кислоты (Анвифен®).
Аминофенилмасляная кислота представляет собой фенильное производное гамма-аминомасляной кислоты (ГАМК). Фармакологические характеристики, включая влияние на GABA, допаминергические и бензодиазепиновые рецепторы, оказались сопоставимы с таковыми у диазепама и пирацетама. Аминофенилмасляная кислота и ГАМК обладают одинаковым действием на ионные каналы, что было доказано в исследовании на изолированных нейронах беспозвоночных [15]. Кроме того, препарат оказывает сходное с бензодиазепинами нейрохимическое действие на подкорковые ядра [16, 17]. Показано, что введение фенибута до воздействия стрессового фактора повышает чувствительность бензодиазепиновых рецепторов [16, 17].
Л.С. Мехилане и соавт. провели двойное плацебо-контролируемое слепое исследование эффективности аминофенилмасляной кислоты у пациентов с невротическими и психотическими расстройствами [18]. В данном исследовании было показано, что назначение препарата в дозе 0,25-0,5 г трижды в день приводит к активизации интеллектуальных функций, увеличению физической выносливости, мотивационной активности, уменьшает симптомы астении и раздражительности.
В детском возрасте аминофенилмасляная кислота используется преимущественно для коррекции негрубых тикозных расстройств и заикания [19, 20]. До последнего времени препарат был представлен исключительно в дозе 0,25 г (Фенибут), что при лечении детей дошкольного возраста вызывало необходимость деления таблеток и было неудобно. Кроме того, существовала вероятность негативного раздражающего действия на желудочно-кишечный тракт. В последние годы появился новый препарат Анвифен®, преимуществами которого являются капсулированная форма и наличие детской дозировки (50 мг). Это сделало возможным использование лекарства с 3-летнего возраста.
Мы использовали препарат аминофенилмасляной кислоты для лечения 25 больных тиками в стадии дебюта в возрасте 5–10 лет с целью действия на тормозные ГАМК-ергические системы мозга. Дозы составляли, исходя из инструкции к препарату, для детей 5–8 лет 50–100 мг 3 раза в день, 8–10 лет 250 мг 3 раза в день [21], курс лечения — 3–6 мес. Наряду со снижением симптоматики тиков (учащенного мигания) и движения крыльев носа уменьшились проявления заикания, улучшилась речь. Через 10–12 мес. все больные были без терапии, и у 3 из них отмечалось обострение симптоматики тиков с увеличением гиперкинезов от исходных показателей в 2 раза, в связи с чем назначили клоназепам. Использование аминофенилмасляной кислоты приводит к полному исчезновению единичных локальных тиков в период ее приема, одновременно препарат оказывает положительное воздействие на заикание клонической формы. При отсутствии эффекта лечения препаратом можно повысить дозировку до максимально переносимой дозы и удлинить курс лечения до 12 мес.
Наряду со снижением симптоматики тиков (учащенного мигания) и движения крыльев носа уменьшились проявления заикания, улучшилась речь. Через 10–12 мес. все больные были без терапии, и у 3 из них отмечалось обострение симптоматики тиков с увеличением гиперкинезов от исходных показателей в 2 раза, в связи с чем назначили клоназепам. Использование аминофенилмасляной кислоты приводит к полному исчезновению единичных локальных тиков в период ее приема, одновременно препарат оказывает положительное воздействие на заикание клонической формы. При отсутствии эффекта лечения препаратом можно повысить дозировку до максимально переносимой дозы и удлинить курс лечения до 12 мес.
Критерием стадии экспрессии — пика клинических проявлений тиков — является более 50 тиков за 20 мин подсчета (тикозный статус). В стадии экспрессии симптомов детям 8–12 лет мы рекомендуем начинать лечение с Анвифена, в случае отсутствия динамики симптомов через 3–4 нед. переходить к лечению антиконвульсантами и нейролептиками:
антиконвульсанты: клоназепам, топирамат, леветирацетам;
нейролептики: тиаприд 100–300 мг, галоперидол 1,5–3 мг (уровень доказательности А), рисперидон 2–4 мг, арипипразол (уровень доказательности С), оланзапин (уровень доказательности В) [22, 23]. Перспективно использование поведенческой терапии у детей начиная с 9–10 лет в качестве дополнительного или альтернативного лечения, тренинг купирования симптомов, предотвращения привычных тиков или замены одних движений другими (в англоязычном варианте — Habit reversal training), цель которого — обучить ребенка навыкам предотвращения тика до его появления [24]. Предложенные в нашей работе ЭМГ-критерии тиков позволят контролировать медикаментозное лечение, а также выводить на экран перед больным залповую и фоновую активность мышц во время сеанса поведенческой терапии.
Перспективно использование поведенческой терапии у детей начиная с 9–10 лет в качестве дополнительного или альтернативного лечения, тренинг купирования симптомов, предотвращения привычных тиков или замены одних движений другими (в англоязычном варианте — Habit reversal training), цель которого — обучить ребенка навыкам предотвращения тика до его появления [24]. Предложенные в нашей работе ЭМГ-критерии тиков позволят контролировать медикаментозное лечение, а также выводить на экран перед больным залповую и фоновую активность мышц во время сеанса поведенческой терапии.
Отмену антитикозной терапии целесообразно проводить в период ремиссии заболевания, желательно в период школьных каникул.
Боковой амиотрофический склероз (БАС) — симптомы и диагностика заболевания. Лечение амиотрофического склероза в Москве
Боковой амиотрофический склероз (БАС) – это прогрессирующее нейродегенеративное заболевание центральной нервной системы. Оно развивается под воздействием нескольких факторов, которые вызывают полное разрушение и гибель периферических и центральных двигательных нейронов. Сначала развивается клиника паралича, затем наступает атрофия мышцы. В патологический процесс постепенно вовлекается одна группа мышц за другой. Когда поражаются диафрагмальные мышцы, пациент утрачивает способность самостоятельно дышать и нуждается в проведении искусственной вентиляции лёгких.
Сначала развивается клиника паралича, затем наступает атрофия мышцы. В патологический процесс постепенно вовлекается одна группа мышц за другой. Когда поражаются диафрагмальные мышцы, пациент утрачивает способность самостоятельно дышать и нуждается в проведении искусственной вентиляции лёгких.
Болезнь встречается редко (по статистике, она поражает 2-5 человек на 100 тысяч населения в год), а во всем мире ею страдают порядка 70 тысяч человек. Также известно, что болезнь чаще наблюдается у мужчин, нежели у женщин, а возраст пациентов обычно старше 50 лет. Заболевание, как правило, возникает у высокоинтеллектуальных людей и спортсменов, отличающихся хорошим здоровьем на протяжении всей жизни.
В настоящее время отсутствует единое фармакологическое средство, которое излечивало бы от БАС. Врачи клиники неврологии проводят симптоматическую терапию препаратами, зарегистрированными в РФ. Благодаря тому, что на базе Юсуповской больницы проводятся клинические исследования, пациенты имеют уникальную возможность проходить лечение новейшими лекарственными средствами, которые отсутствуют в аптеках. Специалисты клиники физической реабилитации применяют инновационные методики, направленные на увеличение силы мышц. При наличии показаний врачи отделения реанимации и интенсивной терапии проводят искусственную вентиляцию лёгких дыхательными аппаратами экспертного класса.
Специалисты клиники физической реабилитации применяют инновационные методики, направленные на увеличение силы мышц. При наличии показаний врачи отделения реанимации и интенсивной терапии проводят искусственную вентиляцию лёгких дыхательными аппаратами экспертного класса.
Причины и механизмы развития
Учёные считают, что боковой амиотрофический склероз может развиться под воздействием следующих факторов:
- Аутоиммунных процессов – явлений, при которых иммунная система воспринимает здоровые клетки в качестве чужеродных элементов и разрушает их;
- Воздействия экзотоксин – термолабильных белков, которые выделяют микроорганизмы;
- Излишнего поступления внутрь нервных клеток ионов кальция;
- Курения.
Некоторые исследователи считают, что боковой амиотрофический склероз имеет наследственную природу возникновения. Заболевание может наследоваться по аутосомно-рецессивному и аутосомно-доминантному типу. В 15% случаев у пациентов полностью отсутствовал или имел дефект ген, который кодирует важный фермент – супероксиддисмутазу-1. Он – часть антиоксидантной системы организма человека. Супероксиддисмутаза-1 преобразует супероксид (продукт радикального окисления) в кислород. Супероксид поражает нервные клетки.
В 15% случаев у пациентов полностью отсутствовал или имел дефект ген, который кодирует важный фермент – супероксиддисмутазу-1. Он – часть антиоксидантной системы организма человека. Супероксиддисмутаза-1 преобразует супероксид (продукт радикального окисления) в кислород. Супероксид поражает нервные клетки.
В основе механизма развития заболевания лежит патологическое аномальное объединение белковых молекул в цитоплазме моторных нейронов головного и спинного мозга. При дальнейшем прогрессировании заболевания происходят следующие патологические процессы:
- Атрофируются скелетные мыщцы;
- Перерождаются кортикоспинальные и кортикобульбарные спинномозговые тракты;
- Атрофируются моторные нейроны головного мозга;
- Истончается подъязычный нерв и передние корешки спинного мозга.
Исследователи до сих пор не установили причины внезапного начала процесса разрушения и гибели двигательных нейронов. Некоторые учёные предполагают, что нейрогенерация происходит под воздействием клеточных и молекулярных процессов. В результате усиленной работы моторных нейронов повышается выброс глутамата. В клетках накапливается избыточное количество кальция. Он активирует распад внутриклеточных белков. Высвобождается большое количество свободных радикалов, в том числе супероксиддисмутаза -1. Они, повреждая астроглию, микроглию и двигательные нейроны, вызывают их дегенерацию.
В результате усиленной работы моторных нейронов повышается выброс глутамата. В клетках накапливается избыточное количество кальция. Он активирует распад внутриклеточных белков. Высвобождается большое количество свободных радикалов, в том числе супероксиддисмутаза -1. Они, повреждая астроглию, микроглию и двигательные нейроны, вызывают их дегенерацию.
Мнение эксперта
Алексей Владимирович Васильев
Руководитель НПЦ болезни двигательного нейрона/БАС, кандидат медицинских наук, врач высшей категорииБоковой амиотрофический склероз — это смертельная болезнь, которая развивается очень медленно и характеризуется поражением двигательных нейронов — атрофируются мышцы, развивается парез и паралич конечностей.
Симптомы БАС схожи с симптомами миопатии. Разница в том, что амиотрофический склероз — это заболевание ЦНС, а миопатия — это мышечная дистрофия. Главный способ диагностики БАС — электромиография, а в качестве второстепенных используются МРТ, биохимический анализ крови, исследования ликвора, биопсия мышц.
Боковой амиотрофический синдром — очень редкое заболевание — не более 5 человек из 100 тысяч. Эта патология также носит название болезнь Шарко или болезнь Лу Герига, впервые была описана во второй половине 19 века. Примерно 5% случаев — наследственные, причем уже выявлены гены, отвечающие за это заболевание.
Как и другие дегенеративные заболевания ЦНС болезнь Шарко вылечить нельзя, можно только замедлить развитие. Конечно, чем раньше заболевание диагностировано, тем лучше можно купировать синдромы. Болезнь заканчивается полной атрофией мышц, больной теряет способность передвигаться и самостоятельно дышать.
Клинические формы
В зависимости от уровня поражения центральной нервной системы неврологи выделяют следующие виды БАС:
Также врачи различают классическую форму БАС, прогрессирующий бульбарный паралич, первичный боковой склероз, прогрессирующую мышечную атрофию, БАС-паркинсонизм-деменцию. По частоте встречаемости бывает спорадический (единичный) и семейный боковой амиотрофический склероз.
Симптомы
Клиническая картина заболевания зависит от формы БАС. При прогрессировании заболевания патологический процесс захватывает все мышцы, и симптомы будут одинаковыми для всех форм бокового амиотрофического склероза. Для БАС характерны следующие общие симптомы:
Фасцикуляции (подёргивание мышц) – один из первых симптомов БАС, который со временем может исчезнуть сам по себе;
Слюнотечение, возникающее из-за скопления слюны в ротовой полости;
Мышечная слабость, развивающаяся по той причине, что мускулатура стремительно теряет массу;
Болезненные судороги и спазмы мышц, которые вызывают сложности во время движения;
Быстрая утомляемость, возникающая по той причине, что мышцам требуется больше затрат для совершения обычных действий;
Боль, возникающая во время спазма, судорог, подёргивания мышц;
Проблемы с глотанием, которые приводят к тому, что пациент утрачивает способность питаться;
Кашель и чувство удушья, возникающие при попадании слюны в дыхательные пути;
Проблемы с дыханием, требующие в последствие переведения пациента на искусственную вентиляцию лёгких.
Также у пациента возникают проблемы с речью и общением. С данной проблемой пациентам помогают справиться психологи Юсуповской больницы. Они обучают общению с помощью машинок для письма, компьютеров, досок, таблиц. Специальной терапии требует эмоциональная лабильность пациента. Она может проявляться невольным смехом или плачем. Также у больных БАС возникают перепады настроения, развивается депрессивный синдром, они становятся раздражительными.
Нарушение высших психических функций проявляется нарушением памяти, мышления, понижением интеллекта. Справиться с проблемой помогают опытные врачи клиники неврологии и психологи. БАС не затрагивает зрительную и слуховую функции, обоняние и осязание. У пациентов не нарушается функция кишечника, сексуальная функция, не поражается сердечная мышца.
Пояснично-крестцовая форма бокового амиотрофического синдрома в дебюте заболевания проявляется слабостью мышц нижних конечностей. Сначала заболевает одна нога, спустя некоторое время – другая. Со временем в них снижаются сухожильные рефлексы, возникает сильный зуд.
Со временем в них снижаются сухожильные рефлексы, возникает сильный зуд.
С прогрессированием болезни поражаются мышцы рук. Они резко уменьшаются в объёме. Затем нарушается глотание, голос становится гнусавым, истончается язык. Пациент начинает попёрхиваться, у него начинаются проблемы с приёмом пищи. Ему всё труднее становится жевать. Затем у больного человека отвисает челюсть, и он утрачивает способность самостоятельно питаться.
Другая группа симптомов БАС свидетельствует о поражении как центрального, так и периферического моторных нейронов. Слабость в ногах совмещается с увеличением рефлексов. Часто появляется неконтролируемая дрожь. Это же происходит и с верхними конечностями. Когда поражаются нейроны головного мозга, возникают проблемы с пережёвыванием пищи и глотанием. У пациента отвисает челюсть, что не позволяет ему самостоятельно питаться. Иногда у пациента возникают приступы несдерживаемого смеха или плача.
Шейно-грудная форма БАС возникает при разрушении периферического двигательного нейрона. У пациента появляется слабость в мышцах кисти. Рука начинает атрофироваться. Сначала проявления болезни имеют место в одной верхней конечности, но через несколько месяцев поражается и другая рука.
У пациента появляется слабость в мышцах кисти. Рука начинает атрофироваться. Сначала проявления болезни имеют место в одной верхней конечности, но через несколько месяцев поражается и другая рука.
В нижних конечностях патологический процесс протекает иначе. Мышцы ног не атрофируются. Вначале отмечается нарастание рефлексов. Со временем появляется боль и мышечная слабость в ногах. К этому времени нарушается речевой аппарат, появляется слабость мышц шеи – голова начинает свисать. При синхронном разрушении периферического и центрального моторных нейронов мышцы рук и ног заболевшего атрофируются, но рефлексы сохраняются.
В дебюте бульбарной формы БАС пациента имеют место следующие симптомы:
Сложности с глотанием;
Нарушение артикуляции;
Попёрхивание во время приём пищи;
Фасцикуляция и атрофия языка;
Гнусавость голоса.
Из-за проблем с движением языка затрудняется процесс произношения звуков. При разрушении центрального двигательного нейрона нарушается психосоматика. Пациент может проявлять несдерживаемые эмоции: смех или плач. Нередко у него без причины возникает неконтролируемый рвотный рефлекс. Спустя некоторое время снижается сила мышц верхних и нижних конечностей, и они атрофируются. Развивается парез (неполный паралич).
При разрушении центрального двигательного нейрона нарушается психосоматика. Пациент может проявлять несдерживаемые эмоции: смех или плач. Нередко у него без причины возникает неконтролируемый рвотный рефлекс. Спустя некоторое время снижается сила мышц верхних и нижних конечностей, и они атрофируются. Развивается парез (неполный паралич).
Высокая форма БАС развивается при разрушении центрального мотонейрона. При этой форме заболевания вместе с поражением мышц нарушается функция нервной системы. У пациента нарушается психическое здоровье. Он начинает плохо запоминать информацию, у него существенно снижается уровень интеллекта. Впоследствии развивается деменция (слабоумие).
Диффузная форма бокового амиотрофического синдрома начинается с развития вялого асимметричного тетрапареза (неполного паралича всех четырёх конечностей). Затем присоединяется бульбарный синдром в виде дисфонии (расстройства речи) и дисфагии (нарушения глотания). Респираторная форма заболевания протекает очень тяжело. В связи с нарушением дыхания пациенты нуждаются в срочной искусственной вентиляции лёгких.
В связи с нарушением дыхания пациенты нуждаются в срочной искусственной вентиляции лёгких.
Прогноз
Следует заметить, что высокая и бульбарная формы бокового амиотрофического склероза являются наиболее неблагоприятными — при них срок жизни заболевших значительно сокращается. Однако какими бы ни были первые симптомы, болезнь быстро прогрессирует, в дальнейшем овладевает всем телом, и пациент утрачивает способность самостоятельно питаться, двигаться. Иногда возникает одышка — при физических нагрузках и порой даже без них. Больной чувствует нехватку воздуха, что рождает панику. В дальнейшем он может прекратить дышать самостоятельно, и для того, чтобы обеспечивать его кислородом, понадобится постоянная искусственная вентиляция легких. В некоторых случаях в конце болезни могут появляться трудности с мочеиспусканием. Вследствие атрофии заболевший сбрасывает вес.
Боковой атрофический склероз сопровождается вегетативными расстройствами: конечности ощутимо холодеют, происходит окрашивание участков кожи, увеличивается потливость и сальность кожи.
Продолжительность жизни составляет примерно от 2 до 12 лет, однако большинство заболевших умирают через 5 лет после обнаружения диагноза.
Методы диагностики
Установить диагноз бокового амиотрофического склероза обычно удаётся не сразу. Неврологи Юсуповской больницы проводят комплексное обследовании пациентов. Оно включает следующие методы исследования:
- Магнитно-резонансную томографию (МРТ) спинного и головного мозга – наиболее информативный метод, с помощью которого рентгенологи имеют возможность визуализировать дегенерацию пирамидных структур и атрофию моторных отделов головного мозга;
- Люмбальную пункцию – выполняется для получения спинно-мозговой жидкости, в которой лаборанты обнаруживают повышенное содержание белка;
- Биохимический анализ крови – позволяет установить повышение уровня КФК, АЛТ, АСТ, креатинина и мочевины;
- Нейрофизиологические методы диагностики – электронейрографию, электромиографию, транскраниальную магнитную стимуляцию;
- Генетический анализ – выявление гена, который кодирует супероксиддисмутазу – 1.

Неврологическое обследование пациентов, страдающих боковым амиотрофическим склерозом, включает в себя оценку функции черепно-мозговых нервов, бульбарных функций, мышечного тонуса по шкале Британского совета медицинских исследований и двигательных нарушений по шкале Ашфорта. Во время магнитно-резонансной томографии шеи при боковом амиотрофическом склерозе определяются дегенеративные процессы в черепно-мозговых нервах и атрофические изменения в передних рогах спинного мозга. С помощью электромиографии определяют острую и хроническую денервацию, что подтверждает поражение центральных нейронов. На электромиограмме отмечается так называемый «ритм частокола» – ритмичные потенциалы фасцикуляций.
Электронейрография позволяет неинвазивным методом измерить скорость проведения электрического импульса по нервным волокнам. В процессе транскраниальной магнитной стимуляции при помощи коротких магнитных импульсов стимулируется кора головного мозга. Оба метода наглядно показывают, какие нейродегенеративные процессы происходят в головном и спинном мозге на данном этапе патологического процесса. С помощью дополнительных методов исследования врачи проводят дифференциальную диагностику и определяют, какая нервная функция нарушена.
С помощью дополнительных методов исследования врачи проводят дифференциальную диагностику и определяют, какая нервная функция нарушена.
Диагноз БАС врачи клиники неврологии устанавливают при наличии следующих критериев:
- Признаков поражения периферического и центрального двигательного нейрона;
- Данных электрофизиологических и патоморфологических исследований;
- Прогрессирования болезни;
- Распространения симптомов в одной или нескольких зонах иннервации.
Знания и большой опыт работы, использование результатов новейших диагностических исследований позволяет неврологам Юсуповской больницы установить диагноз БАС на ранней стадии заболевания.
Лечение
Терапия БАС во многих случаях малоэффективна. Цель лечения – замедление прогрессирования симптомов заболевания, увеличение периода, в продолжении которого пациент сможет себя самостоятельно обслуживать и у него сохранятся жизненно важные функции.
Единственный препарат, который разрешён FDA (Американским Федеральным управлением по надзору за качеством пищевых и лекарственных препаратов), – рилутек, но он не зарегистрирован в РФ. Рилутек замедляет действие глутамата в клетках головного мозга, тем самым улучшает работу супероксиддисмутазы – 1. Препарат назначают пациентам пожизненно. Каждые три месяца врачи проводят мониторинг уровня печёночных трансаминаз. Для предотвращения гибели и улучшения роста нервных клеток больным боковым амиотрофическим склерозом выполняют трансплантацию стволовых клеток.
Для лечения БАС неврологи назначают пациентам следующие лекарственные препараты:
Прозерин – средство, препятствующее разрушению ацетилхолина в нейромышечных синапсах;
Ретаболил – анаболик, увеличивающий мышечную массу;
Витамины группы А, В, С – для улучшения проведения нервных импульсов.
При развитии инфекционных осложнений проводят терапию антибиотиками широкого спектра действия. Паллиативная терапия заключается в устранении дисфагии, дизартрии, мышечных спазмов, фасцикуляций, депрессии. В терминальной стадии болезни пациентам проводят эндоскопическую гастротомию, трахеостомию и искусственную вентиляцию лёгких. Врачи отделения реанимации и интенсивной терапии Юсуповской больницы благодаря наличию современной аппаратуры эффективно поддерживают все витальные функции пациента, что позволяет увеличить продолжительности его жизни.
Паллиативная терапия заключается в устранении дисфагии, дизартрии, мышечных спазмов, фасцикуляций, депрессии. В терминальной стадии болезни пациентам проводят эндоскопическую гастротомию, трахеостомию и искусственную вентиляцию лёгких. Врачи отделения реанимации и интенсивной терапии Юсуповской больницы благодаря наличию современной аппаратуры эффективно поддерживают все витальные функции пациента, что позволяет увеличить продолжительности его жизни.
Как улучшают качество жизни больного
При возникновении у больных боковым амиотрофическим склерозом проблем с пережёвыванием и глотанием пищи, следует готовить им жидкие и перемолотые блюда. Супы, каши можно взбивать блендером. Когда пациент утрачивает способность самостоятельно глотать пищу, хирурги Юсуповской больницы выполняют операцию гастростомию. После неё пищу вводят непосредственно в желудок через трубку, внедренную через стому в передней брюшной стенке. В некоторых случаях проводят парентеральное питание – смеси, которые содержат все необходимые ингредиенты, вводят внутривенно капельно.
При нарушении речи больные БАС утрачивают способность разговаривать. В этом случае они могут общаться с окружающими с помощью печатного устройства. Также с этой целью используют системы с автоматическими датчиками, которые расположены на глазных яблоках.
Если пациент утрачивает способность самостоятельного передвигаться, прибегают к ортопедическим приспособлениям, используют особую обувь, трости и коляски. Голову фиксируют специальным держателем. При прогрессировании болезни пациента следует обеспечить функциональной кроватью.
Прогноз
Прогноз для выздоровления пациентов, страдающих боковым амиотрофическим склерозом, пессимистичный. Терапия заболевания направлена на улучшение качества и увеличение продолжительности жизни пациента. Единственный препарат, который влияет на механизм развития заболевания, не ввозится в РФ. Наиболее неблагоприятный прогноз при высокой и бульбарной форме бокового амиотрофического склероза.
Уход и паллиативную терапию пациентам, страдающим БАС, проводят в клинике неврологии и хосписе Юсуповской больницы. Врачи отделения реанимации и интенсивной терапии с помощью современной аппаратуры поддерживают витальные функции пациента. Чтобы получить полную информацию о заболевании, стоимости лечения, записаться на консультацию невролога, звоните по номеру телефона контакт-центра. Он работает 24 часа в сутки без выходных и обеденного перерыва.
Врачи отделения реанимации и интенсивной терапии с помощью современной аппаратуры поддерживают витальные функции пациента. Чтобы получить полную информацию о заболевании, стоимости лечения, записаться на консультацию невролога, звоните по номеру телефона контакт-центра. Он работает 24 часа в сутки без выходных и обеденного перерыва.
Dermatomes — Physiopedia
Contents loading…
Editors loading…
Categories loading…
Ссылаясь на доказательства в академическом письме, вы всегда должны ссылаться на первичный (оригинальный) источник. Обычно это журнальная статья, в которой информация была впервые изложена. В большинстве случаев статьи Physiopedia являются вторичным источником и поэтому не должны использоваться в качестве ссылок. Статьи из Physiopedia лучше всего использовать для поиска первоисточников информации (см. список литературы внизу статьи).
Если вы считаете, что эта статья Physiopedia является основным источником информации, на которую вы ссылаетесь, вы можете использовать кнопку ниже, чтобы получить доступ к соответствующему заявлению о цитировании.
Перейти к:навигация, поиск
Оригинальный редактор — Люсинда Хэмптон
Ведущие участники — Special:Contributors/Dermatomes
Ведущие редакторы
Содержимое
- 1 Дерматомы
- 2 Назначение
- 3 Техника
- 4 Споры
- 5 Клиническое значение
- 6 Каталожные номера
Дерматом представляет собой участок кожи, который в основном иннервируется афферентными нервными волокнами от дорсального корешка одного спинномозгового нерва. Всего имеется 30 дематомов — 8 шейных нервов (обратите внимание на С1 без дерматома), 12 грудных нервов, 5 поясничных нервов и 5 крестцовых нервов. Каждый из этих корешков спинномозговых нервов передает ощущение от определенного участка кожи в мозг. [1] Дисфункция или повреждение корешка спинномозгового нерва в результате инфекции, сдавления или травматического повреждения может вызвать симптомы в соответствующем дерматоме. [2]
[2]
[3]
[4]
| Корень нерва | Дерматом | ||
|---|---|---|---|
| Шейный | С2 | Кожа шеи снабжения | Висок, лоб, затылок |
| С3 | Вся шея, задняя часть щеки, височная область, продолжение вперед под нижней челюстью | ||
| С4 | Плечевая область, ключичная область, верхняя лопаточная область | ||
| С5 | Поставка оружия | Дельтовидная область, передняя часть всей руки до основания большого пальца | |
| С6 | Передняя часть руки, лучевая сторона кисти до большого и указательного пальцев | ||
| С7 | Латеральная поверхность руки и предплечья до указательного, длинного и безымянного пальцев | ||
| С8 | Медиальная часть руки и предплечья к длинному, безымянному и мизинцу | ||
| Грудной отдел | Т1 | Медиальная сторона предплечья до основания мизинца | |
| Т2 | Снабжение грудной клетки и брюшной полости | От медиальной стороны плеча до медиальной части локтя, грудной и средней лопаточной областей | |
| Т3 — 6 | Верхняя часть грудной клетки | ||
| Т5 — 7 | Реберная граница | ||
| Т8 — 12 | Область живота и поясницы | ||
| Поясничный отдел | Л1 | Спина, над вертлугом и пахом | |
| Л2 | Спина, передняя часть бедра до колена | ||
| Л3 | Снабжение кожи ног | Спина, верхняя часть ягодиц, передняя часть бедра и колена, медиальная часть голени | |
| Л4 | Медиальная часть ягодицы, латеральная поверхность бедра, медиальная часть голени, тыльная поверхность стопы, большой палец ноги | ||
| Л5 | Ягодицы, задняя и латеральная поверхности бедра, латеральная сторона голени, тыльная поверхность стопы, медиальная половина подошвы, первый, второй и третий пальцы | ||
| Крестцовый | С1 | Ягодицы, бедра и задние конечности | |
| С2 | Снабжение паха | То же, что и S1 | |
| С3 | Пах, медиальная часть бедра до колена | ||
| С4 | Промежность, половые органы, нижняя часть крестца | ||
| Копчиковый | Дерматом, соответствующий копчиковым нервам, расположен на ягодицах, в области непосредственно вокруг копчика. [5] [6] [5] [6] | ||
Исследование дерматомов является частью неврологического обследования. Они в основном используются для определения того, соответствует ли потеря чувствительности на конечности одному сегменту позвоночника, что подразумевает поражение этого нервного корешка (т. е. радикулопатия), и для определения неврологического «уровня» поражения спинного мозга [7] .
Дерматом Тестирование лучше всего проводить с помощью булавки и ваты. Попросите пациента закрыть глаза и дайте терапевту обратную связь относительно различных раздражителей. Тестирование должно проводиться на конкретных дерматомах и должно сравниваться с двусторонним.
- Тест на легкое прикосновение — Ощущение легкого прикосновения — Нанесите кусочек ваты на участок кожи [8]
- Тест на укол булавкой — Ощущение боли — Аккуратно коснитесь кожи булавкой, спросите пациента, ощущается ли она острой или тупой
Во время обзора систем пациента просят подробно описать характер или распределение сенсорных симптомов (например, покалывание, онемение, ослабление или отсутствие чувствительности), чтобы дать терапевту предварительную информацию, которая поможет направить обследование и помочь в идентификации пораженного дерматома(ов) и нерва(ов).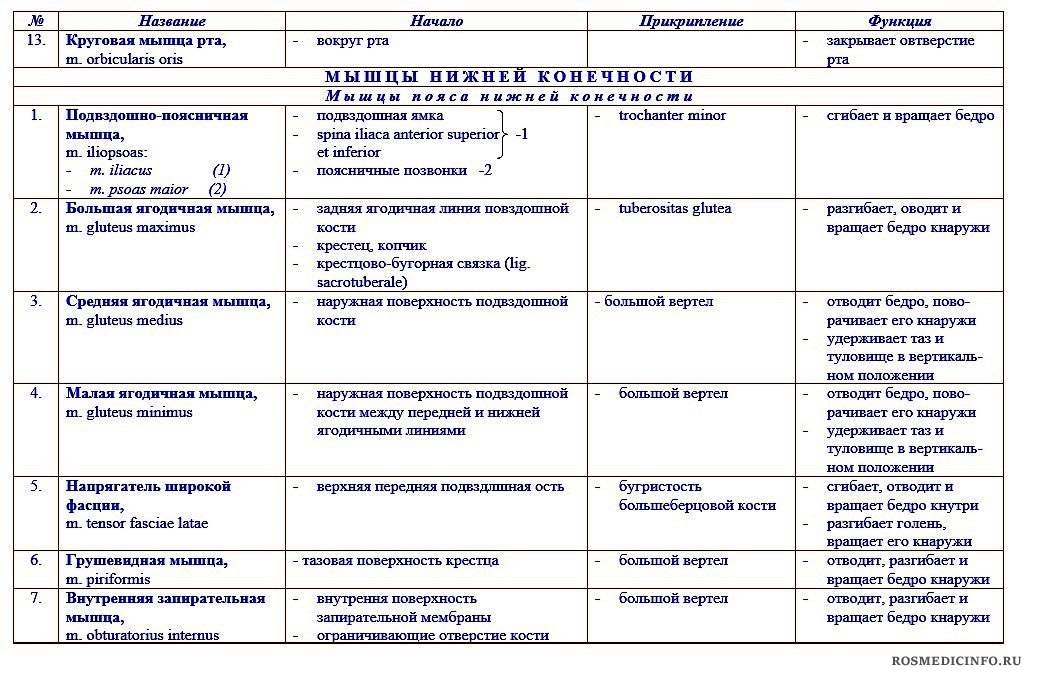 [9]
[9]
Дерматомы легкого прикосновения больше, чем дерматомы боли. Когда поражены только один или два сегмента, проверка болевой чувствительности является более чувствительным методом исследования, чем проверка на легкое прикосновение. [7]
Дерматомы имеют сегментированное распределение по всему телу. Точный рисунок дерматома может варьироваться от человека к человеку. Также может происходить некоторое перекрытие между соседними дерматомами. Существуют некоторые расхождения между опубликованными картами дерматомов, основанными на методологиях, используемых для определения иннервации сегментов кожи. В клиническом комментарии Даунс и Лапорт обсуждают историю картирования дерматомов, включая различия в используемых методологиях и несоответствия в картах дерматомов, используемых в обучении и практике. [9] [[Laporte C. Противоречивые карты дерматомов: образовательные и клинические значения. журнал ортопедической и спортивной физиотерапии. 2011 Jun;41(6):42 [10] 7-34.]]
2011 Jun;41(6):42 [10] 7-34.]]
Дерматомы важны, поскольку они могут помочь в оценке и диагностике различных состояний. Неврологическая оценка дерматомов помогает оценить модели потери чувствительности, которые могут указывать на специфическое поражение спинномозговых нервов. Например, симптомы, возникающие вдоль определенного дерматома, могут указывать на нарушение или повреждение определенного нервного корешка в позвоночнике.
- Защемление нерва
- Радикулопатия
- Травма спинного мозга
- Herpes Zoster (опоясывающий лишай) [2]
- ↑ Википедия Дерматом. Доступно по адресу: https://en.wikipedia.org/wiki/Dermatome_(anatomy) (последний доступ 23 апреля 2019 г.)
- ↑ 2.0 2.1 Медицинские новости сегодня Что и где дерматомы? Доступно: https://www.
 medicalnewstoday.com/articles/what-are-dermatomes (по состоянию на 25.05.2022)
medicalnewstoday.com/articles/what-are-dermatomes (по состоянию на 25.05.2022) - ↑ М Рёрс. Дерматомы. Доступно по адресу: https://www.youtube.com/watch?v=CYZBH6NX8wg&feature=youtu.be (последний доступ 23 апреля 2019 г.)
- ↑ Обзор дерматомов — © Kenhub — иллюстратор: Ирина Мюнстерманн https://www.kenhub.com/en/library/anatomy/dermatomes
- ↑ Медицинские новости сегодня Что и где дерматомы? Доступно: https://www.medicalnewstoday.com/articles/what-are-dermatomes (по состоянию на 25.05.2022)
- ↑ Дэвид Дж. Маги. Ортопедическая физическая оценка. 6-е издание. Эльзевир. 2014.
- ↑ 7.0 7.1 Либенсон К., изд. Реабилитация позвоночника: руководство для практикующего врача. Липпинкотт Уильямс и Уилкинс; 2007. Доступно: https://www.sciencedirect.com/topics/medicine-and-dentistry/dermatome (по состоянию на 25 мая 2022 г.)
- ↑ Поделиться слайдом. Дерматомы и миотомы. Доступно по адресу: https://www.slideshare.net/TafzzSailo/special-test-for-dermatomes-and-myotomes (последний доступ 23 апреля 2019 г.
 )
) - ↑ 9.0 9.1 Сьюзан Б.О’Салливан, Томас Дж. Шмитц, Джордж Д. Фулк. Физическая реабилитация. 6-е издание. Компания Ф. А. Дэвиса. 2014.
- ↑ Даунс М.Б., Лапорт С. Конфликтующие карты дерматомов: образовательные и клинические последствия. журнал ортопедической и спортивной физиотерапии. 2011 июнь;41(6):427-34.
Клинические рекомендации (сестринское дело): Нейроваскулярные наблюдения
Введение
Задержка в распознавании нейроваскулярного нарушения может привести к необратимому дефициту, потере конечности и даже смерти, поэтому оценка сосудисто-нервного статуса необходима для раннего распознавания ухудшения или нарушения сосудисто-нервного аппарата .
Цель
Цель этого руководства по медицинскому уходу состоит в том, чтобы наметить необходимую нейроваскулярную оценку для раннего выявления нарушений и предотвращения необратимого повреждения конечностей.
Определение терминов
- Активное движение : Способность произвольно разгибать и сгибать конечность или палец.

- Наполнение капилляров : Это оценка возврата артериального кровоснабжения. Его оценивают путем сильного нажатия на ногтевое ложе пальцев рук или ног, кратковременного прерывания кровоснабжения в капиллярной системе, вызывающего побледнение ногтевого ложа, и определения времени, необходимого для возвращения крови. Цвет должен вернуться в течение 2-3 секунд после сброса давления.
- Компартмент-синдром : Увеличение давления в закрытом мышечном компартменте, вызывающее ишемию мышц и нервов.
- Непропорциональная боль : Боль, превышающая ожидаемую после травмы или хирургического вмешательства, которая не снимается анальгезией.
- Фасциотомия : Хирургический разрез, сделанный через фасцию в мышечный компартмент из-за повышения давления на ткани. Целью этой процедуры является снижение давления для улучшения периферического сосудисто-нервного статуса и предотвращения долгосрочных осложнений
- Мышечный отдел : Четко определенное пространство в теле, состоящее из группы мышц, нервов и кровеносных сосудов в определенном сегменте.
 Мышечный компартмент ограничен фасцией, тканью, которая не растягивается и не расширяется и удерживает компартмент на месте. Например, нижняя часть ноги содержит четыре мышечных блока.
Мышечный компартмент ограничен фасцией, тканью, которая не растягивается и не расширяется и удерживает компартмент на месте. Например, нижняя часть ноги содержит четыре мышечных блока. - Опорно-двигательный аппарат : Структурно включает сочетание мышц, костей, сухожилий, связок, суставов и хрящей.
- Нервно-сосудистая система : Структура и функция сосудистой и нервной систем в сочетании.
- Пассивное движение : Оценивает способность разгибать и сгибать конечность или палец.
Оценка
Критерии для оценки сосудисто-нервного аппарата
Пациенты, которым требуется оценка сосудисто-нервного характера, включают, но не ограничиваются:
- Скелетно-мышечные травмы конечностей
- Перелом
- Размозжение
- Послеоперационный
- Внутренняя или внешняя фиксация перелома
- Ортопедическая хирургия
- Хирургия позвоночника
- Пластические операции на конечностях или фалангах пальцев
- Катетеризация сердца
- Жгут применяется в течение длительного времени
- Наложение гипсовой повязки
- Ограничительная повязка
- Ограничительная повязка
- Применение тяги
- Кожа и скелет
- Кожа и скелет
- Ожоговые больные
- Окружные ожоги
- Окружные ожоги
- Признаки инфекции конечности
Периодичность наблюдений
- 1 раз в час в течение первых 24 часов после травмы, операции или наложения гипсовой повязки.

- Затем каждые 4 часа в течение следующих 48 часов или по указанию лечащей медицинской бригады.
- Чаще при любых отклонениях от базовых наблюдений. Частота должна быть указана лечащей медицинской бригадой.
Для частоты
наблюдений за пациентами с сердечным катетером см. Клинические рекомендации по уходу за пациентом после катетеризации сердца.
Нейроваскулярная оценка
Нервно-сосудистая оценка требуется для каждой пораженной конечности и включает оценку:
- Боль
- ощущение
- Двигательная функция
- Перфузия
Боль
Наиболее важным показателем нейроваскулярного нарушения является боль, непропорциональная травме. Боль, связанная с компартмент-синдромом, как правило, постоянна, однако усиливается при пассивных движениях в направлении разгибания и не купируется опиоидной анальгезией. Признаки боли у невербальных пациентов включают беспокойство, гримасничанье, настороженность, тахикардию, гипотонию, тахипноэ и/или потливость. Если боль непропорциональна травме, следует немедленно связаться с медицинской бригадой.
Признаки боли у невербальных пациентов включают беспокойство, гримасничанье, настороженность, тахикардию, гипотонию, тахипноэ и/или потливость. Если боль непропорциональна травме, следует немедленно связаться с медицинской бригадой.
См. Клиническое руководство по оценке и измерению боли для получения дополнительной информации об оценке боли у детей.
Чувствительность и двигательная функция
При нарушении нейроваскулярного статуса пациенты могут жаловаться на снижение чувствительности, потерю чувствительности, дизестезию, онемение, покалывание или покалывание. Изменение чувствительности может быть результатом блокады нерва или эпидуральной анестезии. Если это так, то это должно быть задокументировано при нейроваскулярной оценке пациента в
схемы в EMR.
При оценке двигательной функции следует отметить величину боли при движении в пораженной конечности, в том числе, если это была боль при активном или пассивном движении. Крайне важно сравнивать движение пальцев на двусторонней основе и с базовыми наблюдениями, поскольку некоторые
пациенты могли иметь ограниченные движения или вообще не двигаться до травмы.
Крайне важно сравнивать движение пальцев на двусторонней основе и с базовыми наблюдениями, поскольку некоторые
пациенты могли иметь ограниченные движения или вообще не двигаться до травмы.
В таблице ниже показано, как оценивать чувствительность и двигательную функцию каждого нерва в руках и ногах.
Цвет, температура, капиллярное наполнение, отек и пульс должны быть оценены при завершении нейроваскулярной оценки. Нервно-сосудистые нарушения могут привести к неадекватному артериальному кровоснабжению (уменьшение кровотока из артерий к периферии пораженной конечности) или неадекватному венозному возврату (снижение кровотока).
от периферии пораженной конечности к сердцу), что приводит к изменению этих показателей.
Пожалуйста, обратитесь к таблице ниже, чтобы определить показатели нормальной перфузии, неадекватного артериального кровоснабжения и неадекватного венозного возврата. Об изменениях перфузии следует немедленно сообщать медицинской бригаде.
Об изменениях перфузии следует немедленно сообщать медицинской бригаде.
Документация
Исходная оценка сосудисто-нервного аппарата обеих конечностей необходима для выявления нарушений сосудисто-нервного характера. Нейроваскулярные наблюдения для верхних и нижних конечностей могут быть добавлены в технологические схемы в EMR для документирования через вкладку заказов.
Изменения в нейроваскулярном статусе должны быть задокументированы в технологических картах, и медицинская бригада должна быть немедленно уведомлена. Фотографии могут быть сделаны с согласия лиц, осуществляющих уход, и/или пациента (в зависимости от возраста) и сохранены в медиафайле в EMR для документирования любых изменений в нейроваскулярном статусе и позволяют медицинским бригадам просматривать
прогресс. См. клинические изображения
Политика.
Ведение
Если есть подозрение на нейроваскулярную недостаточность или ухудшение состояния, заполните приведенные ниже многоточия, ожидая срочного осмотра медицинской бригадой.
Лечение нейроваскулярного нарушения
- Поднимите конечность не выше уровня сердца. Нижние конечности можно приподнять с помощью подушек или с помощью механики кровати. Верхние конечности можно поднимать на подушке, слинге или коробчатом слинге.
- Раздельные гипсовые повязки с одобрения лечащей бригады или разрезание/удаление повязок.
- Поддерживайте выравнивание конечностей.
- Увеличить частоту нейроваскулярных наблюдений (частота определяется лечащей бригадой).
- Немедленно уведомить лечащую бригаду.
Если сосудисто-нервный статус улучшается, держите пораженную конечность в приподнятом положении и продолжайте тщательное наблюдение.
Если сосудисто-нервный статус не улучшается или продолжает ухудшаться, пациенту может потребоваться посещение операционной для контроля давления и/или фасциотомии.
Для пациентов с сердечным катетером:
Если выявляются какие-либо изменения в нейроваскулярных наблюдениях (т.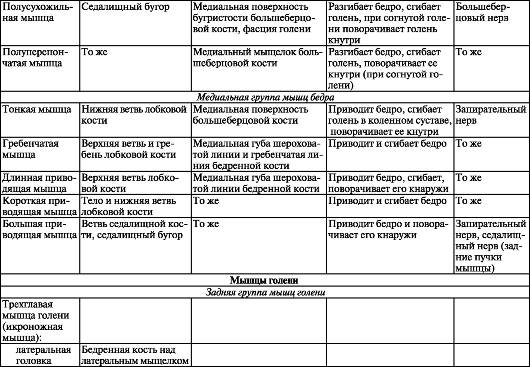 е. снижение пульсового давления, изменение цвета конечностей или цвета конечностей), о результатах следует сообщить лечащей бригаде или специалисту по катетеризации. Подумайте о необходимости УЗИ
подтвердить или исключить тромб.
См. Руководство по уходу за пациентом после катетеризации сердца.
е. снижение пульсового давления, изменение цвета конечностей или цвета конечностей), о результатах следует сообщить лечащей бригаде или специалисту по катетеризации. Подумайте о необходимости УЗИ
подтвердить или исключить тромб.
См. Руководство по уходу за пациентом после катетеризации сердца.
Компартмент-синдром
Компартмент-синдром — серьезное осложнение скелетно-мышечной травмы. Пациенты с высоким риском компартмент-синдрома включают открытые переломы, высокоэнергетические травмы, одновременные переломы плечевой кости и предплечья, размозженные травмы и наложение тугих повязок и/или гипсовых повязок. Компартмент-синдром возникает в результате увеличения
давление внутри компартмента, состоящего из мышц и нервов и окруженного фасцией. Фасция неэластична и не расширяется для увеличения объема или давления. Когда давление в компартменте увеличивается, нервы и мышцы сдавливаются, что приводит к снижению кровотока и перфузии тканей, мышц и
ишемия нерва и потеря или изменение чувствительности, поэтому важно раннее выявление и вмешательство.
Компартмент-синдром требует неотложной хирургической помощи. Чтобы уменьшить давление или уменьшить объем внутри компартмента, хирургический разрез, известный как фасциотомия, делается через фасцию и в пораженный мышечный компартмент. Это сохранит приток крови к ишемическим мышцы и нервы, тем самым предотвращая долговременные нервно-мышечные осложнения, такие как мышечный фиброз, атрофия, контрактуры и деформации.
Признаки компартмент-синдрома включают «5 Ps», как указано ниже:
- Боль: Боль, непропорциональная травме, сильная боль при пассивных движениях и боль, не купируемая опиоидной анальгезией, является первым и наиболее достоверным признаком компартмент-синдрома.
- Парестезии: Возникает в результате сдавления нерва и обычно проявляется покалыванием, покалыванием или онемением.
- Бледность: Указывает на артериальную недостаточность ниже уровня повреждения. Ниже уровня травмы будет ощущаться холодность на ощупь и бледность.
- Паралич: Обычно является поздним признаком компартмент-синдрома и возникает в результате длительного сдавления нерва или повреждения мышц. Паралич проявляется неспособностью активно двигать конечностью и усилением боли при пассивном движении, которая не уменьшается при разгибании.
- Безимпульсный: Отсутствие пульса является поздним признаком и указывает на отмирание тканей.
Дополнительные признаки компартмент-синдрома включают:
- Температура: Похолодание конечности дистальнее места повреждения указывает на снижение артериального кровоснабжения.
- Капилляр Сменный блок: Указывает на перфузию конечностей. Капиллярное наполнение более 3 секунд указывает на неадекватную перфузию конечностей.
- Отек и Повышенное давление: В результате повышенного внутрикамерного давления кожа становится стянутой и блестящей.
При подозрении на компартмент-синдром следует немедленно связаться с медицинской бригадой для осмотра.
Информация для лиц, осуществляющих уход,
Во время госпитализации лица, осуществляющие уход, и пациенты должны быть проинформированы о важности проведения нейроваскулярной оценки и о том, почему необходимо продолжать наблюдение, даже когда пациент спит.
Многие пациенты с риском нарушения сосудисто-нервной системы покидают больницу до того, как исчезнет риск компартмент-синдрома, поэтому крайне важно проводить обучение при выписке об оценке сосудисто-нервного характера. Лица, осуществляющие уход, должны быть осведомлены о признаках и симптомах нервно-сосудистые нарушения, и когда вернуться к своему терапевту или RCH, если они обеспокоены. Кроме того, пациенту должно быть предоставлено соответствующее возрасту образование, в том числе поощрение пациента к регулярному шевелению пальцами.
Для кардиологических
катетерные пациенты: См. Руководство по уходу за пациентом после катетеризации сердца.
Ссылки
- Рекомендации по уходу
- Клинические рекомендации (сестринское дело): оценка боли и лечение
- Клинические рекомендации (сестринское дело): уход за пациентом после катетеризации сердца
- Информация о здоровье детей
- Информация о здоровье детей: уход за гипсовой повязкой
- Информация о здоровье детей: уход за ранами
Таблица доказательств
Нажмите
здесь, чтобы просмотреть таблицу доказательств для этого руководства.