Триглицериды
Триглицериды – жиры, один из основных источников энергии для клеток организма. Повышение их уровня увеличивает риск заболевания сердца и сосудов, а также риск развития острого панкреатита.
Синонимы русские
Липиды крови, нейтральные жиры, ТГ.
Синонимы английские
TG, Trig, Triglycerides.
Метод исследования
Колориметрический фотометрический метод.
Единицы измерения
Ммоль/л (миллимоль на литр).
Какой биоматериал можно использовать для исследования?
Венозную кровь.
Как правильно подготовиться к исследованию?
- Не принимать пищу в течение 12 часов до исследования.
- Исключить физическое и эмоциональное перенапряжение и не курить 30 минут до исследования.
Общая информация об исследовании
Триглицериды – это жиры, которые являются основным источником энергии для организма.
Так как триглицериды нерастворимы в воде, они переносятся в крови с белком в виде комплекса, который называется липопротеином. Есть несколько типов липопротеинов, различающихся пропорциями входящих в их состав компонентов:
- липопротеины очень низкой плотности (ЛПОНП),
- липопротеины низкой плотности (ЛПНП),
- липопротеины высокой плотности (ЛПВП).
Большинство триглицеридов в организме переносятся липопротеинами очень низкой плотности (ЛПОНП).
Увеличение количества триглицеридов повышает риск развития сердечно-сосудистых заболеваний, хотя их причины до конца не выяснены.
Кроме того, триглицериды значительно повышают риск развития острого воспаления поджелудочной железы – острого панкреатита.
Для чего используется исследование?
- Чтобы оценить риск развития атеросклероза и проблем с сердцем и сосудами. Атеросклероз – процесс роста внутри сосудов бляшек, которые могут ограничивать кровоток или полностью перекрывать просвет сосуда.
- Для контроля за эффективностью диеты со сниженным количеством животных жиров и наблюдения за уровнем липидов крови после назначения препаратов, снижающих уровень триглицеридов и холестерола (холестерина).
Когда назначается исследование?
- Вместе с тестом на общий холестерол или в составе липидограммы, которая также включает определение уровня ХС ЛПНП, ХС ЛПОНП, ХС ЛПВП, триглицеридов и коэффициента атерогенности.
 Липидограмму рекомендуется сдавать всем взрослым старше 20 лет не реже одного раза в 5 лет.
Липидограмму рекомендуется сдавать всем взрослым старше 20 лет не реже одного раза в 5 лет. - При плановых профилактических осмотрах или чаще (несколько раз в год), если человеку предписана диета с ограничением приема животных жиров и/или он принимает лекарства, снижающие уровень триглицеридов и холестерола. В этих случаях проверяют, достигается ли целевой уровень липидов и, соответственно, снижается ли риск сердечно-сосудистых заболеваний.
- Особенно важно проверять триглицериды при сахарном диабете, так как колебания уровня сахара способствует повышению триглицеридов.
- Если в жизни пациента присутствует один или несколько факторов риска развития сердечно-сосудистых заболеваний:
- курение,
- возраст (мужчины старше 45 лет, женщины старше 55 лет),
- повышенное артериальное давление (140/90 мм. рт. ст и выше),
- повышенный холестерол или сердечно-сосудистые заболевания у других членов семьи (инфаркт или инсульт у ближайшего родственника мужского пола моложе 55 лет или женского моложе 65 лет),
- ишемическая болезнь сердца, инфаркт сердечной мышцы или инсульт,
- сахарный диабет,
- избыточная масса тела,
- злоупотребление алкоголем,
- прием большого количества пищи, содержащей животные жиры,
- низкая физическая активность.

- Если у ребенка в семье были случаи повышенного холестерола или заболеваний сердца в молодом возрасте, то впервые анализ на холестерол рекомендуется сдавать в возрасте от 2 до 10 лет.
Что означают результаты?
Референсные значения (норма триглицеридов):
Согласно клиническим рекомендациям1, уровень
«Диагностика и коррекция нарушений липидного обмена с целью профилактики и лечения атеросклероза. Российские рекомендации, VII пересмотр. 2020».
«2019 ESC/EAS Guidelines for the management of dyslipidaemias: lipid modification to reduce cardiovascular risk».
Интерпретация результатов должна производиться с учетом других анализов, входящих в липидограмму.
Причины повышения уровня триглицеридов (гипертриглицеридемии)
Гипертриглицеридемия может быть результатом наследственной предрасположенности или избыточного приема с пищей животных жиров. У большинства людей с повышенным холестерином в той или иной мере задействованы оба фактора.
Перед назначением лечения необходимо исключить другие причины повышенного содержания триглицеридов:
- алкоголизм,
- хроническое воспаление почек, приводящее к нефротическому синдрому,
- хроническая почечная недостаточность,
- снижение функции щитовидной железы (гипотиреоз),
- плохо вылеченный сахарный диабет,
- панкреатит,
- инфаркт миокарда – в этом случае повышенные уровни могут сохраняться до нескольких месяцев,
- подагра.
Пониженный уровень триглицеридов (гипотриглицеридемия) особого клинического значения не имеет. Может встречаться при следующих состояниях:
- наследственная гиполипропротеинемия,
- повышение функции щитовидной железы (гипертиреоз),
- нарушения всасывания в кишечнике,
- хроническая обструктивная болезнь легких,
- инфаркт мозга.
Что может влиять на результат?
Уровень триглицеридов может оставаться значительно (до 5-10 раз) повышенным даже через несколько часов после приема пищи.
Показатели проб крови, взятой натощак в разное время, также могут быть неодинаковыми. У некоторых людей уровень триглицеридов меняется на 40 % в течение одного месяца. Это явление называется биологической вариацией и отражает нормальные колебания метаболизма холестерола в организме. В итоге единичное измерение не всегда отражает «обычный» уровень триглицеридов, поэтому иногда требуется пересдача анализа.
Повышают уровень триглицеридов:
- богатая жирами пища,
- прием алкоголя,
- беременность (анализ следует сдавать по меньшей мере через 6 недель после родов),
- оральные контрацептивы, холестирамин, фуросемид, верошпирон, кордарон, кортикостероиды.
Снижают уровень триглицеридов:
- интенсивная физическая нагрузка,
- статины, метформин.
Важные замечания
- Анализ на триглицериды необходимо сдавать, когда человек относительно здоров. После острого заболевания, инфаркта, хирургической операции необходимо подождать как минимум 6 недель.

- Убедительных доказательств того, что снижение уровня триглицеридов уменьшает риск развития сердечно-сосудистых заболеваний, пока нет. Однако у тех, у кого ХС ЛПНП выше нормы или ХС ЛПВП ниже нормы, повышенный уровень триглицеридов увеличивает риск развития ишемической болезни сердца.
- В США липиды измеряются в миллиграммах на децилитр, в России и в Европе – в миллимолях на литр. Пересчет осуществляется по формуле: ТГ (мг/дл) = ТГ (ммоль/л) × 88,5 или ТГ(ммоль/л) = ТГ (мг/дл) х 0,0113.
Также рекомендуется
- Холестерол общий
- Холестерол – липопротеины высокой плотности (ЛПВП)
- Холестерол – липопротеины низкой плотности (ЛПНП)
- Коэффициент атерогенности
- Аполипопротеин A1
- Аполипопротеин B
Кто назначает исследование?
Врач общей практики, терапевт, кардиолог.
Триглицериды ( в крови )
Мы на связи: (056)744-46-83, (056)744-11-07, (068)205-93-94
RU / ENG / UA
Триглицериды – одна из основных форм (наряду с холестерином) депонирования жиров в организме, потенциальный источник энергии.
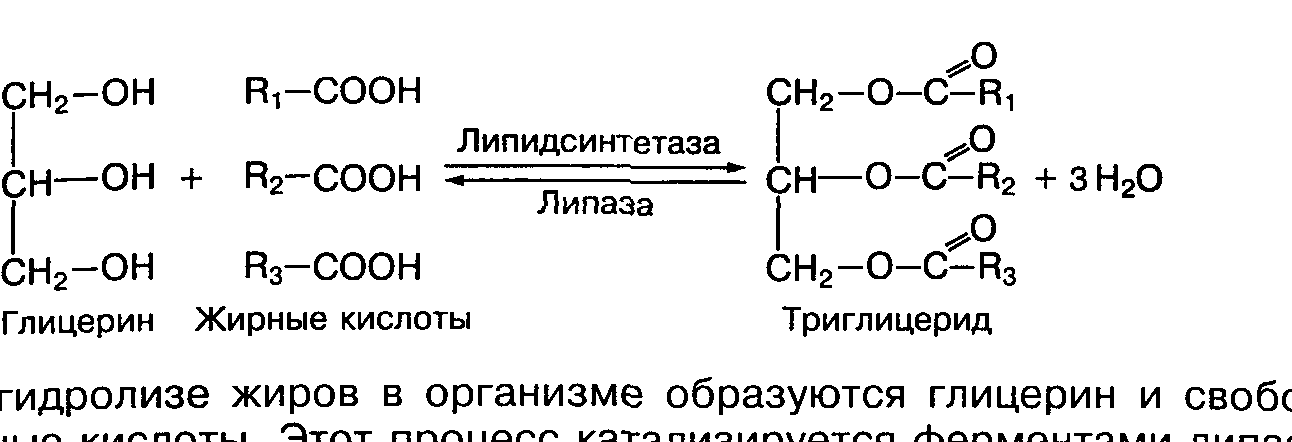
Триглицериды (нейтральные жиры) — это эфиры трехатомного спирта глицерина и высших жирных кислот (стеариновой, линолевой, линоленовой, пальмитиновой и др.). Это жиры, присутствующие в жировых тканях и входящие в состав растительных масел. Поступают в организм человека с пищей, перевариваются до жирных кислот и глицерола и всасываются в тонком кишечнике. Ресинтез так называемых «пищевых» триглицеридов происходит в клетках эпителия тонкого кишечника, далее они включаются в состав одного из видов липопротеинов – хиломикронов — и в таком виде транспортируются к тканям. Липопротеины расщепляются липопротеин-липазами, продуцирующимися разными клетками. Освобождающиеся жирные кислоты в жировых клетках ресинтезируются в триглицериды, в мышечных клетках они используются как источник энергии. Жировая ткань депонирует триглицериды (особенно при избыточном поступлении калорий и сниженном расходовании энергии). При необходимости в процессе гидролиза триглицериды расщепляются до глицерина и жирных кислот, давая при утилизации в два раза больше калорий на 1 г массы, чем углеводы и белки.
В большинстве случаев повышение уровня трилицеридов («хилез» крови) является следствием особенностей диеты. Вторичная триглицеридемия часто наблюдается при сахарном диабете, злоупотреблении алкоголем, почечной недостаточности. Довольно редко увеличение концентрации триглицеридов может быть следствием наследственных нарушений липидного метаболизма и значения тогда в десятки раз могут превышать верхний предел референсных значений. Уровень триглицеридов крови значительно колеблется в течение дня. После приема пищи через 15-30 мин их содержание в сыворотке крови увеличивается и только через 9-12 ч возвращается к исходному уровню, поэтому определение уровня триглицеридов необходимо проводить натощак, обычно после ночного периода голодания. Содержание триглицеридов также в значительной степени зависит от возраста.
Показания к назначению анализа «Триглицериды»
- Диагностика первичных и вторичных нарушений метаболизма липидов.
- В комплексе анализов липидного профиля для оценки риска атеросклероза и его осложнений.
Подготовка к исследованию
Взятие крови утром строго натощак, через 12-14 часов после последнего приема пищи. Накануне принятая пища не должна содержать жиры животного происхождения, а также исключается молочная пища. За три дня до исследования исключить прием алкоголя.
Материал для исследования: сыворотка крови.
Метод определения: ферментативный с липазой и пероксидазой.
Единицы измерения: ммоль/л.
Референтные значения ( Триглицериды — норма ):
до 10 лет женщины 0,40 – 1,24 ммоль/л;
мужчины 0,34 – 1,13 ммоль/л;
10 – 15 лет женщины 0,42 – 1,48 ммоль/л;
мужчины 0,36 – 1,41 ммоль/л;
15 — 20 лет женщины 0,40 – 1,53 ммоль/л;
мужчины 0,45 – 1,81 ммоль/л;
20 — 25 лет женщины 0,41 – 1,48 ммоль/л;
мужчины 0, 50 – 2,27 ммоль/л;
25 — 30 лет женщины 0,42 – 1,63 ммоль/л;
мужчины 0,52 – 2,81 ммоль/л;
30 — 35 лет женщины 0,44 – 1,70 ммоль/л;
мужчины 0,56 – 3,01ммоль/л;
35 — 40 лет женщины 0,45 – 1,99 ммоль/л;
мужчины 0,61 – 3,62 ммоль/л;
40 — 45 лет женщины 0,51 – 2,16 ммоль/л;
мужчины 0,62 – 3,61 ммоль/л;
45 — 50 лет женщины 0,52 – 2,42 ммоль/л;
мужчины 0,65 – 3,70 ммоль/л;
50 — 55 лет женщины 0,59 – 2,63 ммоль/л;
мужчины 0,65 – 3,61 ммоль/л;
55 — 60 лет женщины 0,62 – 2,96 ммоль/л;
мужчины 0,65 – 3,23 ммоль/л;
60 — 65 лет женщины 0,63 – 2,70 ммоль/л;
мужчины 0,65 – 3,29 ммоль/л;
>65 лет женщины 0,68 – 2,71 ммоль/л;
мужчины 0,62 – 2,94 ммоль/л.
Повышение значений Триглицеридов
Первичные гиперлипидемии: гиперлипопротеинемии I, Ib, III, IV и V типов, вызванные семейной или спорадической эндогенной гипертриглицеридемией, семейная дисбеталипопротеидемия, наследственный дефицит липопротеинлипазы, семейная комбинированная гиперлипидемия, дефицит кофактора липопротеидлипазы, эрозивные или плоские ксантомы.
Вторичные гиперлипидемии:
- Ожирение.
- Нарушение толерантности к глюкозе.
- Поражения печени: цирроз печени, вирусные гепатиты, обтурация желчевыводящих путей.
- Острый и хронический панкреатит.
- Нефротический синдром, хроническая почечная недостаточность.
- Сердечно-сосудистые заболевания: острый инфаркт миокарда, артериальная гипертония, хроническая ишемическая болезнь сердца, тромбоз сосудов головного мозга.
- Гипотиреоз.
- Сахарный диабет.
- Подагра.
- Беременность.
- Гликогенозы I, III и IV типов.
- Большая талассемия.

- Синдром Дауна.
- Респираторный дистресс-синдром.
- Невротическая анорексия.
- Идиопатическая гиперкальциемия.
- Острая перемежающаяся порфирия.
- Стресс.
- Высококалорийная пища, диета с высоким содержанием углеводов.
- Прием таких препаратов, как холестирамин, бета-блокаторы, эстрогены, кортикостероиды, диуретики и т.д.
- Алкоголизм.
Снижение значений Триглицеридов
- Гиполипопротеинемия.
- Гипертиреоз.
- Гиперпаратиреоз.
- Недостаточность питания.
- Синдром нарушенного кишечного всасывания (мальабсорбция).
- Лимфагиэктазия кишечника.
- Хронические обструктивные заболевания легких.
- Прием холестирамина, гепарина, витамина С, прогестинов.
Стоимость исследования «Триглицериды»
Консультация врача-лаборанта
Отзывы
В настоящее время я житель Крыма, узнал о уникальных методах лечения в Клинике приехал сюда с проблемными. ..
..
окулисту Ольге Валентиновне оргромадное спасибо за консультацию — очень хороший врач — посоветую всем!
Я пришла в КДК с болью в суставах, выраженным варикозом, жалобами на работу желудка.
После проведения…
У меня так получилось, что я уже падала с ног. У меня были проблемы со щитовидной железой, сильно болели кости,…
Болею я давно. Сильно болят суставы, беспокоит щитовидная железа. Суставы болят и при нагрузке и в состоянии…
Я 35 лет проработала преподавателем медицинской академии, более 10 лет страдаю ревматоидным артритом….
Попал я в клинику с проблемами поджелудочной железы. Пройдя диагностику и курс лечения остался доволен и…
хочу выразить сердечную благодарность Юрию Николаевичу Куликовичу за создание такой клиники, за доброе…
Мы приехали из далека, и очень тронуты заботой и вниманием которыми нас окружили в Клинике. Большое спасибо,…
Обратиться в клинику меня заставили жалобы на опорно двигательный аппарат, болели коленные, тазобедренные. ..
..
Обратиться в клинику меня заставили жалобы на опорно двигательный аппарат, болели коленные, тазобедренные…
Хочу высказать благодарность всему коллективу Клиники Куликовича, за оказанную мне помощь в лечении, в…
Первое, что впечатлило — это фешенебельность, но ведь это оболочка. Самое главное, что в процессе лечения я…
Очень благодарна людям, которые здесь работают за доброту и тепло, что они излучают, за отношение, которое…
Сердечно выражаю благодарность всему персоналу клиники за теплое профессиональное отношение к пациенту, за…
Я, медработник с 17ти летним стажем работы. Работаю в ЦРБ г.Верхнеднепровска. До сегодняшнего дня в частных…
От всей души хочу выразить слова благодарности за чуткое отношение и профессиональное лечение всему…
От всей души благодарю, Доктора Куликовича Ю.Н., за создание современного центра отечественной медицины….
Выношу огромную благодарность товю Куликовичу Юрию Николаевичу и медперсоналу за чуткость и постоянную. ..
..
Врач выбирает метод лечения в соответствии с характером болезни, — целитель в соответствии с характером…
Я пришла в «Клинику доктора Куликовича» с болью в пояснице и между лопатками. За 8 лечебных сеансов боль…
Выражаю благодарность доктору Куликовичу Юрию Николаевичу и его медперсоналу врачам и сестрам за…
Все отзывы
Поиск по сайту
Next image Enlarge Close Play Slideshow Stop Slideshow Previous image |
Определение и примеры триглицеридов — Биологический онлайн-словарь
Словарь > Триглицерид
Определение
сущ. во множественном числе: триглицериды
Богатое энергией соединение, состоящее из одной молекулы глицерина и трех молекул жирной кислоты, служит основным компонентом животных и растительных масел и жиров
Дополнение
Триглицерид представляет собой богатое энергией соединение и служит для хранения энергии. Он состоит из глицерина и трех жирных кислот. Все три гидроксильные группы глицерина в триглицериде этерифицированы. Триглицерид является основным компонентом животных и растительных масел и жиров. У растений они являются второстепенным компонентом клеточной мембраны растений, а жирные кислоты в основном ненасыщенные. У животных жирнокислотный компонент в значительной степени насыщен.
Он состоит из глицерина и трех жирных кислот. Все три гидроксильные группы глицерина в триглицериде этерифицированы. Триглицерид является основным компонентом животных и растительных масел и жиров. У растений они являются второстепенным компонентом клеточной мембраны растений, а жирные кислоты в основном ненасыщенные. У животных жирнокислотный компонент в значительной степени насыщен.
Триглицериды животного происхождения являются важным источником энергии и присутствуют в жировых тканях, кровотоке и сердечной мышце. Триглицериды клинически измеряются и контролируются. Это связано с тем, что повышенный уровень триглицеридов коррелирует с повышенным риском атеросклероза, гипертонии, диабета, сердечных заболеваний и инсульта. Соответственно, нормальный уровень триглицеридов в крови составляет от 10 до 150 миллиграммов на децилитр. Повышение уровня триглицеридов (особенно в связи с повышенным уровнем холестерина) коррелирует с развитием атеросклероза, основной причиной сердечных заболеваний и инсульта.
Триглицериды иногда называют «жирами» , поскольку они относятся к триглицеридам, которые обычно находятся в твердом состоянии при комнатной температуре. И наоборот, триглицерид, который является жидким при комнатной температуре, называется «маслом» . Термин нейтральные жиры также используется как синоним триглицеридов. Нейтральные жиры, в частности, представляют собой жиры, которые описываются как нейтральные, потому что они не заряжены и не содержат кислотных или основных групп. Они неполярны и гидрофобны. Они часто встречаются в области бедер и туловища, где они обеспечивают изоляцию для сохранения тепла и запасов топлива в организме. Срок жир также часто ассоциируется с триглицеридами. Это потому, что триглицериды являются основными составляющими жировых отложений, а также растительных жиров.
Триглицериды принадлежат к «глицеридам» , группе сложных эфиров, образующихся из глицерина, реагирующего с жирными кислотами. Они классифицируются на основе количества жирных кислот, реагирующих с глицерином. Таким образом, триглицерид будет иметь три жирные кислоты, реагирующие с функциональной гидроксильной группой глицерина. Другими примерами глицеридов являются моноглицериды и диглицериды.
Они классифицируются на основе количества жирных кислот, реагирующих с глицерином. Таким образом, триглицерид будет иметь три жирные кислоты, реагирующие с функциональной гидроксильной группой глицерина. Другими примерами глицеридов являются моноглицериды и диглицериды.
Триглицериды можно рассматривать как подгруппу глицеролипидов, группу липидных молекул, каждая из которых имеет основную структуру, состоящую из глицеринового остова и жирной кислоты (кислот). Из-за этого триглицериды также могут называться триацилглицеринами. Другими подгруппами глицеролипидов являются моноглицерины и диглицерины, которые характеризуются количеством жирных кислот.
Происхождение слова: три – (три) + глицерид
Аббревиатура/Акроним:
- ТГ
- ТЭГ
Синоним(ы):
См. также:
- 9003 9 глицерид
- жирная кислота
- моноглицерид
- диглицерид
- глицеролипид
Связанный термин(ы):
Последнее обновление: 12 июля 2021 г.
Вам также понравится…
Генетика биосинтеза нейтральных липидов: эволюционная перспектива
1. Accad M, Smith SJ, Newland DL, Sanan DA, King LE Jr, Linton MF, Fazio S, Farese RV Jr Массивный ксантоматоз и измененный состав атеросклеротических поражений у мышей с гиперлипидемией, лишенных ацил-КоА:холестеролацилтрансферазы Штейнбухель А. Триацилглицерины в прокариотических микроорганизмах. Appl Microbiol Biotechnol 60: 367–376, 2002. [PubMed] [Google Scholar]
3. Ashrafi K, Chang FY, Watts JL, Fraser AG, Kamath RS, Ahringer J, Ruvkun G. Полногеномный анализ РНК-интерференции генов, регулирующих жир Caenorhabditis elegans. Nature 421: 268–272, 2003. [PubMed] [Google Scholar]
4. Афинштадт К., Даум Г. Жизненный цикл нейтральных липидов: синтез, хранение и деградация. Cell Mol Life Sci 63: 1355–1369, 2006. [PubMed] [Google Scholar]
5. Borradaile NM, Han X, Harp JD, Gale SE, Ory DS, Schaffer JE. Нарушение структуры и целостности эндоплазматического ретикулума при липотоксической гибели клеток. J Lipid Res 47: 2726–2737, 2006. [PubMed] [Google Scholar]
J Lipid Res 47: 2726–2737, 2006. [PubMed] [Google Scholar]
6. Брей Г.А., Тарталья Л.А. Лекарственные стратегии в лечении ожирения. Nature 404: 672–677, 2000. [PubMed] [Google Scholar]
7. Brouwers JF, Smeenk IM, van Golde LM, Tielens AG. Включение, модификация и оборот жирных кислот у взрослых особей Schistosoma mansoni. Mol Biochem Parasitol 88: 175–185, 1997. [PubMed] [Google Scholar]
8. Buhman KK, Accad M, Novak S, Choi RS, Wong JS, Hamilton RL, Turley S, Farese RV Jr. Устойчивость к диете индуцированная гиперхолестеринемия и образование камней в желчном пузыре у мышей с дефицитом ACAT2. Nat Med 6: 1341–1347, 2000. [PubMed] [Google Scholar]
9. Buhman KK, Chen HC, Farese RV Jr. Ферменты синтеза нейтральных липидов. J Biol Chem 276: 40369–40372, 2001. [PubMed] [Google Scholar]
10. Buszczak M, Lu X, Segraves WA, Chang TY, Cooley L. Мутации в промежуточном гене разрушают ацилкофермент A дрозофилы: диацилглицерин. ацилтрансфераза. Genetics 160: 1511–1518, 2002. [Бесплатная статья PMC] [PubMed] [Google Scholar]
[Бесплатная статья PMC] [PubMed] [Google Scholar]
11. Cao J, Burn P, Shi Y. Свойства мышиного кишечного ацил-КоА:моноацилглицеролацилтрансферазы, MGAT2. J Biol Chem 278: 25657–25663, 2003. [PubMed] [Google Scholar]
12. Cao J, Cheng L, Shi Y. Каталитические свойства MGAT3, предполагаемой триацилгицеролсинтазы. J Lipid Res 48: 583–591, 2007. [PubMed] [Google Scholar]
13. Cao J, Hawkins E, Brozinick J, Liu X, Zhang H, Burn P, Shi Y. Преобладающая роль MGAT2 в питании. абсорбция жира, связанная с распределением в тканях, субклеточной локализацией и активацией диеты с высоким содержанием жиров. J Biol Chem 279: 18878–18886, 2004. [PubMed] [Google Scholar]
14. Cao J, Lockwood J, Burn P, Shi Y. Клонирование и функциональная характеристика мышиного кишечного ацил-КоА:моноацилглицеролацилтрансферазы, MGAT2 . J Biol Chem 278: 13860–13866, 2003. [PubMed] [Google Scholar]
15. Cases S, Novak S, Zheng YW, Myers HM, Lear SR, Sande E, Welch CB, Lusis AJ, Spencer TA, Krause BR, Erickson SK, Farese RV Jr. ACAT-2, вторая ацил- КоА: холестеринацилтрансфераза. Его клонирование, экспрессия и характеристика. J Biol Chem 273: 26755–26764, 1998. [PubMed] [Google Scholar]
ACAT-2, вторая ацил- КоА: холестеринацилтрансфераза. Его клонирование, экспрессия и характеристика. J Biol Chem 273: 26755–26764, 1998. [PubMed] [Google Scholar]
16. Cases S, Smith SJ, Zheng YW, Myers HM, Lear SR, Sande E, Novak S, Collins C, Welch CB, Lusis AJ, Erickson SK, Farese RV Jr. Идентификация гена, кодирующего ацил-КоА: диацилглицерол-ацилтрансферазу, ключевой фермент в синтезе триацилглицерина. Proc Natl Acad Sci USA 95: 13018–13023, 1998. [Бесплатная статья PMC] [PubMed] [Google Scholar]
17. Cases S, Stone SJ, Zhou P, Yen E, Tow B, Lardizabal KD, Voelker T, Farese RV Jr. Клонирование DGAT2, второй диацилглицерол-ацилтрансферазы млекопитающих, и родственных членов семейства. J Biol Chem 276: 38870–38876, 2001. [PubMed] [Google Scholar]
18. Chang CC, Huh HY, Cadigan KM, Chang TY. Молекулярное клонирование и функциональная экспрессия кДНК ацил-коэнзима А:холестеролацилтрансферазы человека в мутантных клетках яичника китайского хомячка. J Biol Chem 268: 20747–20755, 1993.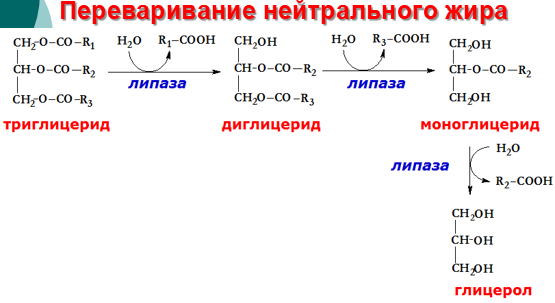 [PubMed] [Google Scholar]
[PubMed] [Google Scholar]
19. Chang CC, Lee CY, Chang ET, Cruz JC, Levesque MC, Chang TY. Рекомбинантная ацил-КоА:холестеролацилтрансфераза-1 (ACAT-1), очищенная до существенной гомогенности, использует холестерин в смешанных мицеллах или в везикулах высококооперативным образом. J Biol Chem 273: 35132–35141, 1998. [PubMed] [Google Scholar]
20. Chang CC, Sakashita N, Ornvold K, Lee O, Chang ET, Dong R, Lin S, Lee CY, Strom SC, Kashyap R, Fung JJ, Farese RV Jr, Patoiseau JF, Delhon A, Chang TY. Иммунологический количественный анализ и локализация ACAT-1 и ACAT-2 в печени и тонком кишечнике человека. J Biol Chem 275: 28083–28092, 2000. [PubMed] [Google Scholar]
21. Chen HC, Jensen DR, Myers HM, Eckel RH, Farese RV Jr. Устойчивость к ожирению и усиленный метаболизм глюкозы у мышей, которым трансплантировали белую жировую ткань, лишенную ацил-КоА: диацилглицерол-ацилтрансферазы. 1. J Clin Invest 111: 1715–1722, 2003. [Бесплатная статья PMC] [PubMed] [Google Scholar]
22. Chen HC, Stone SJ, Zhou P, Buhman KK, Farese RV Jr. Диссоциация ожирения и нарушений удаление глюкозы у мышей со сверхэкспрессией ацилкофермента а: диацилглицерол-ацилтрансферазы 1 в белой жировой ткани. Диабет 51: 3189–3195, 2002. [PubMed] [Google Scholar]
Chen HC, Stone SJ, Zhou P, Buhman KK, Farese RV Jr. Диссоциация ожирения и нарушений удаление глюкозы у мышей со сверхэкспрессией ацилкофермента а: диацилглицерол-ацилтрансферазы 1 в белой жировой ткани. Диабет 51: 3189–3195, 2002. [PubMed] [Google Scholar]
23. Chen N, Liu L, Zhang Y, Ginsberg HN, Yu YH. Инсулинорезистентность всего тела при отсутствии ожирения у мышей FVB с гиперэкспрессией Dgat1 в жировой ткани. Diabetes 54: 3379–3386, 2005. [PubMed] [Google Scholar]
24. Cheng D, Chang CC, Qu X, Chang TY. Активация ацилкоэнзима А:холестеролацилтрансферазы холестерином или оксистеролом в бесклеточной системе. J Biol Chem 270: 685–695, 1995. [PubMed] [Google Scholar]
25. Ченг Д., Лю Дж., Чанг CCY, Чанг TY. Семейства генов ACAT и DGAT2 млекопитающих. В: Метаболизм липидов и биогенез мембран, под редакцией Даума Г. Берлин: Springer-Verlag, 2004, с. 241–265.
26. Ченг Д., Нельсон Т.С., Чен Дж., Уокер С.Г., Уордвелл-Суонсон Дж., Мигалла Р., Тауб Р., Биллхаймер Дж. Т., Рамакер М., Федер Дж.Н. Идентификация ацил-кофермента А: моноацилглицерол-ацилтрансферазы 3, кишечного специфического фермента, участвующего в абсорбции пищевых жиров. J Biol Chem 278: 13611–13614, 2003. [PubMed] [Google Scholar]
Т., Рамакер М., Федер Дж.Н. Идентификация ацил-кофермента А: моноацилглицерол-ацилтрансферазы 3, кишечного специфического фермента, участвующего в абсорбции пищевых жиров. J Biol Chem 278: 13611–13614, 2003. [PubMed] [Google Scholar]
27. Ченг Дж. Б., Рассел Д. В. Биосинтез воска млекопитающих. II. Клонирование экспрессии кДНК восковой синтазы, кодирующей член семейства ферментов ацилтрансфераз. J Biol Chem 279: 37798–37807, 2004. [Бесплатная статья PMC] [PubMed] [Google Scholar]
29. Chung WK, Goldberg-Berman J, Power-Kehoe L, Leibel RL. Молекулярное картирование мутации Tubby (Tub) на мышиной хромосоме 7. Genomics 32: 210–217, 1996. [PubMed] [Google Scholar]
30. Chung WK, Power-Kehoe L, Chua M, Leibel RL. Картирование рецептора OB на 1p в области неконсервативного порядка генов от мыши и крысы до человека. Геном Рез. 6: 431–438, 1996. [PubMed] [Google Scholar]
31. Cunha DA, Hekerman P, Ladrière L, Bazarra-Castro A, Ortis F, Wakeham MC, Moore F, Rasschaert J, Cardozo AK, Bellomo E, Overbergh L, Mathieu C , Lupi R, Hai T, Herchuelz A, Marchetti P, Rutter GA, Eizirik DL, Cnop M. Инициация и выполнение липотоксического стресса ER в бета-клетках поджелудочной железы. J Cell Sci 121: 2308–2318, 2008. [Бесплатная статья PMC] [PubMed] [Google Scholar]
Инициация и выполнение липотоксического стресса ER в бета-клетках поджелудочной железы. J Cell Sci 121: 2308–2318, 2008. [Бесплатная статья PMC] [PubMed] [Google Scholar]
32. Dahlqvist A, Stahl U, Lenman M, Banas A, Lee M, Sandager L, Ronne H, Stymne S Фосфолипид:диацилглицерол-ацилтрансфераза: фермент, который катализирует независимое от ацил-КоА образование триацилглицерина в дрожжах и растениях. Proc Natl Acad Sci USA 97: 6487–6492, 2000. [Бесплатная статья PMC] [PubMed] [Google Scholar]
33. Даунинг Д.Т., Стюарт М.Е., Верц П.В., Колтон С.В., Абрахам В., Штраус Дж.С. Липиды кожи: обновление. J Invest Dermatol 88: 2s–6s, 1987. [PubMed] [Google Scholar]
34. Farese RV Jr, Cases S, Smith SJ. Синтез триглицеридов: выводы из клонирования диацилглицерол-ацилтрансферазы. Curr Opin Lipidol 11: 229–234, 2000. [PubMed] [Google Scholar]
35. Fazio S, Major AS, Swift LL, Gleaves LA, Accad M, Linton MF, Farese RV Jr. Повышенный атеросклероз рецепторов ЛПНП. нулевые мыши, лишенные ACAT1 в макрофагах. J Clin Invest 107: 163–171, 2001. [Бесплатная статья PMC] [PubMed] [Google Scholar]
J Clin Invest 107: 163–171, 2001. [Бесплатная статья PMC] [PubMed] [Google Scholar]
36. Friedman JM, Leibel RL, Bahary N. Молекулярное картирование генов ожирения. Mamm Genome 1: 130–144, 1991. [PubMed] [Google Scholar]
37. Friedman JM, Leibel RL, Bahary N, Siegel DA, Truett G. Генетический анализ сложных заболеваний. Молекулярное картирование генов ожирения у мышей и людей. Ann NY Acad Sci 630: 100–115, 1991. [PubMed] [Google Scholar]
38. Friedman JM, Leibel RL, Siegel DS, Walsh J, Bahary N. Молекулярное картирование obмутации мыши. Геномика 11: 1054–1062, 1991. [PubMed] [Google Scholar]
39. Гарбарино Дж., Стерли С.Л. Гомеостатические системы для стеролов и других липидов. Biochem Soc Trans 33: 1182–1185, 2005. [PubMed] [Google Scholar]
40. Garbarino JM, Sturley SL. Насыщенные жиром: новые взгляды на липотоксичность. Curr Opin Clin Nutr Metab Care. 12: 110–116, 2009. [PubMed] [Google Scholar]
41. Gotto AM Jr. Триглицериды как фактор риска ишемической болезни сердца.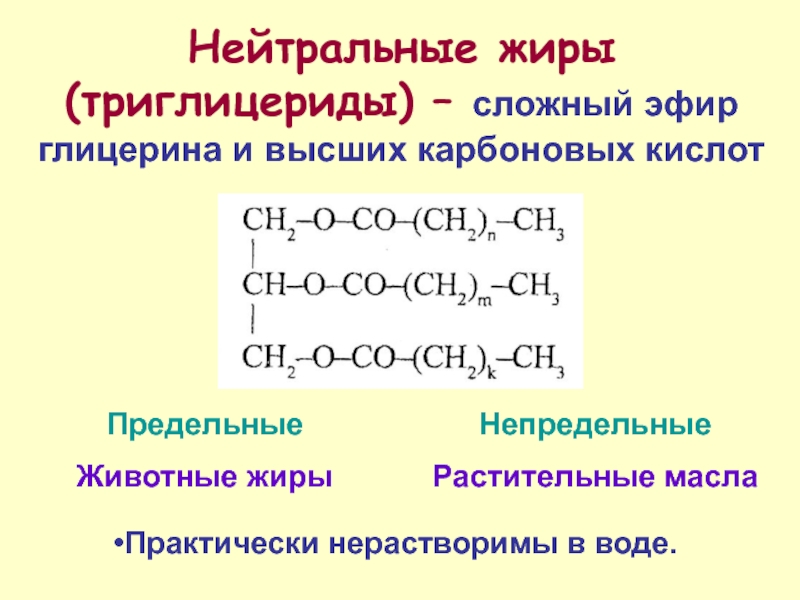 Am J Cardiol 82: 22Q–25Q, 1998. [PubMed] [Google Scholar]
Am J Cardiol 82: 22Q–25Q, 1998. [PubMed] [Google Scholar]
42. Хэдер Т., Мюллер С., Агилера М., Эйленберг К.Г., Штойернагель А., Чиоссек Т., Кюнляйн Р.П., Лемер Л., Фрич Р., Дорманн С., Феттер И.Р., Джекле Х., Доан В.В., Бреннер Г. Контроль хранения триглицеридов белком с доменом WD40/TPR. EMBO Rep 4: 511–516, 2003. [Бесплатная статья PMC] [PubMed] [Google Scholar]
43. Hirsch J, Leibel RL. Генетика ожирения. Hosp Pract (Minneap) 33: 55–59, 62–;–55, 69–70 passim, 1998. [PubMed] [Google Scholar]
44. Holland WL, Brozinick JT, Wang LP, Hawkins ED, Sargent KM, Лю Ю., Нарра К., Хён К.Л., Ноттс Т.А., Сиски А., Нельсон Д.Х., Каратанасис С.К., Фонтенот Г.К., Бирнбаум М.Дж., Саммерс С.А. Ингибирование синтеза церамидов улучшает инсулинорезистентность, вызванную глюкокортикоидами, насыщенными жирами и ожирением. Cell Metab 5: 167–179, 2007. [PubMed] [Google Scholar]
45. Hori M, Satoh M, Furukawa K, Sakamoto Y, Hakamata H, Komohara Y, Takeya M, Sasaki Y, Miyazaki A, Horiuchi S. Ацил-коэнзим A: холестерин ацилтрансфераза-2 (ACAT-2) отвечает за повышенную активность ACAT в кишечнике у крыс с диабетом. Arterioscler Thromb Vasc Biol 24: 1689–1695, 2004. [PubMed] [Google Scholar]
Ацил-коэнзим A: холестерин ацилтрансфераза-2 (ACAT-2) отвечает за повышенную активность ACAT в кишечнике у крыс с диабетом. Arterioscler Thromb Vasc Biol 24: 1689–1695, 2004. [PubMed] [Google Scholar]
46. Ishige T, Tani A, Sakai Y, Kato N. Производство восковых эфиров бактериями. Curr Opin Microbiol 6: 244–250, 2003. [PubMed] [Google Scholar]
47. Jeffcoat R. Ожирение — точка зрения, основанная на биохимической взаимосвязи липидов и углеводов. Med Hypotheses 68: 1159–1171, 2007. [PubMed] [Google Scholar]
48. Kalscheuer R, Luftmann H, Steinbüchel A. Синтез новых липидов в Saccharomyces cerevisiae путем гетерологичной экспрессии неспецифической бактериальной ацилтрансферазы. Appl Environ Microbiol 70: 7119–7125, 2004. [Статья бесплатно PMC] [PubMed] [Google Scholar]
биосинтез триацилглицерина в Acinetobacter calcoaceticus ADP1. J Biol Chem 278: 8075–8082, 2003. [PubMed] [Google Scholar]
50. Kalscheuer R, Stöveken T, Luftmann H, Malkus U, Reichelt R, Steinbüchel A. Биосинтез нейтральных липидов в искусственных кишечных палочках: маслоподобные восковые эфиры жожоба и бутиловые эфиры жирных кислот. Appl Environ Microbiol 72: 1373–1379, 2006. [Статья PMC бесплатно] [PubMed] [Google Scholar]
Биосинтез нейтральных липидов в искусственных кишечных палочках: маслоподобные восковые эфиры жожоба и бутиловые эфиры жирных кислот. Appl Environ Microbiol 72: 1373–1379, 2006. [Статья PMC бесплатно] [PubMed] [Google Scholar]
51. Kalscheuer R, Uthoff S, Luftmann H, Steinbüchel A. Биосинтез восковых диэфиров неспецифическая бифункциональная синтаза эфира воска / ацил-КоА: диацилглицеролацилтрансфераза из Acinetobacter calcoaceticus ADP1. Eur J Lipid Sci Tech 105: 578–584, 2003. [Google Scholar]
52. Кинг А., Нам Дж.В., Хан Дж., Хиллиард Дж., Яворски Дж.Г. Биосинтез кутикулярного воска в лепестках петунии: клонирование и характеристика алкоголь-ацилтрансферазы, которая синтезирует эфиры воска. Planta 226: 381–394, 2007. [PubMed] [Google Scholar]
53. Krauss RM Триглицериды и атерогенные липопротеины: обоснование для управления липидами. Am J Med 105: 58S–62S, 1998. [PubMed] [Google Scholar]
54. Lardizabal KD, Metz JG, Sakamoto T, Hutton WC, Pollard MR, Lassner MW. Очистка синтазы воска эмбриона жожоба, клонирование его кДНК и производство высоких уровней воска в семенах трансгенного арабидопсиса. Plant Physiol 122: 645–655, 2000. [Бесплатная статья PMC] [PubMed] [Google Scholar]
Очистка синтазы воска эмбриона жожоба, клонирование его кДНК и производство высоких уровней воска в семенах трансгенного арабидопсиса. Plant Physiol 122: 645–655, 2000. [Бесплатная статья PMC] [PubMed] [Google Scholar]
55. Ли А.Х., Скапа Э.Ф., Коэн Д.Е., Глимчер Л.Х. Регуляция печеночного липогенеза фактором транскрипции XBP1. Science 320: 1492–1496, 2008. [Бесплатная статья PMC] [PubMed] [Google Scholar]
56. Лейбель Р.Л. Ожирение: игра в дюймы. Pediatrics 95: 131–132, 1995. [PubMed] [Google Scholar]
57. Лейбель Р.Л. Ожирение с одним геном у грызунов: возможная связь с человеческим ожирением. J Nutr 127: 1908S, 1997. [PubMed] [Google Scholar]
58. Leibel RL, Chung WK, Chua SC Jr. Молекулярная генетика ожирения грызунов с одним геном. Дж. Биол. Хим. 272: 31937–31940, 1997. [PubMed] [Google Scholar]
59. Liang JJ, Oelkers P, Guo C, Chu PC, Dixon JL, Ginsberg HN, Sturley SL. Сверхэкспрессия диацилглицеролацилтрансферазы 1 человека, ацил-КоА:холестеролацилтрансферазы 1 или ацил-КоА:холестеролацилтрансферазы 2 стимулирует секрецию липопротеинов, содержащих аполипопротеин В, в клетках McA-RH7777. J Biol Chem 279: 44938–44944, 2004. [PubMed] [Google Scholar]
J Biol Chem 279: 44938–44944, 2004. [PubMed] [Google Scholar]
61. Liang K, Vaziri ND. Активация ацил-КоА:холестеролацилтрансферазы при хронической почечной недостаточности. Am J Physiol Endocrinol Metab 283: E676–E681, 2002. [PubMed] [Google Scholar]
62. Listenberger LL, Han X, Lewis SE, Cases S, Farese RV Jr, Ory DS, Schaffer JE. Накопление триглицеридов защищает от липотоксичности, вызванной жирными кислотами. Proc Natl Acad Sci USA 100: 3077–3082, 2003. [Бесплатная статья PMC] [PubMed] [Google Scholar]
63. Listenberger LL, Ory DS, Schaffer JE. Индуцированный пальмитатом апоптоз может происходить независимым от церамидов путем. J Biol Chem 276: 14890–14895, 2001. [PubMed] [Google Scholar]
64. Listenberger LL, Schaffer JE. Механизмы липоапоптоза: значение для сердечно-сосудистых заболеваний человека. Trends Cardiovasc Med 12: 134–138, 2002. [PubMed] [Google Scholar]
65. Лю Ю., Миллар Дж. С., Кромли Д. А., Грэм М., Крук Р., Биллхеймер Дж. Т. , Рейдер Д. Д. Нокдаун ацил-КоА: диацилглицеролацилтрансферазы 2 с помощью антисмыслового олигонуклеотида снижает секрецию ТГ ЛПОНП и апоВ у мышей. Biochim Biophys Acta 1781: 97–104, 2008. [PubMed] [Google Scholar]
, Рейдер Д. Д. Нокдаун ацил-КоА: диацилглицеролацилтрансферазы 2 с помощью антисмыслового олигонуклеотида снижает секрецию ТГ ЛПОНП и апоВ у мышей. Biochim Biophys Acta 1781: 97–104, 2008. [PubMed] [Google Scholar]
66. Локвуд Дж. Ф., Цао Дж., Берн П., Ши Ю. Моноацилглицерол-ацилтрансфераза кишечника человека: дифференциальные особенности тканевой экспрессии и активности. Am J Physiol Endocrinol Metab 285: E927–E937, 2003. [PubMed] [Google Scholar]
67. Man WC, Miyazaki M, Chu K, Ntambi J. Колокализация SCD1 и DGAT2: подразумевает предпочтение эндогенных мононенасыщенных жирных кислот в синтезе триглицеридов. J Lipid Res 47: 1928–1939, 2006. [PubMed] [Google Scholar]
68. McCulley JP, Shine WE. Липидный слой слез: зависит от функции мейбомиевых желез. Exp Eye Res 78: 361–365, 2004. [PubMed] [Google Scholar]
69. McGarry JD Banting, лекция 2001: нарушение регуляции метаболизма жирных кислот в этиологии диабета 2 типа. Диабет 51: 7–18, 2002. [PubMed] [Google Scholar]
70. Meegalla RL, Billheimer JT, Cheng D. Согласованное повышение активности ацил-кофермента A: диацилглицерол-ацилтрансферазы (DGAT) посредством независимой стимуляции экспрессии мРНК DGAT1 и DGAT2 углеводами и инсулином. Biochem Biophys Res Commun 298: 317–323, 2002. [PubMed] [Google Scholar]
Meegalla RL, Billheimer JT, Cheng D. Согласованное повышение активности ацил-кофермента A: диацилглицерол-ацилтрансферазы (DGAT) посредством независимой стимуляции экспрессии мРНК DGAT1 и DGAT2 углеводами и инсулином. Biochem Biophys Res Commun 298: 317–323, 2002. [PubMed] [Google Scholar]
71. Millar JS, Stone SJ, Tietge UJ, Tow B, Billheimer JT, Wong JS, Hamilton RL, Farese RV Jr, Rader DJ . Кратковременная сверхэкспрессия DGAT1 или DGAT2 увеличивает продукцию триглицеридов в печени, но не триглицеридов ЛПОНП или апоВ. J липидный рез 47: 2297–2305, 2006. [PubMed] [Google Scholar]
72. Monetti M, Levin MC, Watt MJ, Sajan MP, Marmor S, Hubbard BK, Stevens RD, Bain JR, Newgard CB, Farese RV Sr, Hevener AL , Farese RV Jr. Диссоциация стеатоза печени и резистентности к инсулину у мышей со сверхэкспрессией DGAT в печени. Cell Metab 6: 69–78, 2007. [PubMed] [Google Scholar]
73. Mullner H, Daum G. Динамика накопления нейтральных липидов в дрожжах. Acta Biochim Pol 51: 323–347, 2004. [PubMed] [Google Scholar]
[PubMed] [Google Scholar]
74. Nicolaides N, Kaitaranta JK, Rawdah TN, Macy JI, Boswell FM 3rd, Smith RE. Исследования мейбомиевых желез: сравнение липидов бычка и человека. Invest Ophthalmol Vis Sci 20: 522–536, 1981. [PubMed] [Google Scholar]
75. O’Byrne SM, Wongsiriroj N, Libien J, Vogel S, Goldberg IJ, Baehr W, Palczewski K, Blaner WS. Абсорбция и накопление ретиноидов нарушены у мышей, у которых отсутствует лецитин: ретинолацилтрансфераза (LRAT). J Biol Chem 280: 35647–35657, 2005. [Бесплатная статья PMC] [PubMed] [Google Scholar]
76. Oelkers P, Behari A, Cromley D, Billheimer JT, Sturley SL. Характеристика двух генов человека, кодирующих ацилкофермент А: ферменты, родственные холестеринацилтрансферазе. J Biol Chem 273: 26765–26771, 1998. [PubMed] [Google Scholar]
77. Oelkers P, Cromley D, Padamsee M, Billheimer JT, Sturley SL. Ген DGA1 определяет второй путь синтеза триглицеридов у дрожжей. J Biol Chem 277: 8877–8881, 2002. [PubMed] [Google Scholar]
78. Oelkers P, Tinkelenberg A, Erdeniz N, Cromley D, Billheimer JT, Sturley SL. Ген, подобный лецитин-холестерол-ацилтрансферазе, опосредует этерификацию диацилглицерина у дрожжей. J Biol Chem 275: 15609–15612, 2000. [PubMed] [Google Scholar]
Oelkers P, Tinkelenberg A, Erdeniz N, Cromley D, Billheimer JT, Sturley SL. Ген, подобный лецитин-холестерол-ацилтрансферазе, опосредует этерификацию диацилглицерина у дрожжей. J Biol Chem 275: 15609–15612, 2000. [PubMed] [Google Scholar]
79. Олкерс П.М., Стерли С.Л. Механизмы и медиаторы биосинтеза нейтральных липидов в эукариотических клетках. В: Метаболизм липидов и биогенез мембран, под редакцией Даума Г. Берлин: Springer-Verlag, 2004, с. 281–311.
80. Orland MD, Anwar K, Cromley D, Chu CH, Chen L, Billheimer JT, Hussain MM, Cheng D. Зависимая этерификация ретинола от ацилкофермента А ацилкоэнзимом А: диацилглицеролацилтрансфераза 1. Biochim Biophys Acta 1737: 76– 82, 2005. [PubMed] [Google Scholar]
81. Ota T, Gayet C, Ginsberg HN. Ингибирование секреции аполипопротеина B100 липид-индуцированным стрессом эндоплазматического ретикулума печени у грызунов. J Clin Invest 118: 316–332, 2008. [Бесплатная статья PMC] [PubMed] [Google Scholar]
82. Папе М. Е., Шульц П.А., Ри Т.Дж., Дематтос Р.Б., Кифт К., Бисгайер С.Л., Ньютон Р.С., Краузе Б.Р. Тканеспецифические изменения ацил-КоА: уровни мРНК холестеринацилтрансферазы (АСАТ) у кроликов. J Lipid Res 36: 823–838, 1995. [PubMed] [Google Scholar]
Е., Шульц П.А., Ри Т.Дж., Дематтос Р.Б., Кифт К., Бисгайер С.Л., Ньютон Р.С., Краузе Б.Р. Тканеспецифические изменения ацил-КоА: уровни мРНК холестеринацилтрансферазы (АСАТ) у кроликов. J Lipid Res 36: 823–838, 1995. [PubMed] [Google Scholar]
83. Payne VA, Au WS, Gray SL, Nora ED, Rahman SM, Sanders R, Hadaschik D, Friedman JE, O’Rahilly S , Рочфорд Дж. Последовательная регуляция экспрессии диацилглицеролацилтрансферазы 2 с помощью СААТ/энхансер-связывающего белка бета (C/EBPbeta) и C/EBPalpha во время адипогенеза. J Biol Chem 282: 21005–21014, 2007. [Бесплатная статья PMC] [PubMed] [Google Scholar]
84. Ранганатан Г., Унал Р., Покровская И., Яо-Боренгассер А., Фанаван Б., Лека-Черник Б., Расули Н., Керн П.А. Липогенные ферменты DGAT1, синтетаза жирных кислот и липопротеинлипаза в жировой ткани: последствия ожирения, резистентность к инсулину и лечение тиазолидиндионами. J Lipid Res 47: 2444–2450, 2006. [Бесплатная статья PMC] [PubMed] [Google Scholar]
85. Reneerkens J, Piersma T, Damsté JS. Выражение годовых циклов в восковом составе красных сучков: ограничения на изменение фенотипа. J Exp Zool Часть A Ecol Genet Physiol 307: 127–139, 2007. [PubMed] [Google Scholar]
Выражение годовых циклов в восковом составе красных сучков: ограничения на изменение фенотипа. J Exp Zool Часть A Ecol Genet Physiol 307: 127–139, 2007. [PubMed] [Google Scholar]
86. Reneerkens J, Piersma T, Damste JS. Переход на диэфирные воски может уменьшить хищничество птичьих гнезд хищниками млекопитающими, использующими обонятельные сигналы. J Exp Biol 208: 4199–4202, 2005. [PubMed] [Google Scholar]
87. Reneerkens J, Piersma T, Sinninghe Damsté JS. Кулики (Scolopacidae) переключаются с моноэфирных восков на диэфирные во время ухаживания и инкубации, но почему? Proc Biol Sci 269: 2135–2139, 2002. [Бесплатная статья PMC] [PubMed] [Google Scholar]
88. Роншауген М., МакГиннис Н., Инглис Д., Чоу Д., Чжао Дж., МакГиннис В. Структура и характер экспрессии TULP и TUSP дрозофилы, членов семейства тубби-подобных генов. Mech Dev 117: 209–215, 2002. [PubMed] [Google Scholar]
89. Rosenbaum M, Leibel RL. Роль лептина в физиологии человека. N Engl J Med 341: 913–915, 1999. [PubMed] [Google Scholar]
[PubMed] [Google Scholar]
90. Ross R Патогенез атеросклероза: взгляд на 1990-е годы. Nature 362: 801–809, 1993. [PubMed] [Google Scholar]
91. Schaffer JE Липотоксичность: при переедании тканей. Curr Opin Lipidol 14: 281-287, 2003. [PubMed] [Google Scholar]
апоптоз нейронов и эндотелиальных клеток. Apoptosis 11: 1111–1119, 2006. [PubMed] [Google Scholar]
93. Seo T, Oelkers PM, Giattina MR, Worgall TS, Sturley SL, Deckelbaum RJ. Дифференциальная модуляция транскрипции и активности ACAT1 и ACAT2 длинноцепочечными свободными жирными кислотами в культивируемых клетках. Биохимия 40: 4756–4762, 2001. [PubMed] [Google Scholar]
94. Симха В., Гарг А. Липодистрофия: уроки липидного и энергетического обмена. Curr Opin Lipidol 17: 162–169, 2006. [PubMed] [Google Scholar]
95. Smith SJ, Cases S, Jensen DR, Chen HC, Sande E, Tow B, Sanan DA, Raber J, Eckel RH, Farese RV Jr. Устойчивость к ожирению и множественные механизмы синтеза триглицеридов у мышей, лишенных Dgat. Nat Genet 25: 87–90, 2000. [PubMed] [Google Scholar]
Nat Genet 25: 87–90, 2000. [PubMed] [Google Scholar]
96. Song BL, Qi W, Yang XY, Chang CC, Zhu JQ, Chang TY, Li BL. Организация гена ACAT-2 человека и его промоторная активность, специфичная для клеточного типа. Biochem Biophys Res Commun 282: 580–588, 2001. [PubMed] [Google Scholar]
97. Spady DK, Willard MN, Meidell RS. Роль ацилкофермента А: холестеринацилтрансферазы-1 в контроле секреции липопротеинов очень низкой плотности в печени и экспрессии рецепторов липопротеинов низкой плотности у мышей и хомяков. J Biol Chem 275: 27005–27012, 2000. [PubMed] [Google Scholar]
98. Stewart ME Липиды сальных желез. Semin Dermatol 11: 100–105, 1992. [PubMed] [Google Scholar]
99. Stone SJ, Myers HM, Watkins SM, Brown BE, Feingold KR, Elias PM, Farese RV Jr. Липопения и нарушения кожного барьера в DGAT2 -дефицитные мыши. Дж Биол Хим 279: 11767–11776, 2004. [PubMed] [Google Scholar]
100. Stöveken T, Kalscheuer R, Malkus U, Reichelt R, Steinbüchel A. Синтаза сложного эфира воска / ацилкоэнзим A: диацилглицеролацилтрансфераза из Acinetobacter sp. штамм ADP1: характеристика нового типа ацилтрансферазы. J Bacteriol 187: 1369–1376, 2005. [Бесплатная статья PMC] [PubMed] [Google Scholar]
штамм ADP1: характеристика нового типа ацилтрансферазы. J Bacteriol 187: 1369–1376, 2005. [Бесплатная статья PMC] [PubMed] [Google Scholar]
101. Taskinen MR Триглицерид является основным атерогенным липидом при NIDDM. Diabetes Metab Rev 13: 93–98, 1997. [PubMed] [Google Scholar]
102. Tsai J, Qiu W, Kohen-Avramoglu R, Adeli K. Ингибирование MEK-ERK исправляет дефект сборки ЛПОНП в клетках HepG2: потенциальная роль ERK в сборке частиц VLDL-ApoB100. Arterioscler Thromb Vasc Biol 27: 211–218, 2007. [PubMed] [Google Scholar]
103. Turkish A, Sturley SL. Регуляция метаболизма триглицеридов. I. Эукариотический синтез нейтральных липидов: «Многие способы снять кожу с ACAT или DGAT». Am J Physiol Gastrointest Liver Physiol 292: G953–G957, 2007. [PubMed] [Google Scholar]
104. Турецкий А.Р., Хеннеберри А.Л., Кромли Д., Падамси М., Олкерс П., Бацци Х., Кристиано А.М., Биллхеймер Дж.Т., Стерли С.Л. Идентификация двух новых ацил-КоА восковых спиртацилтрансфераз человека: членов надсемейства генов диацилглицерол-ацилтрансферазы 2 (DGAT2). J Biol Chem 280: 14755–14764, 2005. [PubMed] [Google Scholar]
J Biol Chem 280: 14755–14764, 2005. [PubMed] [Google Scholar]
105. Uelman PJ, Oka K, Sullivan M, Chang CC, Chang TY, Chan L. Тканеспецифическая экспрессия и регуляция холестерина ацилкофермента A :холестеролацилтрансфераза (АСАТ) у мышей. Молекулярное клонирование кДНК АСАТ мыши, хромосомная локализация и регуляция АСАТ in vivo и in vitro. J Биол Хим 270: 26192–26201, 1995. [PubMed] [Google Scholar]
106. Unger RH, Orci L. Липоапоптоз: его механизм и его заболевания. Biochim Biophys Acta 1585: 202–212, 2002. [PubMed] [Google Scholar]
107. Вазири Н.Д., Лян К. Активация ацил-кофермента А: холестеринацилтрансферазы (АСАТ) при нефротическом синдроме. Kidney Int 61: 1769–1775, 2002. [PubMed] [Google Scholar]
108. Wältermann M, Stöveken T, Steinbüchel A. Ключевые ферменты для биосинтеза нейтральных запасных соединений липидов у прокариот: свойства, функции и возникновение воскового эфира синтазы/ацил-КоА: диацилглицеролацилтрансферазы. Биохимия 89: 230–242, 2007. [PubMed] [Google Scholar]
[PubMed] [Google Scholar]
109. Willner EL, Tow B, Buhman KK, Wilson M, Sanan DA, Rudel LL, Farese RV Jr. Дефицит ацил-КоА: холестеринацилтрансферазы 2 предотвращает атеросклероз у мышей с дефицитом аполипопротеина Е. Proc Natl Acad Sci USA 100: 1262–1267, 2003. [Бесплатная статья PMC] [PubMed] [Google Scholar]
110. Wisotzkey RG, Johnson AN, Takaesu NT, Newfeld SJ. Альфа/бета-гидролаза 2, предикатный ген, смежный с mad у Drosophila melanogaster, принадлежит к новому глобальному мультигенному семейству и ассоциирован с ожирением. J Mol Evol 56: 351–361, 2003. [PubMed] [Google Scholar]
111. Wongsiriroj N, Piantedosi R, Palczewski K, Goldberg IJ, Johnston TP, Li E, Blaner WS. Молекулярная основа поглощения ретиноидов: генетическое вскрытие. J Biol Chem 283: 13510–13519, 2008. [Бесплатная статья PMC] [PubMed] [Google Scholar]
112. Yagyu H, Kitamine T, Osuga J, Tozawa R, Chen Z, Kaji Y, Oka T, Perrey S , Tamura Y, Ohashi K, Okazaki H, Yahagi N, Shionoiri F, Iizuka Y, Harada K, Shimano H, Yamashita H, Gotoda T, Yamada N, Ishibashi S. Отсутствие ACAT-1 ослабляет атеросклероз, но вызывает сухость глаз и кожные заболевания. ксантоматоз у мышей с врожденной гиперлипидемией. J Biol Chem 275: 21324–21330, 2000. [PubMed] [Google Scholar]
Отсутствие ACAT-1 ослабляет атеросклероз, но вызывает сухость глаз и кожные заболевания. ксантоматоз у мышей с врожденной гиперлипидемией. J Biol Chem 275: 21324–21330, 2000. [PubMed] [Google Scholar]
113. Ямагути К., Ян Л., МакКолл С., Хуан Дж., Ю. ХХ., Пандей С.К., Бханот С., Мониа Б.П., Ли YX, Диль А.М. Ингибирование синтеза триглицеридов улучшает стеатоз печени, но усугубляет повреждение и фиброз печени у мышей с ожирением и неалкогольным стеатогепатитом. Hepatology 45: 1366–1374, 2007. [PubMed] [Google Scholar]
114. Yamazaki T, Sasaki E, Kakinuma C, Yano T, Miura S, Ezaki O. Повышенная секреция липопротеинов очень низкой плотности и масса гонадного жира у мышей избыточная экспрессия печеночного DGAT1. J Biol Chem 280: 21506–21514, 2005. [PubMed] [Google Scholar]
115. Yang H, Bard M, Bruner DA, Gleeson A, Deckelbaum RJ, Aljinovic G, Pohl TM, Rothstein R, Sturley SL. Этерификация стеролов в дрожжах: двухгенный процесс. Science 272: 1353–1356, 1996. [PubMed] [Google Scholar]
116. Yang H, Cromley D, Wang H, Billheimer JT, Sturley SL. Функциональная экспрессия кДНК ацил-кофермента А человека: холестеринацилтрансферазы в дрожжах. Видозависимая субстратная специфичность и чувствительность к ингибиторам. J Biol Chem 272: 3980–3985, 1997. [PubMed] [Google Scholar]
Yang H, Cromley D, Wang H, Billheimer JT, Sturley SL. Функциональная экспрессия кДНК ацил-кофермента А человека: холестеринацилтрансферазы в дрожжах. Видозависимая субстратная специфичность и чувствительность к ингибиторам. J Biol Chem 272: 3980–3985, 1997. [PubMed] [Google Scholar]
117. Yen CL, Brown CH 4th, Monetti M, Farese RV Jr. Многофункциональная O-ацилтрансфераза кожи человека, которая катализирует синтез ацилглицеролов, воска и ретиниловых эфиров. J Lipid Res 46: 2388–2397, 2005. [Бесплатная статья PMC] [PubMed] [Google Scholar]
118. Yen CL, Farese RV Jr. MGAT2, моноацилглицерол-ацилтрансфераза, экспрессируемая в тонком кишечнике. J Biol Chem 278: 18532–18537, 2003. [PubMed] [Google Scholar]
119. Yen CL, Monetti M, Burri BJ, Farese RV Jr. Фермент синтеза триацилглицерина DGAT1 также катализирует синтез диацилглицеролов, восков и ретиниловые эфиры. J Lipid Res 46: 1502–1511, 2005. [PubMed] [Google Scholar]
120. Yen CL, Stone SJ, Cases S, Zhou P, Farese RV Jr.

