Аминокислоты с разветвленной цепью – питание и черепно-мозговая травма
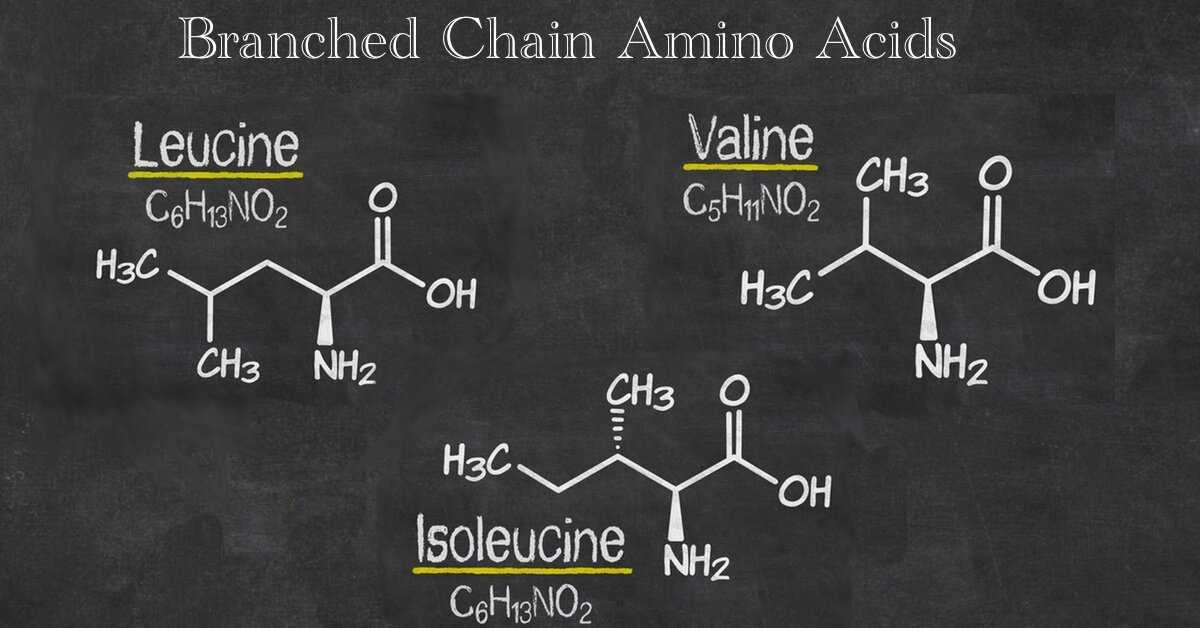
Аминокислоты с разветвленной цепью (BCAA) (лейцин, изолейцин и валин) необходимы для питания, поскольку они не могут синтезироваться эндогенно в организме человека и должны поступать с пищей. Они отличаются от других незаменимых аминокислот тем, что в печени отсутствуют ферменты, необходимые для их катаболизма.
В дополнение к их функции в качестве структурных компонентов белков, BCAA, по-видимому, также осуществляют регуляторный контроль белкового метаболизма. В тканях грызунов in vitro повышенные концентрации BCAA стимулируют синтез белка и подавляют катаболизм белка, тогда как другие смеси аминокислот, не содержащие BCAA, не оказывают такого влияния. У людей BCAA ингибируют катаболизм белков, но мало влияют на их синтез (см. обзор Matthews, 2005).
АМИНОКИСЛОТЫ С РАЗВЕТВЛЕННЫМИ ЦЕПЯМИ И МОЗГ
В головном мозге BCAA оказывают два важных влияния на выработку нейротрансмиттеров. Как доноры азота они способствуют синтезу возбуждающей глутаматной и тормозной гамма-аминомасляной кислоты (ГАМК) (Yudkoff et al., 2005). Они также конкурируют за транспорт через гематоэнцефалический барьер (ГЭБ) с триптофаном (предшественником серотонина), а также с тирозином и фенилаланином (предшественниками катехоламинов) (Fernstrom, 2005). Таким образом, прием BCAA вызывает быстрое повышение концентрации BCAA в плазме и увеличивает поглощение BCAA мозгом, но снижает поглощение триптофана, тирозина и фенилаланина. Снижение этих ароматических аминокислот напрямую влияет на синтез и высвобождение серотонина и катехоламинов. Читатель отсылается к Fernstrom (2005) для обзора биохимии транспорта BCAA в мозг. Пероральные ВСАА были исследованы в качестве средства для лечения неврологических заболеваний, таких как мания, нарушение двигательных функций, боковой амиотрофический склероз и дегенерация спинно-мозговых нервов. Эксайтотоксичность в результате чрезмерной стимуляции нейротрансмиттерами, такими как глутамат, приводит к повреждению клеток после черепно-мозговой травмы (ЧМТ).
Как доноры азота они способствуют синтезу возбуждающей глутаматной и тормозной гамма-аминомасляной кислоты (ГАМК) (Yudkoff et al., 2005). Они также конкурируют за транспорт через гематоэнцефалический барьер (ГЭБ) с триптофаном (предшественником серотонина), а также с тирозином и фенилаланином (предшественниками катехоламинов) (Fernstrom, 2005). Таким образом, прием BCAA вызывает быстрое повышение концентрации BCAA в плазме и увеличивает поглощение BCAA мозгом, но снижает поглощение триптофана, тирозина и фенилаланина. Снижение этих ароматических аминокислот напрямую влияет на синтез и высвобождение серотонина и катехоламинов. Читатель отсылается к Fernstrom (2005) для обзора биохимии транспорта BCAA в мозг. Пероральные ВСАА были исследованы в качестве средства для лечения неврологических заболеваний, таких как мания, нарушение двигательных функций, боковой амиотрофический склероз и дегенерация спинно-мозговых нервов. Эксайтотоксичность в результате чрезмерной стимуляции нейротрансмиттерами, такими как глутамат, приводит к повреждению клеток после черепно-мозговой травмы (ЧМТ). Однако, поскольку BCAA также способствуют синтезу тормозных нейротрансмиттеров, неясно, в какой степени роль BCAA в синтезе как возбуждающих, так и тормозных нейротрансмиттеров может способствовать их потенциальному влиянию на исходы ЧМТ.
Однако, поскольку BCAA также способствуют синтезу тормозных нейротрансмиттеров, неясно, в какой степени роль BCAA в синтезе как возбуждающих, так и тормозных нейротрансмиттеров может способствовать их потенциальному влиянию на исходы ЧМТ.
Перечень исследований на людях (с 1990 г. и позже), в которых оценивалась эффективность BCAA в обеспечении устойчивости или лечении ЧМТ или сопутствующих заболеваний или состояний (например, субарахноидальное кровоизлияние, внутричерепная аневризма, инсульт, аноксическая или гипоксическая ишемия, эпилепсия) при остром фаза представлена в ; это также включает подтверждающие данные, полученные на животных моделях ЧМТ. Возникновение или отсутствие побочных эффектов у людей включается, если сообщается авторами.
ТАБЛИЦА 8-1
Идентифицированы релевантные данные для BCAA.
ПРИМЕНЕНИЕ И БЕЗОПАСНОСТЬ
Расчетная средняя потребность (EAR) в лейцине, изолейцине и валине составляет 34, 15 и 19 мг/кг/день соответственно (IOM, 2005). Используя рекомендуемое потребление для человека весом 70 кг в качестве эталона, фактическое среднесуточное потребление в Соединенных Штатах для каждого из BCAA примерно в три раза выше для мужчин и примерно в два раза выше для женщин (IOM, 2005). Обогащенные BCAA белки или смеси аминокислот или только BCAA использовались при различных метаболических нарушениях, таких как хронические заболевания печени, энцефалопатия, сепсис и другие, обычно в попытке уменьшить поглощение ароматических аминокислот мозгом и для повышения низких уровней циркулирующих. Добавки BCAA продаются здоровым людям с заявлениями о том, что они увеличивают мышечную массу, уменьшают болезненность после тренировки и уменьшают утомляемость центральной нервной системы, хотя данные рецензируемых исследований редко подтверждают эти утверждения (Wagenmakers, 19).99). Предыдущий комитет Института медицины (IOM) рассмотрел вопрос о добавлении большего количества определенных аминокислот, включая BCAA, в рационы, используемые во время краткосрочных и высокоинтенсивных боевых действий.
Используя рекомендуемое потребление для человека весом 70 кг в качестве эталона, фактическое среднесуточное потребление в Соединенных Штатах для каждого из BCAA примерно в три раза выше для мужчин и примерно в два раза выше для женщин (IOM, 2005). Обогащенные BCAA белки или смеси аминокислот или только BCAA использовались при различных метаболических нарушениях, таких как хронические заболевания печени, энцефалопатия, сепсис и другие, обычно в попытке уменьшить поглощение ароматических аминокислот мозгом и для повышения низких уровней циркулирующих. Добавки BCAA продаются здоровым людям с заявлениями о том, что они увеличивают мышечную массу, уменьшают болезненность после тренировки и уменьшают утомляемость центральной нервной системы, хотя данные рецензируемых исследований редко подтверждают эти утверждения (Wagenmakers, 19).99). Предыдущий комитет Института медицины (IOM) рассмотрел вопрос о добавлении большего количества определенных аминокислот, включая BCAA, в рационы, используемые во время краткосрочных и высокоинтенсивных боевых действий. Этот комитет не нашел оснований рекомендовать добавление определенных аминокислот в эти рационы (IOM, 2006). В результате заявлений о пользе для фитнеса спортсмены и военнослужащие, стремящиеся повысить физическую работоспособность, могут потреблять BCAA даже выше, чем у обычных людей. Опрос Lieberman et al. (2010) обнаружили, что 23 процента военнослужащих, участвовавших в боевых действиях, и 47 процентов военнослужащих сил специального назначения принимали белковые или аминокислотные добавки.
Этот комитет не нашел оснований рекомендовать добавление определенных аминокислот в эти рационы (IOM, 2006). В результате заявлений о пользе для фитнеса спортсмены и военнослужащие, стремящиеся повысить физическую работоспособность, могут потреблять BCAA даже выше, чем у обычных людей. Опрос Lieberman et al. (2010) обнаружили, что 23 процента военнослужащих, участвовавших в боевых действиях, и 47 процентов военнослужащих сил специального назначения принимали белковые или аминокислотные добавки.
В отчете IOM за 2005 г. не было обнаружено исследований нежелательных явлений, связанных с нормальным питанием, содержащим BCAA, или с введением дополнительных доз до 9,75 г, но не был определен верхний допустимый уровень потребления (UL) из-за отсутствия данных доза-реакция. Исследования острого или хронического перорального приема BCAA не выявили побочных эффектов даже при высокой разовой дозе 60 граммов (Fernstrom, 2005). Интересующие результаты, измеренные в этих исследованиях, были связаны с физической работоспособностью, фенилкетонурией, циррозом печени, неврологическими и психическими заболеваниями. Однако трудно оценить, будут ли некоторые результаты, которые не считались неблагоприятными последствиями, проблемой в военных условиях. Например, изучив одно из исследований, в котором не сообщалось об отсутствии побочных эффектов, комитет пришел к выводу, что чрезмерное потребление BCAA может быть вредным; в этом исследовании пероральные дозы 10, 30 и 60 граммов BCAA вызывали небольшое увеличение латентного периода пространственной памяти у здоровых людей, но не вызывали изменений в обработке визуальной информации или распознавании образов (Gijsman et al., 2002). Авторы связывают повышенную латентность со сниженным соотношением (тирозин + фенилаланин) к BCAA, что приводит к снижению транспорта тирозина и фенилаланина через ГЭБ и, следовательно, к снижению синтеза дофамина.
Однако трудно оценить, будут ли некоторые результаты, которые не считались неблагоприятными последствиями, проблемой в военных условиях. Например, изучив одно из исследований, в котором не сообщалось об отсутствии побочных эффектов, комитет пришел к выводу, что чрезмерное потребление BCAA может быть вредным; в этом исследовании пероральные дозы 10, 30 и 60 граммов BCAA вызывали небольшое увеличение латентного периода пространственной памяти у здоровых людей, но не вызывали изменений в обработке визуальной информации или распознавании образов (Gijsman et al., 2002). Авторы связывают повышенную латентность со сниженным соотношением (тирозин + фенилаланин) к BCAA, что приводит к снижению транспорта тирозина и фенилаланина через ГЭБ и, следовательно, к снижению синтеза дофамина.
ДОКАЗАТЕЛЬСТВА, УКАЗЫВАЮЩИЕ ВЛИЯНИЕ НА УСТОЙЧИВОСТЬ
Исследования на людях
Клинических испытаний для проверки влияния BCAA на устойчивость к ЧМТ или связанным с ними заболеваниям или состояниям (например, субарахноидальное кровоизлияние, внутричерепная аневризма, инсульт, аноксическая или гипоксическая ишемия, эпилепсия).
Исследования на животных
Исследования на животных, посвященные повышению устойчивости к ЧМТ, не проводились. В одном исследовании изучалась возможность негативного влияния BCAA в высоких концентрациях. Contrusciere и коллеги (2010) заметили высокий риск бокового амиотрофического склероза среди профессиональных футболистов и предположили, что это может быть связано с чрезмерным потреблением спортивных напитков, содержащих BCAA. Эти напитки обычно содержат 1–3 грамма BCAA на порцию в 12 унций. Чтобы проверить свою гипотезу, авторы инкубировали культуры нейронов крыс с концентрациями 2,5–25 мМ BCAA и обнаружили, что эти чрезвычайно высокие дозы вызывают токсичность. Обратите внимание, что нормальные концентрации BCAA в спинномозговой жидкости человека на несколько порядков ниже и варьируются от ~ 5 до 15 мкМ (Garseth et al., 2001).
Был также проведен обзор литературы по исходам, связанным с болезненным процессом ЧМТ (например, субарахноидальное кровоизлияние, внутричерепная аневризма, инсульт, аноксическая или гипоксическая ишемия, эпилепсия). Поиск влияния BCAA на эпилепсию выявил несколько исследований, в которых изучалось их влияние либо на латентный период до приступа, либо на продолжительность приступа. В двух исследованиях использовались разные модели животных (приступы, вызванные пентилентетразолом или пикротоксином), но были получены сходные результаты: лейцин и изолейцин увеличивали латентный период припадков (показатель судорожного порога) по сравнению с контролируемым, сбалансированным раствором аминокислот (Dufour et al. ., 1999; Ски и др., 1994). Однако исследования различались по влиянию валина на латентный период; в то время как Skeie и коллеги (1994) обнаружили, что валин в дозе 300 мг/кг увеличивает среднее латентное время до начала судорог, исследование Dufour не обнаружило такого эффекта для валина.
Поиск влияния BCAA на эпилепсию выявил несколько исследований, в которых изучалось их влияние либо на латентный период до приступа, либо на продолжительность приступа. В двух исследованиях использовались разные модели животных (приступы, вызванные пентилентетразолом или пикротоксином), но были получены сходные результаты: лейцин и изолейцин увеличивали латентный период припадков (показатель судорожного порога) по сравнению с контролируемым, сбалансированным раствором аминокислот (Dufour et al. ., 1999; Ски и др., 1994). Однако исследования различались по влиянию валина на латентный период; в то время как Skeie и коллеги (1994) обнаружили, что валин в дозе 300 мг/кг увеличивает среднее латентное время до начала судорог, исследование Dufour не обнаружило такого эффекта для валина.
ДОКАЗАТЕЛЬСТВА, УКАЗЫВАЮЩИЕ ВЛИЯНИЕ НА ЛЕЧЕНИЕ
Исследования на людях
Только одно проспективное рандомизированное клиническое исследование изучало эффективность BCAA в качестве неотложного лечения ЧМТ (Ott et al.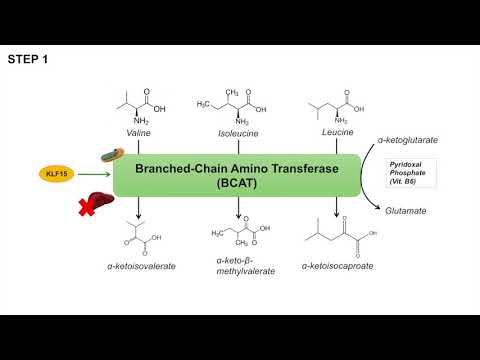 , 1988). Начиная с первого дня госпитализации, 20 пациентов с травмами головного мозга были рандомизированы для получения либо стандартной внутривенной аминокислотной смеси, либо смеси с более высоким процентным содержанием лейцина (154 процента от стандартной формулы), изолейцина (153 процента) и валина (174 процента). ). Формулы имели эквивалентные общие калории и белок. У пациентов, получавших смесь, обогащенную BCAA, был положительный баланс азота (+1,8%), тогда как у пациентов, получавших стандартную смесь, был отрицательный баланс (-8,0%) (Ott et al., 19).88).
, 1988). Начиная с первого дня госпитализации, 20 пациентов с травмами головного мозга были рандомизированы для получения либо стандартной внутривенной аминокислотной смеси, либо смеси с более высоким процентным содержанием лейцина (154 процента от стандартной формулы), изолейцина (153 процента) и валина (174 процента). ). Формулы имели эквивалентные общие калории и белок. У пациентов, получавших смесь, обогащенную BCAA, был положительный баланс азота (+1,8%), тогда как у пациентов, получавших стандартную смесь, был отрицательный баланс (-8,0%) (Ott et al., 19).88).
Опубликовано два небольших рандомизированных плацебо-контролируемых исследования, в которых сообщается, что добавки BCAA улучшают восстановление когнитивных функций у пациентов с ЧМТ (Aquilani et al., 2005, 2008). Тем не менее, в этих исследованиях ВСАА начинали вводить где-то через 19-140 дней после травмы, и поэтому не рассматривали эффективность ВСАА при лечении первичных или вторичных последствий нейротравмы.
Семь дополнительных исследований изучали прием добавок BCAA при других формах травм (обзор в De Bandt and Cynober, 2006). Из них четыре сообщили об отсутствии положительного влияния на баланс азота, тогда как три обнаружили положительные результаты. Количество пациентов в каждом исследовании, как правило, было небольшим (от 5 до 101, среднее значение = 31), и пациенты были неоднородны по типу и тяжести травмы.
Из них четыре сообщили об отсутствии положительного влияния на баланс азота, тогда как три обнаружили положительные результаты. Количество пациентов в каждом исследовании, как правило, было небольшим (от 5 до 101, среднее значение = 31), и пациенты были неоднородны по типу и тяжести травмы.
Проспективное рандомизированное контролируемое исследование пациентов, перенесших лечебную резекцию печени, показало, что периоперационное пероральное питание, включая BCAA, приводило к более высоким концентрациям эритропоэтина в сыворотке, чем контрольная диета (для пациентов, у которых не было гепатита). Авторы предположили, что более высокие концентрации эритропоэтина могут обеспечивать защиту от ишемического повреждения (Ishikawa et al., 2010).
Когда BCAA были добавлены в качестве дополнительной терапии к кетогенной диете детей с рефрактерной эпилепсией, 13 из 17 получили пользу, с уменьшением приступов на 50–100 процентов по сравнению с одной кетогенной диетой (Evangeliou et al. , 2009).). Авторы предположили, что BCAA могут не только повысить эффективность кетогенной диеты, но и облегчить ее переносимость пациентами из-за изменения соотношения жиров и белков.
, 2009).). Авторы предположили, что BCAA могут не только повысить эффективность кетогенной диеты, но и облегчить ее переносимость пациентами из-за изменения соотношения жиров и белков.
Исследования на животных
Коул и его коллеги сообщили, что у мышей с травмой головного мозга наблюдалось улучшение когнитивных функций при приеме питьевой воды с добавками BCAA (каждая BCAA в концентрации 100 мМ) через два дня после травмы (Cole et al., 2010). . Травма представляла собой 20-миллисекундный импульс давления физиологического раствора на твердую мозговую оболочку, а когнитивные функции, зависящие от гиппокампа, оценивали с помощью условной реакции страха. Реакция травмированных мышей уменьшилась примерно на 50% по сравнению с контрольной группой, в то время как поведение травмированных мышей, которые пили воду с добавками BCAA, не отличалось от контроля. В дополнение к поведенческим оценкам Cole et al. (2010) проанализировали синаптические функции in vitro. Возбуждающие постсинаптические потенциалы, генерируемые в срезах гиппокампа травмированных мышей, были снижены по сравнению с контрольной группой, но инкубация срезов с BCAA в концентрации 100 мкМ полностью восстанавливала синаптическую функцию (Cole et al. , 2010).
, 2010).
ВЫВОДЫ И РЕКОМЕНДАЦИИ
Лейцин и другие незаменимые аминокислоты необходимы, и их преимущества в увеличении синтеза белка и мышечной массы тела хорошо документированы. Тем не менее, пока нет убедительных данных, подтверждающих рекомендацию добавлять в рационы BCAA для облегчения или лечения ЧМТ. В пилотном исследовании есть некоторые указания на то, что BCAA могут действовать синергетически с кетогенной диетой при эпилепсии, одном из многих возможных последствий ЧМТ.
Единственное рандомизированное клиническое исследование (Ott et al., 1988) предполагает, что внутривенное вливание BCAA может быть полезным для поддержания положительного баланса азота после ЧМТ, но о влиянии BCAA на заболеваемость и смертность не сообщалось. Существует одно обнадеживающее исследование на животных, в котором мыши, получавшие BCAA (растворенные в воде в концентрации 100 мМ), показали улучшение когнитивных функций и снижение возбуждающих потенциалов в срезах гиппокампа (Cole et al. , 2010). Однако в целом недостаточно данных исследований на животных, чтобы поддержать начало исследований на людях.
, 2010). Однако в целом недостаточно данных исследований на животных, чтобы поддержать начало исследований на людях.
Поскольку большой процент военнослужащих принимает BCAA в качестве добавки к своему рациону, BCAA следует включать в оценку потребления пищи пациентами с ЧМТ в лечебных учреждениях для определения потребления пищи и состояния до травмы, а также потребления пищи на различных этапах лечения. Эти данные могут быть использованы для установления потенциальных взаимосвязей между потреблением/статусом питания до травмы и прогрессом восстановления.
РЕКОМЕНДАЦИЯ 8-1. Министерству обороны следует продолжать отслеживать литературу о влиянии нутриентов, диетических добавок и диет на ЧМТ, особенно тех, которые рассмотрены в этом отчете, но также и других, которые могут стать потенциально эффективными в будущем. Например, несмотря на то, что доказательства не были достаточно убедительными, чтобы рекомендовать проведение исследований по BCAA, Министерству обороны следует отслеживать научную литературу на предмет соответствующих исследований.
ССЫЛКИ
Аквилани Р., П. Ядарола, А. Контарди, М. Боселли, М. Верри, О. Пасторис, Ф. Боски, П. Арсидиако и С. Вильо. 2005. Аминокислоты с разветвленной цепью улучшают восстановление когнитивных функций у пациентов с тяжелой черепно-мозговой травмой. Архив физической медицины и реабилитации 86 (9): 1729–1735. [PubMed: 16181934]
Аквилани, Р., М. Боселли, Ф. Боски, С. Вильо, П. Ядарола, М. Доссена, О. Пасторис и М. Верри. 2008. Аминокислоты с разветвленной цепью могут улучшить восстановление после вегетативного состояния или состояния минимального сознания у пациентов с черепно-мозговой травмой: экспериментальное исследование. Архив физической медицины и реабилитации 89 (9): 1642–1647. [PubMed: 18760149]
Коул, Дж. Т., К. М. Митала, С. Кунду, А. Верма, Дж. А. Элкинд, И. Ниссим и А. С. Коэн. 2010. Диетические аминокислоты с разветвленной цепью улучшают когнитивные нарушения, вызванные травмами. Proceedings of the National Academy of
 [Бесплатная статья PMC: PMC2806733] [PubMed: 19995960]
[Бесплатная статья PMC: PMC2806733] [PubMed: 19995960]Contrusciere, V., S. Paradisi, A. Matteucci, and F. Malchiodi-Albedi. 2010. Аминокислоты с разветвленной цепью вызывают нейротоксичность в культурах коры головного мозга крыс. Исследование нейротоксичности 17: 392–397. [PubMed: 19763733]
Де Бандт, Дж.-П. и Л. Кинобер. 2006. Терапевтическое применение аминокислот с разветвленной цепью при ожогах, травмах и сепсисе. Журнал питания 136:308С–313С. [PubMed: 16365104]
Dufour, F., K.A. Nalecz, M.J. Nalecz и A. Nehlig. 1999. Модуляция судорожной активности, вызванной пентилентетразолом, аминокислотами с разветвленной цепью и α-кетоизокапроатом. Исследование мозга 815 (2): 400–404. [PubMed: 9878852]
Евангелиоу, А., М. Спилиоти, В. Дулиоглу, П. Калайдопулу, А. Илиас, А. Скарпалезу, И. Кацаника, С. Каламицу, К. Василаки, И. Хациоанидис, К. Гарганис, Э. Павлоу, С. Варламис и Н. Николаидис.
 2009. Аминокислоты с разветвленной цепью в качестве дополнительной терапии к кетогенной диете при эпилепсии: пилотное исследование и гипотеза. Детский журнал Неврология 24 (10): 1268–1272. [PubMed: 19687389]
2009. Аминокислоты с разветвленной цепью в качестве дополнительной терапии к кетогенной диете при эпилепсии: пилотное исследование и гипотеза. Детский журнал Неврология 24 (10): 1268–1272. [PubMed: 19687389]Фернстром, Дж. Д. 2005. Аминокислоты с разветвленной цепью и функция мозга. Journal of Nutrition 135(6 Suppl.): 1539S–1546S. [PubMed: 15930466]
Гарсет М., Л. Р. Уайт и Дж. Аасли. 2001. Небольшие изменения в аминокислотах спинномозговой жидкости при подтипах рассеянного склероза по сравнению с острой полирадикулоневропатией. Международная нейрохимия 39(2):111–115. [PubMed: 11408089]
Гийсман, Х. Дж., А. Скарна, К. Дж. Хармер, С. Ф. Б. Мактавиш, Дж. Одонтиадис, П. Дж. Коуэн и Г. М. Гудвин. 2002. Исследование по определению дозы воздействия аминокислот с разветвленной цепью на суррогатные маркеры функции дофамина в головном мозге. Психофармакология 160 (2): 192–197. [PubMed: 11875637]
МОМ (Институт медицины).
 2005. Справочное потребление энергии, углеводов, клетчатки, жира, жирных кислот, холестерина лестерина, белка и аминокислот . Вашингтон, округ Колумбия:
Издательство национальных академий. [PubMed: 12449285]
2005. Справочное потребление энергии, углеводов, клетчатки, жира, жирных кислот, холестерина лестерина, белка и аминокислот . Вашингтон, округ Колумбия:
Издательство национальных академий. [PubMed: 12449285]МОМ. 2006. Питательный состав пайков для кратковременных, высокоинтенсивных боевых действий . Вашингтон, округ Колумбия: Издательство национальных академий.
Исикава Ю., Х. Ёсида, Ю. Мамада, Н. Таниай, С. Мацумото, К. Бандо, Ю. Мидзугути, Д. Какинума, Т. Канда и Т. Тадзири. 2010. Проспективное рандомизированное контролируемое исследование краткосрочного периоперационного перорального питания с аминокислотами с разветвленной цепью у пациентов, перенесших операцию на печени. Гепато-гастроэнтерология 57(99–100):583–590. [PubMed: 20698232]
Либерман, Х. Р., Т. Б. Ставиноха, С. М. Макгроу, А. Уайт, Л. С. Хадден и Б. П. Марриотт. 2010. Использование пищевых добавок среди военнослужащих армии США.
 Американский журнал клинического питания 92(4):985–995. [PubMed: 20668050]
Американский журнал клинического питания 92(4):985–995. [PubMed: 20668050]Мэтьюз, Д. Э. 2005. Наблюдения за введением аминокислот с разветвленной цепью у людей. Journal of Nutrition 135(6 Suppl.):1580S–1584S. [Бесплатная статья PMC: PMC2268017] [PubMed: 15930473]
Ott, L.G., JJ Schmidt, AB Young, DL Twyman, RP Rapp, PA Tibbs, RJ Dempsey и CJ McClain. 1988. Сравнение введения двух стандартных внутривенных аминокислотных смесей пациентам с тяжелыми повреждениями головного мозга.
Ски, Б., А. Дж. Петерсен, Т. Мэннер, Дж. Асканази и П. А. Стин. 1994. Влияние валина, лейцина, изолейцина и сбалансированного раствора аминокислот на порог судорожной готовности к пикротоксину у крыс. Фармакология Биохимия и поведение 48(1):101–103. [PubMed: 8029279]
Вагенмакерс, Эй Джей М. 1999. Аминокислотные добавки для улучшения спортивных результатов.