характеристика, формула, воздействие на организм и правила применения

© designer491 — stock.adobe.com
Аспарагиновая кислота представляет собой одну из 20 важнейших аминоскислот организма. Она существует как в свободном виде, так и в качестве составляющего компонента белка. Способствует передаче нервных импульсов от центральной нервной системы к периферической. Входит в состав многих биодобавок, применяемых спортсменами.
Характеристика
Химическая формула аспарагиновой кислоты представляет собой прозрачные кристаллы. Вещество имеет и другие названия – аминоянтарная кислота, аспартат, аминобутандиовая кислота.
Максимальной концентрации аспарагиновая кислота достигает в клетках головного мозга. Благодаря возбуждающему воздействию на клетки ЦНС улучшает способность усвоения информации.
Взаимодействуя с фенилаланином, аспартат образует новое соединение, используемое как пищевой подсластитель – аспартам. Он является раздражителем нервной системы, поэтому добавки с его содержанием не рекомендуются к применению у детей, чья нервная система не окончательно сформирована.
Значение для организма
Укрепляет защитные функции организма, увеличивая количество выработанного иммуноглобулина и антител.
- Борется с хронической усталостью.
- Участвует в формировании других необходимых для нормальной жизнедеятельности организма аминокислот.
- Способствует доставке минералов к ДНК и РНК.
- Улучшает работу мозга.
- Нормализует работу нервной системы.
- Выводит из организма токсины.
- Помогает бороться со стрессом и депрессиями.
- Участвует в процессе преобразования углеводов в энергию.
Формы аспарагиновой кислоты
Аминокислота имеет две основные формы – L и D. Они являются зеркальным отображением друг друга по молекулярному составу. Зачастую производители на упаковках с добавками объединяют их под одним названием – аспарагиновая кислота. Но у каждой формы свой функционал.
L-форма аминокислоты содержится в организме гораздо в большем количестве, чем D. Она активно участвует в синтезе белка, а также играет ведущую роль в выведении токсинов, особенно, аммиака. D-форма аспартата регулирует выработку гормонов, улучшает работу мозга. Преимущественно встречается лишь в организме взрослого человека.
Значение L-формы
Широко используется для производства протеинов. Ускоряет процесс образования мочи, что способствует скорейшему выведению токсинов из организма. L-форма аспарагиновой кислоты активно участвует в синтезе глюкозы, благодаря чему в организме образуется больше энергии. Это свойство широко применяется среди спортсменов, которым из-за интенсивных нагрузок требуется колоссальный запас энергии в клетках.
Значение D-формы
Данный изомер способствует нормальному функционированию нервной системы, а также играет важную роль в репродуктивной функции женщин. Максимальной концентрации достигает в мозге и органах половой системы. Оптимизирует выработку гормона роста, а также ускоряет синтез тестостерона, что повышает выносливость организма. Благодаря данному эффекту аспарагиновая кислота получила популярность среди тех, кто регулярно занимается спортом. Она не влияет на скорость роста мышц, но позволяет увеличивать степень нагрузок.
Аминокислота в спортивном питании
Как уже было сказано выше, аспарагиновая кислота влияет на выработку гормонов. Она ускоряет синтез соматотропина (гормона роста), тестостерона, прогестерона, гонадотропина. В совокупности с другими компонентами спортивного питания, способствует наращиванию мышечной массы тела и предотвращает снижение уровня либидо.
Благодаря способности расщеплять белки и глюкозу, аспартат повышает количество энергии в клетках, компенсируя ее затраты во время тренировок.
Пищевые источники кислоты
Несмотря на то, что аминокислота при нормальном функционировании организма вырабатывается им самостоятельно, при интенсивных тренировках потребность в ее концентрации увеличивается. Получить ее можно, применяя в пищу бобовые культуры, авокадо, орехи, фруктовые несладкие соки, говядину и мясо птицы.

© nipadahong — stock.adobe.com
Биологически активные добавки
Рацион питания спортсменов не всегда восполняет потребность в аспартате. Поэтому многие производители предлагают биологически активные добавки, в состав которых входит данный компонент, например:
- DAA Ultra от Trec Nutrition.
- D-Aspartic Acid от AI Sports Nutrition.
- D-Aspartic Acid от Be First.
Благодаря увеличению скорости выработки гормонов появляется возможность усиливать нагрузку, а также ускоряется процесс восстановления организма.

Дозировка
Рекомендуемая норма потребления добавки составляет 3 грамма в сутки. Их необходимо разделить на три приема и употреблять в течение трех недель. После этого нужно сделать перерыв в 1-2 недели и повторить курс заново. При этом необходимо сохранять режим тренировок, постепенно увеличивая нагрузки.
Форма выпуска
Для применения можно выбрать любую удобную форму выпуска. Добавки выпускаются в виде порошка, капсул и таблеток.
Противопоказания
Ввиду того, что в молодом здоровом организме аминокислота вырабатывается в достаточном количестве, употреблять ее дополнительно не нужно. Особенно противопоказано ее применение у кормящих и беременных женщин, а также детей младше 18 лет.
Сочетаемость с другими компонентами спортивного питания
Для спортсменов важным фактором применения добавок является их сочетание с другими составляющимии рациона. Аспарагиновая кислота не подавляет действие активных компонентов спортивного питания и хорошо сочетается с различными протеинами, гейнерами. Главное условие – сделать 20-минутный перерыв между приемами.
С осторожностью следует принимать аминокислоту с другими препаратами, которые увеличивают выработку гормона тестостерона, иначе появляется риск возникновения гормонального сбоя.
Побочные действия и передозировка
- Аминокислота может вызвать избыточную выработку тестостерона, что приведет к появлению акне, выпадению волос.
- Повышение количества эстрогенов в крови может вызвать обратное действие и понизить либидо, а также стать причиной воспаления простаты.
- При избытке аспарагиновой кислоты может возникнуть излишняя возбудимость нервной системы и агрессия.
- Не рекомендуется принимать добавку позже 18:00, так как она подавляет выработку мелатонина.
- Передозировка аминокислоты приводит к нарушениям в работе нервной системы, метеоризму, расстройствам желудка, сгущению крови, сильным головным болям.

Научный консультант проекта. Физиолог (биологический факультет СПБГУ, бакалавриат). Биохимик (биологический факультет СПБГУ, магистратура). Инструктор по хатха-йоге (Институт управления развитием человеческих ресурсов, проект GENERATION YOGA). Научный сотрудник (2013-2015 НИИ акушерства, гинекологии и репродуктологии им. Отта, работа с маркерами женского бесплодия, анализ биологических образцов; 2015-2017 НИИ особо чистых биопрепаратов, разработка лекарственных средств) Автор и научный консультант сайтов по тематике ЗОЖ и науке (в области продления жизни) C 2019 года научный консультант проекта Cross.Expert.
Редакция cross.expert
Аспарагиновая кислота — функции, дефицит
Аспарагиновая кислота (aspartic acid), иные наименования – аминоянтарная кислота, аспартат, аминобутандиовая кислота – заменимое аминокислотное соединение, являющееся строительным блоком белков.«Заменимое соединение» означает, что организм способен синтезировать его, даже если он не получает аминокислоту из продуктов питания. Максимальное количество этой аминокислоты вырабатывается у людей до 35 лет. После этого возраста выработка этого соединения снижается.
Аспартат выполняет роль нейромедиатора в центральной нервной системе.Аспарагиновая кислота обеспечивает полноценное функционирование каждой клетки организма. Она играет роль в синтезе и высвобождении гормонов. Аспартат чрезвычайно важен для организма, поскольку именно он отвечает за правильную передачу нервных импульсов.Данный нейромедиатор оказывает стимулирующее действие на центральную нервную систему и активирует мозговые процессы.Достаточный уровень соединения необходим для концентрации внимания и обучения.

Функции
Эта аминокислота обеспечивает поддержании энергетического потенциала организма. Участвует в орнитиновом цикле – биохимических процессах, в результате которых азотсодержащие продукты распада трансформируются в мочевину, которая выводится из организма почками. Аспартат принимает участие в реакциях трансаминирования – переносе a-аминогруппы с аминокислоты на а-кетокислота.
Эта аминокислота необходима для умственной выносливости и здоровья головного мозга. Недавно было обнаружено, что аспарагиновая кислота очень важна для поддержания здорового генетического фонда, для производства иммуноглобулина и синтеза антител.Считается, что аспартат помогает организму стимулировать метаболизм. Именно поэтому вещество нашло применение в лечении астении и синдрома хронической усталости.
Производство энергии
Аспарагиновая кислота жизненно важна для создания и поддержания клеточной активности. Он транспортирует молекулы коферментного никотинамидадениндинуклеотида (НАД) из клетки в митохондрии. Здесь организм использует НАД производства аденозинтрифосфата (АТФ). Этот кофермент работает, чтобы транспортировать химическую энергию по клетке, облегчая обмен веществ.
Следовательно, чем выше доступность НАД в клетке, тем больше АТФ может быть произведено. Это приводит к здоровому обмену веществ, что отражается на увеличении энергетических ресурсов организма.
Иммунная функция
Аспарагиновая кислота важна для производства иммуноглобулинов и антител. Это молекулы гликопротеина, продуцируемые лейкоцитами (плазматическими клетками). Они являются важным компонентом иммунной функции организма.
Иммуноглобулины и антитела отвечают за распознавание и связывание с антигенами, такими как вирусы и бактерии. Они также помогают уничтожать эти инородные агенты. Существует множество различных пять классов (изотипов) иммуноглобулинов, и без аспартата организм не может синтезировать многие из этих соединений.
Генетика
Чтобы организм вырабатывал здоровую РНК и ДНК, ему требуется аспарагиновая кислота. Эта аминокислота обеспечивает доставку компонентов, необходимых клеткам для репликации ДНК и РНК.В отсутствие достаточного количества аспартата могут возникнуть генетические мутации.
Когнитивные функции
Это химическое вещество важно для полноценной высшей нервной деятельности, поскольку оно снабжает нейроны энергией. Достаточный энергетический потенциал необходим для поддержания необходимого уровня определенных химических веществ и нейротрансмиттеров в головном мозге. Достигаемый благодаря аспарагиновой кислоте энергетический потенциал для синтеза требуемых нейромедиаторов обеспечивает функции внимания, мышления, памяти. Например, для сосредоточения и удержания внимания структурам головного мозга требуется большой объем энергии. Соответственно, при энергодефиците, человек будет страдать невнимательностью и не сможет усвоить новую информацию.
Удаление токсинов
Вырабатываемые эндогенные токсины представляют собой побочный продукт клеточной активности. Аспартат помогает удалить токсины, такие как аммиак. Но если организм не может наладить синтез аспарагиновой кислоты, уровень аммиака в организме возрастает.
Аммиачное отравление (гипераммониемия) характеризуется развитием опасных для жизни состояний – комы с вероятным летальным исходом. Продолжительное увеличение концентрации аммиака проявляется симптомами угнетения ЦНС. Определяется вялость, снижение тонуса мускулатуры, нарушения дыхания (апноэ), изменение зрачковых реакций, потеря аппетита и отказ от еды). На психическом уровне наблюдается ступор. Длительная гипераммониемия приводит к развитию умственной отсталости.
Репродукция
Аспарагиновая кислота также важна в нейроэндокринной системе. Эта аминокислота играет весовую роль в регулировании производства и выделения определенных гормонов. В гипофизе аспартат стимулирует секрецию пролактина, обеспечивая производство молока у млекопитающих.
Вещество обеспечивает выработку лютеинизирующего гормона. Лютеотропин необходим для нормальной работы репродуктивных органов.Он важен для синтеза тестостерона у мужчин и регуляции менструального цикла и овуляции у женщин. Соединение также регулирует синтез и высвобождение гормона роста.

Дефицит
Поскольку организм способен вырабатывать собственную аспарагиновую кислоту, дефицит встречается редко. Нехватка аспартата обычно определяется только у людей, в рационе которых недостаточно присутствует белковая пища, или у тех, кто страдает от недоедания или расстройства пищевого поведения. Также при некоторых болезненных состояниях увеличивается потребность организма в аспарагиновой кислоте. Например, при патологиях, вызванных значительной умственной и физической перегрузкой, при депрессивных состояниях, сопровождающихся быстрой утомляемостью, астенических явлениях обнаруживается дефицит аспарагина.
При недостатке аспарагиновой кислоты снижаются физические возможности человека. Ухудшается обмен веществ. Одним из распространенных симптомов низкого уровня аспарагиновой кислоты является хроническая усталость и снижение выносливости.Несколько исследований показали, что спортсмены или люди, страдающие хронической усталостью, могут извлечь выгоду из увеличения потребления этой аминокислоты. Кроме того, что дополнительный прием аспартата может помочь поднять уровень энергии, это также способно освободить организм от избытка аммиака. Высокий уровень аммиака и низкая концентрация аспарагиновой кислоты приводят к повреждению мозга, печени и нервной системы. Некоторые из общих симптомов дефицита аспарагина включают раздражительность, плохую концентрацию внимания, потерю энергии, хронические головные боли и непереносимость продуктов с высоким содержанием белка.
Существует связь между низким уровнем этой аминокислоты и дефицитом магния и кальция. Такое явление способствует возникновению иных проблем со здоровьем, часто со стороны сердечно-сосудистой системы.
Пищевые источники
Поскольку аспарагиновая кислота является заменимой аминокислотой, организм способен вырабатывать ее самостоятельно. Это соединение присутствует во многих продуктах питания:
- говядина;
- молочные продукты;
- сахарный тростник;
- мясо птицы;
- морепродукты;
- патока сахарной свеклы;
- спаржа;
- авокадо;
- устрицы.
Аспарагиновая кислота входит в состав многих пищевых добавок. Для людей, занимающихся спортом, где важна физическая выносливость, такие добавки целесообразно регулярно принимать.
Соединение присутствует в некоторых лекарственных препаратах, например, в препарате калия и магния аспартат (Potassium aspartate & magnesium aspartate). Средство используют при нарушениях сердечного ритма, при стенокардии и для профилактики инсульта.
Следует помнить, что чрезмерные дозы этой аминокислоты могут иметь тот же эффект, что и потребление слишком большого количества белка. Это может повредить почки и печень, увеличивая риск развития подагры. Как и с любым лекарственным средством, необходимо проконсультироваться с медицинским работником перед началом приема.
Заключение
Аспарагиновая кислота – важное соединение, являющееся переносчиком ионов калия и магния через клеточные мембраны. Аспартат – незаменимое вещество для образования энергии и обеспечения жизнедеятельности клеток. Достаточный уровень нейромедиатора обеспечивает стабильную полноценную психическую деятельность. Дефицит аспарагиновой кислоты приводит к угнетению функций центральной системы и гипераммониемии – состоянии, способном спровоцировать кому и летальный исход.
АСПАРАГИНОВАЯ КИСЛОТА — Большая Медицинская Энциклопедия
АСПАРАГИНОВАЯ КИСЛОТА (α-аминоянтарная кислота, 1-аминоэтан-1,2-дикарбоновая кислота) — природная аминокислота; важнейшая составная часть белков. Структурная формула:
L-аспарагиновая кислота вращает плоскость поляризации света вправо: |а|25 D = + 6,7° в воде и +33,8° в 5н. HCl. Из всех природных аминокислот у аспарагиновой кислоты наиболее выражены кислотные свойства, ее Изоэлектрическая точка лежит при pH = 2,8; соответственно, константы кислотной диссоциации — рК=1,88, рК2 = = 3,65. Аспарагиновая кислота впервые была получена при кислотном гидролизе амида аспарагиновой кислоты — аспарагина (см.), а затем и из гидролизатов белков [Риттгаузен (H. Ritthausen), 1868]; формула аспарагиновой кислоты установлена Либихом (J. Liebig) в 1833 году аспарагиновая кислота наряду с другими аминокислотами является важнейшей составной частью белков. В составе белков, в свободном состоянии, а также в виде аспарагина и других производных широко распространена в органах и тканях различных организмов. Среди производных аспарагиновой кислоты следует упомянуть N-ацетил-аспарагиновая кислота, которая в заметных количествах содержится в тканях мозга, а также в других тканях. Аспарагиновая кислота, может синтезироваться в организме человека и животных из других веществ и, таким образом, относится к заменимым аминокислотам (см.). Однако для некоторых микроорганизмов аспарагиновая кислота является необходимым фактором роста и обязательно должна присутствовать в питательной среде. Являясь одним из промежуточных продуктов обмена азотистых веществ, аспарагиновая кислота играет важнейшую роль в обмене веществ. Особенно большую роль наряду с глутаминовой кислотой она играет в реакциях переаминирования (см.), перенося аминогруппы на кетокислоты, образуя ряд других аминокислот, превращаясь при этом в щавелевоуксусную кислоту и связывая, таким образом, пути азотистого обмена с окислительными превращениями безазотистых соединений (см. Азотистый обмен, Окисление биологическое). В этих же реакциях аспарагиновая кислота образуется из щавелевоуксусной кислоты после присоединения к ней аминогруппы, отдаваемой какой-либо из других аминокислот.
Образуя аспарагин, аспарагиновая кислота выполняет важную роль, связывая, обезвреживая и перенося аммиак в тканях животных и растений. При расщеплении аспарагина под действием фермента аспарагиназы (К.Ф.3.5.1.1) выделяется аммиак и образуется аспарагиновая кислота.
У бактерий аспарагиновая кислота распадается на аммиак и фумарат или синтезируется из названных продуктов под действием фермента аспартазы (L-аспартат-аммиак-лиазы; К .Ф.4.3.1.1).
У микроорганизмов распространено также декарбоксилирование аспарагиновой кислоты под действием декарбоксилаз аспарагиновой кислоты. (см. Декарбоксилирование).
Аспарагиновая кислота участвует в образовании в организме ряда биологически важных соединений. Так, аспарагиновая кислота является источником 3-го (азотного) и 4, 5 и 6-го (углеродных) атомов пиримидинового кольца, которое образуется из аспарагиновой кислоты и карбамилфосфата через стадии карбамиласпарагиновой, дигидрооротовой и оротовой кислот. При образовании пуриновых нуклеотидов аспарагиновая кислота в присутствии ГТФ аминирует инозиновую кислоту, превращая ее в адениловую кислоту (АМФ) с промежуточным образованием аденилянтарной кислоты. В цикле образования мочевины аспарагиновая кислота аминирует цитруллин, образуя аргининянтарную кислоту, которая далее распадается на аргинин и фумаровую кислоту.
Библиография: Браунштейн А. Е. Биохимия аминокислотного обмена, с. 173, М., 1949; Майстер А. Биохимия аминокислот, пер. с англ., М., 1961; G гееп-stein J. P. a. W i n i t z M. Chemistry of the amino acids, v. 3, N.Y.—L., 1961; Meister A. Biochemistry of the amino acids, N. Y.— L., 1965.
И. Б. Збарский.
Аспарагиновая кислота | Химия онлайн
Аспарагиновая кислота (аспартат) – заменимая алифатическая аминокислота.
Аспарагиновая кислота – продукт промежуточного обмена азотистых веществ в организме.
Аспарагиновая кислота синтезируется в организме из других веществ. Она подвергается окислительному дезаминированию в тканях печени, почек, слизистой оболочке клеток.
Аспарагиновая кислота содержится в мозге в высоких концентрациях.
Аспарагиновая аминокислота относится к моно-аминокарбоновым кислотам, в составе белков, в свободном состоянии, в виде аспарагина и других производных содержится в органах и тканях различных организмов.
Аспарагиновая кислота — 2-аминобутандиовая или α-аминоянтарная кислота.
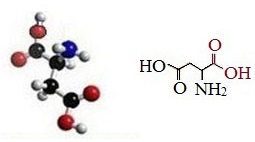
Аспарагиновая кислота (Асп, Asp, D) – НООС-СН2-СН(NН2) -СООН, участвует в синтезе ряда незаменимых аминокислот (метионина, треонина).
Аспарагиновая кислота, выделена в 1868 Г.Г. Риттхуазеном из белкового
гидролизата конглутина.
Суточная потребность нашего организма в аспарагиновой кислоте — 6 грамм.
Физические свойства
Аспарагиновая кислота – бесцветное кристаллическое вещество, плавится с разложением 2700С. Аспарагиновая кислота плохо растворяется в воде, практически не растворима в спирте и эфире.
Биологическая роль
Аспарагиновая кислота является важнейшей составной частью большинства белков. Аспарагиновая кислота важна в работе иммунной системы и синтезе ДНК и РНК, аппарате наследственности, клеточном росте, в процессе деления клеток.
Как промежуточный продукт обмена азотистых веществ аспарагиновая кислота играет важную роль в обмене веществ в организме. Перенося аминогруппы на кетокислоты, образуя ряд других аминокислот, превращаясь в щавелевоуксусную кислоту, аспарагиновая кислота связывает азотистые соединения. Образуя аспарагин, аспарагиновая кислота обезвреживает аммиак в тканях.
Как донор азота в реакциях аспарагиновая кислота играет важную роль в белковом обмене, участвует в одном из этапов синтеза мочевины, являясь предшественником биосинтеза в организме ряда аминокислот, пиридиновых оснований и других биологически активных соединений.
Специфическое свойство аспарагиновой кислоты – ее способность переносить ионы К+ и Mg2+ во внутриклеточное пространство, стимулирует межклеточный синтез фосфатов.
Аспарагиновая кислота оказывает выраженное антигипотоксическое действие.
Аспарагиновая кислота обладает иммуномодулирующим действием, повышает физическую выносливость, нормализует баланс возбуждения и торможения в центральной нервной системе, защитным действием в отношении воздействия радиации.
Аспарагиновая кислота, кроме того улучшает условия кровообращения и увеличивает потребления кислорода в миокарде.
Аспарагиновая кислота оказывает выраженное детоксицирующие действие при отравлении животных эндотоксинами сальмонелл и кишечных палочек.
Аспарагиновая кислота и ее производные снижают уровень аммиака в крови при заболевании печени, способствуя улучшению функционального состояния печени являясь метаболитом, аспарагиновая кислота выполняет роль переносчика ионов K+, Na+, Mg2+ и др.
Благодаря этим свойствам аспарагиновая кислота может служить в качестве основы для синтеза лекарственных препаратов, применяемых в случаях необходимости ввода данных ионов внутрь клетки.
Встречается во всех организмах в свободном виде и в составе белков.
Аспарагиновая кислота обеспечивает превращение углеводов в
мышечную энергию, широко используется в качестве добавок для спортсменов, в период повышенных нагрузок, повышает активность иммунной системы, увеличивает сопротивляемость к утомлению, сохраняет способность к работе, на выносливость, участвует в реакциях цикла мочевины, образует метионин, треонин и лизин.
Природные источники
Аспарагиновая кислота встречается во фруктовых соках и овощах. Также аспарагиновая кислота содержится в картофеле, томатах, кокосе, люцерне, арахисе, мясе (говядина, курица), молоке, яйцах, рыбе, морепродуктах, спарже, сое.
Лекарственные препараты
Специфическое свойство аспарагиновой кислоты переносить ионы калия и магния во внутриклеточное пространство было с успехом использовано для создания панангина (аспаркама) -препарата, предназначенного для лечения сердечной аритмий.
При этом аспарагиновая кислота не только выступает как переносчик ионов, но и сама является эффективным средством нормализации углеводнофосфатного обмена в сердечной мышце.
В кардиологии успешно используется панангин-препарат, содержащий калия аспарагинат и магния аспарагинат. Он оказывает выраженное антиритмическое действие и применяется при нарушения ритма.
Панангин показан при коронарной и сердечной недостаточности, явлениях переутомлениях, дефиците калия и магния в организме во время операций на сердце.
Полимикроэлементный препарат оркомин (комплекс органических соединений микроэлементов) — нормализует изменения при старении, обменные процессы, активирует функцию печени и является эффективным антианемическим средством.
Фармакологическое действие аспаркама
Источник калия (К+) и магния (Mg2+) регулирует метаболические процессы, способствует восстановлению электролитного баланса, оказывает антиаритмическое действие.
Ионы К+ участвует как в проведении импульсов по нервным волокнам, так и в осуществлении мышечных сокращений, поддержания нормальной сердечной деятельности. Нарушение обмена иона К+ приводит к изменению возбудимости нервов и мышц. В малых доза иона К+ расширяет коронарные артерии в больших дозах – суживает.
Ион Мg2+ участвует в процессах, обеспечивающих поступление и расходование энергии, в балансе электролитов, транспорте ионов, проницаемости мембран, нервно-мышечной возбудимости.
Сыворотка, выравнивающая тон кожи
(Сыворотка, выравнивающая тон кожи Luminosity PRO)
Основным действующим компонентом сыворотки является осветляющая L-аспарагиновая кислота, которая присутствует в человеческом организме – это одна из аминокислот, которая присутствует в человеческом организме и отвечает за синтез белков.
Функция этой кислоты в косметологии – уменьшение проявлений пигментных пятен, а также выравнивание тона кожи и борьбы с ее тусклым видом, а специальный компонент – экстракт зерен пшеницы – уменьшает проявление морщин.
Аминокислоты
Классификация аминокислот
аспарагиновая кислота и аспарагин: функции, биосинтез
Аспарагиновая кислота иначе аспартат вместе с большим братом глутаминовой кислотой (глутаматом) относят к дикарбоновым аминокислотам, т.е. соединениям, имеющим два кислотных хвоста СООН. Важность этих соединений такова, что они вместе с амидами составляют половину всего аминного азота тканей, а в нервной системе они составляют 70% всех аминокислот. Прочитайте статью до конца и вы узнаете, в чем важность аспарагиновой кислоты и аспарагина для организма человека. С вами Галина Батуро и аспарагиновая кислота.
Аспарагиновая кислота: структурная формула
Аспарагиновая кислота (аспартат) имеет 2 оптических изомера, которые условно называются L-аспартат и D-аспартат. Природная протеиногенная аминокислота относится к L – изомерам, D- изомер встречается в организме человека в свободном виде, но выполняет свои специфические функции и в состав белка не входит. Далее речь пойдет об L-аспарагиновой кислоте и ее производном аспарагине.
Аспарагиновая кислота входит в состав практически всех белков организма. Так как атомы водорода на кислотных хвостах очень подвижны, они обеспечивают водородные связи, которые формируют вторичную и третичную структуру белковых молекул, стабилизируя их в водной среде. Благодаря наличию двух кислотных хвостов, ее относят к кислым аминокислотам. Кислотные хвосты придают аминокислоте гидрофильные свойства, т.е. она хорошо растворяется в воде. Это имеет значение, т.к. все ферментативные реакции идут в водной среде, а аспарагиновая кислота – весьма активный участник биохимического конвейера.
Аспарагиновая кислота присутствует в плазме крови в сравнительно небольшом количестве, всего 0,01-0,07 мг\на 100 мл. плазмы крови. Наличие аспарагина в плазме крови заслуживает внимания, его содержание 0,6-1,4 мг\на 100 мл. плазмы крови, т.е. почти в 100 раз больше. Аспарагиновая кислота является преобладающим аминокислотным компонентом животных тканей. А вот с мочой в свободном состоянии она почти не выводится.
Аспарагин: структурная формула
Аспарагин представляет собой амид аспарагиновой кислоты, т.е. у второго кислотного хвоста атом водорода замещен на вторую аминную группу. Получается, как бы вторая голова, притороченная к хвосту. В мире химических соединений этим никого не удивишь.
На наше счастье аспарагиновая кислота и аспарагин являются заменимыми аминокислотами, т.е. организм сам синтезирует их на своей биохимической фабрике из соединений — предшественников, которые всегда имеются в достатке. Аспарагин представляет собой широко-распространенное соединение. Он накапливается в значительных концентрациях у некоторых видов высших растений, а также содержится в свободном состоянии в тканях животных.
Аспарагиновая кислота и аспарагин относятся к глюкогенным соединениям. В процессе биосинтеза они превращаются в ОксалАцетат, который либо сгорает с образованием энергии, в цикле Кребса, либо идет на синтез гликогена, который является депо глюкозы в организме и по мере надобности превращается в глюкозу.
Функции аспарагиновой кислоты
- Структурная – входит в состав практически всех белков
- Участие в биосинтезе
- Энергетическая
- Является депо аминных групп
- Участвует в обезвреживании аммиака
- Транспортная
- Является нейромедиатором
- Иммунная активность
Синтез аспарагиновой кислоты и фермент АСТ
Синтез аспарагиновой кислоты непрерывно идет в организме. Еще бы, ведь она вместе с глутаминовой кислотой является этаким складом аминных групп Nh3. Аминокислоты превращаются друг в друга в реакциях переаминирования. При поступлении аминокислот в организм, ферменты трасферазы рубят аминные головы и насаживают их — нет, не на колья — а синтезируя глутамат и аспарагинат. Активным участником реакции переаминирования является пиридоксальфосфат или витамин В6. Он заставляет работать фермент трансферазу, принимая на себя аминную голову от глутамата и передавая ее оксалацетату, который превращается в аспарагиновую кислоту. Оксалацетат — продукт превращения глюкозы в Цикле Кребса, он сам может превратиться в глюкозу, а может стать источником аспарагиновой кислоты.
Фермент АспартатАминоТрансфераза, иначе говоря АСТ (АсАТ) имеет как цитоплазматическую, так и митохондриальную формы. В наибольшем количестве он содержится в клетках сердечной мышцы (миокарде) и печени (гепатоцитах), в значительных количествах он имеется в скелетной мускулатуре. Содержание его в крови очень низкое, т.е. данный фермент является органоспецифичным. Заметно, что максимальный уровень фермента имеется в сократительных клетках, которые выполняют механическую работу (кардиоциты, миоциты), т.е. там, где выделяется много аминного азота. Клетки печени также выполняют специфическую работу по утилизации лишнего аминного азота, синтезируя из вредного аммиака безвредную мочевину. Для всех этих целей требуется аспарагиновая кислота.
При разрушении клеток сердца, печени или скелетной мускулатуры при заболевании (инфаркт миокарда, гепатит, травмы) фермент АСТ поступает в кровь, и его содержание значительно увеличивается. Увеличение АСТ имеет диагностическое значение и свидетельствует о процессе, сопровождающемся разрушением клеток внутренних органов, в первую очередь сердечной мышцы, печени, поджелудочной железы, скелетной мускулатуры при обширных травмах.
Синтез аспарагина
Аспарагиновая кислота является источником аспарагина, приобретая дополнительную аминную группу Nh3. Казалось бы чего проще: взять аммиак, которого всегда полно и который просто необходимо обезвредить, присоединить его к аспарагиновой кислоте — и вот он, аспарагин.
Такая реакция действительно существует. Она идет при участии АТФ под действием фермента АммиакЗависимой АспарагинСинтетазы у многих бактерий. Относительно человека мнения корифеев разнятся: некоторые считают, что данная реакция не характерна для высших животных, другие утверждают обратное. Одно можно сказать наверняка: прямой синтез аспарагина из аспарагиновой кислоты и аммиака не является ведущим у человека. У людей преимущественно протекает другая реакция: см. ниже.
Донором аминной группы для синтеза аспарагина в клетках человека выступает глутамин. При участии фермента ГлутаминЗависимой АспарагинСинтетазы, он отдает одну аминную голову аспарагиновой кислоте, и сам превращается в глутаминовую кислоту. Реакция идет при участии АТФ, от которой отщепляются два остатка фосфорной кислоты, при этом АТФ превращается в АМФ. Синтез аспарагина — энергозатратный процесс, для осуществления которого требуется химическая энергия, запасенная в фосфорных связях АТФ.
Функции аспарагиновой кислоты: синтез
Аспарагиновая кислота — родоначальник многих важных соединений. Она необходима для синтеза другой дикарбоновой кислоты — глутаминовой (глутамата), из нее образуется аспарагин, на ее основе строятся пиримидиновые нуклеотиды, она отдает атом азота для построения пуриновых нуклеотидов, она необходима для синтеза мочевины при утилизации вредного аммиака в печени, при этом образуется аминокислота аргинин. В головном мозге аспарагиновая кислота является источником N-ацетиласпарагиновой кислоты — вещества, необходимого для синтеза миелина — изолятора нервного волокна. Из аспарагиновой кислоты образуется оксалацетат, который в свою очередь запускает энергетический Цикл Кребса. Оксалацетат также является источником глюкозы, которая обеспечивает организм энергией. При участии аспарагиновой кислоты образуется АМФ (АденазинМоноФосфорная кислота), которая является заготовкой для энергетической молекулы АТФ (АденазинТриФосфорная кислота), образующейся в Цикле Кребса. Таким образом аспарагиновая кислота сопрягает пластический и энергетический обмен, а также обмен аминокислот, нуклеотидов и углеводов.
- Аспарагиновая кислота является источником аспарагина. Синтез из аммиака при участии фермента АммиакЗависимойАспарагинСинтетазы и из глутамина при участии фермента ГлутаминЗависимойАспарагинСинтетазы рассмотрен выше.
- Аспарагиновая кислота является предшественником другой дикарбоновой аминокислоты – глутаминовой (глутамата).
В организме постоянно происходит переброс аминных групп с аспартата на глутамат и наоборот. Переброс осуществляется через небезызвестный оксалацетат при участии фермента трансферазы (АСТ) и пиридоксальфосфата (витамин В6).
3. Аспарагиновая кислота является источником для построения пиримидиновых нуклеотидов, которые необходимы для обновления информационных матриц клетки ДНК и перебросе информации при синтезе белка через РНК. Синтез осуществляется через сложную цепь реакций, в которой на начальном этапе задействован КарбамилФосфат (тот же, что и в синтезе мочевины при обезвреживании аммиака). Промежуточным соединением выступает оротовая кислота, которая является строительным материалом для синтеза пиримидинов
4. Аспарагиновая кислота отдает атом азота для построения пуриновых нуклеотидов, также входящих в состав информационных матриц клетки ДНК и участвующих в синтезе белка РНК. Было установлено, что аспарагиновая кислота является источником атома N1 пуриновых нуклеотидов.
5. Синтез АМФ — АденозинМоноФосфорной кислоты. АМФ является предшественником АДФ — АденозинДиФосфорной кислоты, из которой присоединением фосфорного хвоста образуется АТФ — АденозинТриФосфорная кислота — молекула, обеспечивающая клетку химической энергией, запасенной в фосфорных связях. Заготовкой для АМФ выступает инозиновая кислота (ИМФ). Аспарагиновая кислота отдает аминную группу Nh3. Энергией реакцию обеспечивает ГТФ (ГуанидинТриФосфорная кислота). Для синтеза также необходимы ионы Магния.
6. В головном мозге аспарагиновая кислота является источником для синтеза N-Ацетил Аспарагиновой кислоты. Это вещество образуется в митохондриях нейронов из аспарагиновой кислоты и АцетилКоА. Реакция идет при участии фермента Аспартат-N-АцетилТрансферазы (ANAT). Из митохондрий N-АцетилАспартат поступает в олигодендроциты и астроциты — клетки нервной глии, или клетки-помощники, питающие и поддерживающие нервные клетки. N-АцетилАспартат является предшественником другого важного нейротрансмиттера N-АцетилАспартилГлутамата. Также N-АцетилАспартат регулирует осмотическое давление в головном мозге, он участвует в синтезе миелина — вещества, образующего электроизолирующую оболочку отростков нервных клеток.
Функции аспарагиновой кислоты: энергия
Аспарагиновая кислота является источником энергии для организма, недаром она содержится в наибольшем количестве в клетках, выполняющих работу: в кардиоцитах (клетках сердца), гепатоцитах (клетках печени), миоцитах (мускульных клетках). При участии фермента АСТ и пиридоксальфосфата (витамина В6) аспарагиновая кислота отдает аминную голову глутаминовой кислоте, а сама превращается в оксалацетат — вещество, запускающее энергетический Цикл Кребса. Каскад биохимических превращений способствует запасанию биохимической энергии в фосфорных связях молекул АТФ.
Оксалацетат при необходимости может стать источником для выработки глюкозы — молекулы, дающей энергию мышцам и нервной ткани. Аспартат является глюкогенной аминокислотой. При ее избытке, печень быстро переработает ее на гликоген, и это не самый печальный вариант. Глюкоза — источник жира. Жир тоже дает энергию, причем намного больше, только вот извлечь ее сложнее.
И это еще не все. Аспрагиновая кислота отдает свой азот для построения пуриновых нуклеотидов: аденина и гуанина. Аденин является основой молекулы, в которой запасена химическая энергия — АТФ — АденозинТриФосфорная кислота.
Также аспарагиновая кислота участвует в синтезе АМФ (АденозинМоноФосфорной кислоты) — это заготовка, к которой присоединяются дополнительные два фосфорных хвоста, чтобы получилась АТФ — высокоэргическая молекула, в фосфорных связях которой запасена химическая энергия.
Аспарагиновая кислота — вещество, обеспечивающее энергией биохимический конвейер.
Функции аспарагиновой кислоты: переаминирование
Аминный азот практически всех аминокислот (за исключением лизина, треонина и пролина) через посредство ферментов аминотрансфераз переходит на глутамат. Аминный азот этих трех аминокислот тоже в конечном итоге оказывается в составе глутаминовой кислоты, но более сложным путем. Так осуществляется депонирование аминного азота в организме. Накопление аминного азота в форме глутаминовой кислоты происходит в цитозоле клеток. Затем специфические ферменты транслоказы переносят глутамат в митохондрии, где активна специфическая АСТ. АСТ превращает глутамат опять в α-кетоглутарат, а тот вновь вступает в реакции переаминирования, принимая на себя аминные головы различных аминокислот, и вновь превращаясь в глутамат.
Аспартат (аспарагиновая кислота), образующийся в митохондриях в реакциях транс аминирования между оксалацетатом и глутаматом, может транспортироваться в цитозоль клетки, где он отдает аминную группу Nh4 в цикл мочевины, образуя аминокислоту аргинин. Это реакция, составляющая Аспартат-АргининоСукцинатный шунт, обеспечивают связь между путями, в которых утилизируется аминогруппы и углеродный скелет аминокислот. Утилизация аминогрупп в синтезе безвредной мочевины происходит в клетках печени, и в меньшей степени почек.
Реакции трансаминирования являются начальным этапом распада аминокислот в организме. В результате аминный азот через аспарагиновую кислоту перебрасывается на глутаминовую кислоту, а углеродный скелет либо сгорает в цикле Кребса с образованием энергии, либо идет на синтез глюкозы и кетоновых тел. Аспарагиновая кислота выступает посредником в передаче аминного азота в депо, каковым выступает глутаминовая кислота. Только глутаминовая кислота в тканях человека способна подвергаться прямому окислительному дезаминированию. Все остальные аминокислоты подвергаются непрямому дезаминированию с перебросом аминных групп Nh4 первоначально на глутаминовую кислоту, а вторым этапом происходит дезаминирование глутамата.
В мышечной ткани при интенсивной физической нагрузке функционирует другой путь непрямого дезаминирования с непосредственным участием аспарагиновой кислоты. Начальный путь такой же, как и при обычном непрямом дезаминировании, когда аминные группы почти всех аминокислот собираются на глутамат. Потом с глутамата они перебрасываются на аспартат (аспарагиновую кислоту), затем аминная голова с аспартата перекидывается на инозиновую кислоту (ИМФ), в результате получается АМФ. Аспартат, лишившись аминной головы, превращается в фумарат. Далее фумарат по цепочке Цикла Кребса превращается в малат, а тот в оксалацетат, который ловит аминную голову с глутамата, чтобы превратиться в аспартат. Так обеспечивается работа конвейера по переброске аминного азота со всего пула аминокислот на ИМФ. АМФ подвергается гидролитическому дезаминированию, т.е фермент АМФ-дезаминаза откусывает аминную голову у АМФ, получается ИМФ, которая опять готова к работе на конвейере и свободный аммиак Nh4.
Представленная схема отражает последовательность реакций непрямого окислительного дезаминирования в мышечной ткани при интенсивной физической нагрузке.
При интенсивной мышечной работе, когда задействован данный путь дезаминирования, одновременно утилизируется глюкоза с образованием молочной кислоты (лактата), что приводит к закислению внутренней среды клетки, а это нежелательно. Выделяющийся аммиак имеет щелочную реакцию и нейтрализует избыточную кислотность.
Можно выделить 4 стадии процесса:
- Трансаминирование с α-кетоглутаратом, образование глутамата
- Трансаминирование глутамата с оксалацетатом (фермент АСТ), образование аспартата
- Реакция переноса аминогруппы с аспаратата на инозиновую кислоту (ИМФ, ИнозинМоноФосфат), образование АМФ (АденозинМоноФосфат) и фумарата
- Гидролитическое дезаминирование АМФ с выделением аммиака Nh4.
Химические реакции первых двух стадий были представлены выше.
Третьей стадией является реакция переноса аминогруппы с аспартата на инозиновую кислоту происходит в два этапа. На первом этапе под воздействием фермента АденилоСукцитанСинтетазы Аспарагиновая кислота присоединяется к ИМФ, в результате образуется АденилоСукцинат. Процесс идет с затратой энергии, которую отдает ГТФ (ГуанозинТри Фосфат), при этом отщепляется остаток фосфорной кислоты, а ГТФ превращается в ГДФ (ГуанозинДиФосфат). Затем фермент АденилоСукцинат Лиаза расщепляет АденилоСукцинат на АМФ (АденозинМоноФосфат) и Фумаровую кислоту (Фумарат).
Фумаровая кислота отправляется на синтез оксалацетата, который превратится в аспарагиновую кислоту, позаимствовав аминную голову у глутамата. Так замыкается конвейер по транспортировке аминного азота. Отходы минимальны. Все (или почти все) возвращается в биохимический цикл.
Четвертым этапом образовавшийся АденозинМоноФосфат теряет амминую голову и вновь превращается в ИнозинМоноФосфат (ИМФ), который опять отправляется ловить аминную голову у аспартата.
Обезвреживание аммиака
При богатой белками пище аминокислот оказывается больше, чем их необходимо для синтеза белка. Избыток отправляется на плаху, каковая находится в печени. Ферменты рубят аминные головы, скелеты отправляются на переработку в цикл глюконеогенеза, а вот аминная голова начинает жить жизнью зомби, превращаясь в аммиак – клеточный яд. Та же страсть происходит и при интенсивной мышечной работе. Работа – это энергия, для энергии нужна глюкоза, чтобы получить глюкозу…. Ну вы поняли. Блуждающие аминокислотные головы в форме аммиака, которые опасны не менее сказочных упырей, необходимо обезвредить. Аспарагиновая кислота – один из участников этой героической саги.
В печени происходит магическое действо, где образующийся аммиак обезвреживается через каскад реакций, в одной из которых непосредственное участие принимает аспарагиновая кислота. Она участвует в реакции синтеза аргинина, необходимого для обезвреживания аммиака и синтеза мочевины. Аминная группа аспарагиновой кислоты переходит на аргинин. Подробности можно узнать здесь: Аргинин: структурная формула и биосинтез. Заканчивается все это волшебство образованием неопасной мочевины, которая выводится через почки. Половина азота, освобождающего в процессах биохимических трансформаций аминокислот, не образует аммиака, а сразу улавливается аспарагиновой кислотой и вовлекается в синтез мочевины.
Аспарагиновая кислота вместе с глутаминовой кислотой связывают, транспортируют и утилизируют биологически активный азот. Фактически, через две эти аминокислоты проходит весь азот, задействованный в обмене веществ. Аспарагиновая кислота способствует поддержанию азотистого равновесия в организме.
Продолжение об аспарагиновой кислоте читайте здесь: http://zaryad-zhizni.ru/asparaginovaya-kislota-i-golovnoy-mozg/
С вами была Галина Батуро и аспарагиновая кислота. Делитесь информацией в соц. сетях, оставляйте комментарии.
Аспарагиновая кислота — что это, полезные свойства и применение, польза и вред
Д-аспаргиновая кислота (DAA) содержится в продуктах питания, может синтезироваться в организме, но при повышенных нагрузках ее концентрации обычно недостаточно. Чтобы поднять тестостерон, ускорить рост мышечной массы и улучшить спортивные показатели, профессиональные бодибилдеры вводят в рацион добавки, обогащенные DAA.
аспарагиновая кислота: функции в организме человека
Физиологическая роль не ограничивается регулировкой формирования и работы ЦНС и эндокринной системы. Спортивное питание на основе Aspartic Acid:
-
Способствует укреплению иммунитета, увеличивает выработку иммуноглобулина и антител.
-
Противостоит ранней утомляемости и хронической усталости.
-
Стимулирует формирование других аминокислот и преобразование углеводов в энергию.
-
Участвует в обмене азотистых веществ и транспортировке микроэлементов в клетки.
-
Положительно влияет на работу головного мозга.
-
Выводит токсины.
-
Повышает устойчивость к стрессам, физическим и эмоциональным нагрузкам.
Среди уникальных способностей DAA – транспорт ионов, «протаскивание» ионов калия и магния сквозь клеточные мембраны. Калиево- магниевые соли аспарагиновой кислоты (аспартаты) продаются в магазинах здорового питания и используются в спорте для повышения физической выносливости за счет ускоренного выведения аммиака.
Состав и синтез аспарагиновой кислоты
DAA (аминоянтарная кислота, аспартат) – одна из 20-ти важных аминокислот, присутствует в организме в свободном виде и в составе белков. Максимальная концентрация вещества обнаружена в клетках головного мозга. Также может синтезироваться в тестикулах.
Установлено, что концентрация аминокислоты в растет до 35 лет, после чего снижается. То же самое выяснилось по отношению к тестостерону.
Аспарагиновая кислота в продуктах питания позволяет скорректировать недостаточную выработку DAA в организме. При повышенных нагрузках, в период реабилитации после травм, болезней и операций целесообразно ввести в рацион блюда с кукурузой, спаржей, яйцами, морской рыбой, птицей, говядиной. Вегетарианцам следует употреблять больше пищи с бобовыми, авокадо, соей, орехами, арахисом. Увеличить поступление аспартата с пищевыми источниками можно, если принимать казеиновый или соевый протеин.
При взаимодействии с фенилаланином DAA образует новое вещество – дипептид аспартама, подсластитель и сахарозаменитель, который используется в пищевой промышленности при производстве конфет, йогуртов, сладких газированных напитков.
Кому подходит
Добавки, содержащие, можно применять как для наращивания мышечной массы, так и во время сушки. Некоторые спортсмены предпочитают комбинировать аспартат с протеиновыми или аминокислотными комплексами, креатином. Отзывы о таких сочетаниях в основном положительные. Препарат универсален и может использоваться в культуризме, тяжелой атлетике, фитнесе, кроссфите.
Все данные о пользе DAA основаны на лабораторных исследованиях на животных и отзывах спортсменов, которые на свой страх и риск принимали аспарагиновую кислоту.Новички нередко отмечали, что эффекта от приема нет. Однако, по всей видимости, дело в неверно подобранной дозировке. Среди подтвержденных эффектов – подъем естественного уровня соматотропина, тестостерона и инсулиноподобного фактора роста (IGF-1).
В совокупности эти три вещества дают выраженный анаболический отклик при силовом тренинге, ускорение метаболизма, улучшение сексуальной функции у мужчин. Однако на повышенном уровне тестостерон держится около недели, после чего показатели возвращаются к исходным. Но если естественный уровень тестостерона повышенный, принимать Д-аспарагиновую кислоту мужчинам противопоказано.
Что касается целесообразности применения Aspartic Acid для женщин. Производители не рекомендуют такие добавки спортсменкам, так как нет достоверных сведений о воздействии вещества на женский организм. Однако аспартат способен положительно влиять на женское либидо и фертильность, поскольку входит в состав фолликулярной жидкости. Как и у мужчин, у женщин концентрация DAA c возрастом снижается, поэтому дополнительное поступление аспарагиновой кислоты – в продуктах питания или спортивных добавках – может позитивно отразиться на функционировании женской репродуктивной системы.
Действие
Д-аспаргиновая кислота является нейромедиатором – передатчиком нервных импульсов между нейронами. Еще одно свойство — влияние на уровень циклического аденозинмонофосфата (цАМФ), производного аденозинтрифосфата. Википедия и портал «Спортвики « говорят, что цАМФ как вторичный мессенджер улучшает внутриклеточное распространение адреналина, неспособного самостоятельно проникать сквозь клеточную мембрану. Как следствие, действие адреналина становится более выраженным, что проявляется ускорением липолиза (расщепления жиров) при одновременном замедлении синтеза жиров.
Говоря о тестировании на животных, нельзя не сказать, что не так давно проводилось исследование на людях. 23 человека ежедневно принимали DADAVIT (3 г аспартата) на протяжении 12 дней. Контрольная группа из 20 человек получала плацебо. По итогам выяснено, что у принимавших DAA уровень тестостерона вырос на 42%, гонадотропина – на 33%.
аспарагиновая кислота: польза для организма человека
Исследования и субъективное мнение людей, принимавших аспарагиновую кислоту и активно тренировавшихся, подтверждают: атлетам стоит использовать ее.
В спорте аспарагиновую кислоту ценят главным образом за способность увеличивать количество главного анаболического гормона. DAA влияет на высвобождение гонадотропин-релизинг фактора – гормона, регулирующего продукцию соматотропина. Соматотропин, в свою очередь, отвечает за секрецию тестостерона, гормона роста. Повышение либидо, прибавка выносливости, ускоренное восстановление мышц – заслуга DAA.
Вред ДЛЯ ОРГАНИЗМА
-
Неконтролируемое употребление аспарагиновой кислоты вызывает излишнюю возбудимость, немотивированную агрессию, раздражительность.
-
Чрезмерная концентрация тестостерона может спровоцировать себорею, акне, растяжки (стрии), гинекомастию и другие побочные эффекты.
-
Не исключено повышение эстрогенов, что приводит к снижению либидо и воспалению предстательной железы.
-
Так как аминокислота подавляет синтез мелатонина (гормона, облегчающего засыпание), не рекомендуется принимать препарат после 18 ч.
-
Метеоризм, проблемы с ЖКТ, головные боли – также следствие передозировки аспартатом и солями аспарагиновой кислоты.
Формы выпуска
Спортивные добавки выпускаются в порошковой, капсулированной, таблетированной формах.
Кроме D-изомера аспарагиновой кислоты существует другая форма аминокислоты – L-аспарагиновая кислота. Молекулы обоих форм являются зеркальным отражением друг друга.
На упаковках производители нередко пишут «aspartic acid», не указывая конкретно, какая из форм присутствует в составе. Однако свойства аспарагиновой кислоты зависят именно от типа изомера:
-
L-изомер присутствует в организме в большем количестве. Л-форма задействуется в синтезе протеинов, выведении токсинов и аммиака.
-
Функции D-изомера аспарагиновой кислоты – регулирование синтеза гормонов и функционирование нервной системы. Д-форма встречается преимущественно у взрослых.
L-изомер способен трансформироваться в D-изомер, но дополнительный прием Л-аспарагиновой кислоты не влияет на уровень тестостерона.
Применение в спорте и бодибилдинге
L-аспарагиновая кислота в бодибилдинге полезна для активации синтеза глюкозы (и, как следствие, восполнения запасов энергии).
Воздействие D-изомера аспарагиновой кислоты сказывается на работе мозга, фертильности женщин, силе и выносливости.
Аспартат, как выше сказано, усиливает продукцию гормона роста, прогестерона, пролактина, гонадотропина. В итоге массонабор происходит быстрее, а либидо держится на высоком уровне. Кроме того, расщепляя белки и глюкозу, аминокислота восполняет расход энергии во время нагрузок.
Показания к применению
DAA рекомендуют принимать:
-
Мужчинам старше 21 года при низком собственном тестостероне.
-
Атлетам, желающим повысить уровень анаболических гормонов без ААС.
-
Людям с пониженным половым влечением.
-
При долгом восстановлении после тренировок.
До начала применения аминокислоты надо сдать анализ на уровень тестостерона. Проверять уровень также требуется во время и после курса.
Противопоказания к применению
-
Беременность, лактация.
-
Возраст до 18 лет.
-
Высокое содержание естественного тестостерона.
Подтверждена нецелесообразность использования аспартата на ПКТ, так как он повышает пролактин.
Схема и нормы приема
Оптимальный вариант –— принимать аспартат по циклической схеме: 2-3 недели приема, 1-2 недели отдыха.
Порошковую аминокислоту размешивают в жидкости (воде, соке) и употребляют с пищей или в перерывах между едой. Дозы свыше 5 г DAA лучше разделить на утренний и дневной приемы.
Первый цикл лучше начинать с небольшой дозировки – 2-3 г в сутки, после оценки эффективности и переносимости можно постепенно увеличивать дозу, но не более чем до 20 г аспарагиновой кислоты в сутки. Большинству достаточно принимать ежедневно 5-10 г.
Порошок плохо растворяется в воде, прилипает к зубам и гортани. Чтобы суспензию было легче пить, лучше размешивать порошковую кислоту не в 200 мл воды, как советуют производители, а в 50 мл сока и после приема запивать таким же количеством жидкости. Других проблем с добавкой обычно не возникает.
Взаимодействие с другими средствами
Аспарагиновая кислота в продуктах питания и спортпите хорошо сочетается с другими добавками, не искажает их действие. Лучшие результаты дает комбинирование аспартата и протеинов, гейнеров, аминокислот, креатина моногидрата, ZMA. Главное, подождать 20 минут между приемами разных средств.
На форумах не советуют подключать DAA на ПКТ, но рекомендуют сочетать его с аргинина альфа-кетоглютаратом (ААКГ), L-карнитином, L-глютамином.
С осторожностью используют аспарагиновую кислоту с тестостероновыми бустерами (добавками, влияющими на синтез тестостерона).
DAA: универсальная аминокислота для спорта
Практикующие спортсмены, вне зависимости от дисциплины, остаются довольны действием аспарагиновой кислоты. В ТОП добавок с аспартатом входят:
-
DAA Xtreme PROLACT-BLOCK – капсулы с цинком, витаминами В6 и Е для антиоксидантной защиты и нормальной работоспособности.
-
D-Aspartic Acid от PLV – чистая аспарагиновая кислота в порошке без лишних ингредиентов. Одна порция содержит более 3 г DAA.
-
DAA Pro (Scitec Nutrition) – капсулы, обогащенные цинком и пантотеновой кислотой. Цинк нормализует тестостерон и синтез белков, пантотеновая кислота – поддерживает обмен веществ, противостоит утомляемости, улучшает синтез стероидных гормонов.
-
Athletic Xtreme Hard FX – тестобустер для роста мышц и быстрого восстановления.
Консультанты магазина сориентируют по составу и назначению добавок разных брендов, помогут выбрать оптимально подходящий продукт, ответят подробнее, как работает аспарагиновая кислота, что это такое и как ее применять.
Видео по теме «Аспарагиновая кислота»
Функции аспарагина и аспартата. Калий-магний аспарагинат
Аспарагин – моноамид аспарагиновой кислоты – одна из наиболее распространенных аминокислот природного происхождения. Впервые аспарагин найден в спарже, отсюда и произошло его название (на греч. спаржа – asparagos). Аспарагин и аспарагиновая кислота относятся к группе аминокислот, обладающих эндогенными свойствами, т.е. они могут поступать в организм с продуктами питания и могут синтезироваться самим организмом.
Большое количество аспарагина содержится в мясных продуктах.
Полезные свойства аспарагина:
- Помогает выводить вредный аммиак, образующийся в процессе превращения белков
- Способствует извлечению сложных углеводов
- Участвует в процессах детоксикации организма, помогая печени справляться с нагрузкой
- Поддерживает баланс в процессах, происходящих в ЦНС, препятствует чрезмерному торможению и возбуждению
- Участвует в регуляции эндокринной системы, высвобождая гормоны роста и пролактин
- Способствует усилению выработки тестостерона
- Служит сырьем для производства аспарагиновой кислоты
- Необходим для транспортировки минералов, участвующих в формировании и функционировании ДНК и РНК.
Аспарагиновая кислота (аминоянтарная кислота, аспартат) продуцируется из аспарагина, существует в свободном виде и в виде нейромедиатора в центральной нервной системе.
Польза и функции аспарагиновой кислоты:
- Играет важнейшую роль в обмене веществ
- Способствует деактивации аммиака, по этой причине L-аспартат входит в состав гепатотропного препарата под названием Гепа-Мерц (совместно с L-орнитином)
- Содержится в клетках мозга (нейронах), усиливая умственную активность
- Участвует в синтезе других аминокислот таких как аргинин, изолейцин, метионин, лизин и треонин
- Укрепляет иммунитет, повышает синтез антител и иммуноглобулинов
- Помогает в усвоении калия и магния
- Поддерживает эндокринную систему
- Помогает преобразовывать углеводы в энергию, наряду с глутаминовой кислотой
- Улучшает работу сердечной мышцы
- Способствует повышению физической выносливости организма
Избыток аспарагинов проявляется перевозбуждением нервной системы, повышенной агрессивностью, сгущением крови.
Суточная потребность в аспарагинах – 6 грамм, причем сюда входит не только аспарагин, но и аспарагиновая кислота и все аспарагинсодержащие продукты.
Богаты аспарагиновой кислотой пророщенные зерна ржи, спаржа, люцерна, картофель, соевые ростки, кокосы, арахис, бобы, яйца, мясо.
Потребность в аспарагинах возрастает:
- При заболеваниях, связанных с нарушением функционирования нервной системы
- При лечении сердечно-сосудистых заболеваний
- При психических расстройствах и депрессии
- При заболеваниях головного мозга
- При снижении работоспособности
- При ослаблении иммунитета
- При проблемах, связанных нарушением остроты зрения
- При усталости, с целью быстрого восстановления сил
Аспарагины в составе биологически активных добавок предлагает специализированный интернет-магазин IHerb, на сайте которого вы можете найти подходящий препарат, ознакомившись с отзывами.
Рассмотрите аспарагинат калия и магния от элитного бренда Solgar, который поддерживает здоровье мышц и костей, баланс электролитов, функции нервной системы, способствуя оздоровлению всего организма. В кардиологии препарат показал более высокую эффективность, чем аспаркам и панангин.
Купить калий-магний аспарагинат (90 растительных капсул) можно кликнув на фото ниже.
При оформлении покупки в поле «Промокод» укажите – LND618, чтобы гарантированно получить скидку 10%, действующую дополнительно ко всем остальным акциям и предложениям Айхерб.
Самая простая пошаговая инструкция «Как заказать на iHerb» находится здесь.
Добавки аспарагина не рекомендуется употреблять при повышенной выработке мужских половых гормонов, гипертонии, атеросклерозе.
В результате реакции аспарагиновой кислоты с фенилаланином образуется аспартам, который активно применяется в пищевой промышленности как подсластитель. Известно, что аспартам отрицательно действует на нервные клетки, особенно у детей и даже может спровоцировать развитие аутизма.
Частое потребление аспарагинатов противопоказано беременным женщинам, во избежание негативного влияния на здоровье плода.
Недавние исследования американских ученых показали, что большое количество аспарагина может быть опасным, так как увеличивает риск агрессивного развития рака молочной железы. Именно поэтому мы выбираем Ламинин, который отличается от других БАДов тем, что не имеет ограничений в использовании, побочных эффектов и противопоказаний. При этом, Laminine содержит комплекс из 22 аминокислот (в т.ч. аспарагин), необходимых для синтеза любого вида белка, а также молекулу ФРФ (Фактор Роста Фибробластов), регулирующую функцию каждой клетки нашего организма. В связи с чем, он применяется при лечении многих заболеваний, вплоть до онкологии. Узнать все о препарате Ламинин, его составе и применении, можно здесь.
Будьте здоровы и помните: вы на верном пути,
если уже не хочется оглядываться назад!
Аминокислоты аспартат — Большая химическая энциклопедия
| Рис. 2. Разложение аспартама на дикетопипера2ин и / или аспартилфенилаланин, а затем на аминокислоты аспарагиновую кислоту и фенилаланин (22). |
Neotame — это искусственный подсластитель, разработанный для преодоления некоторых проблем с аспартамом. Диметилбутиловая часть молекулы была добавлена для блокирования действия пептидаз, ферментов, которые разрывают пептидную связь между двумя аминокислотами, аспарагиновой кислотой и фенилаланином. Это снижает доступность фенилаланина, устраняя необходимость в предупреждении на этикетках, предназначенных для людей, которые не могут должным образом метаболизировать фенилаланин.[Стр.76]
Ферритин представляет собой глобулярный белок, запасающий железо, который хранит железо в виде FeJ +. Чтобы выйти из ферритина, Fe3 + необходимо сначала восстановить до Fe2 +. Ферритин имеет два типа каналов, через которые Fe + может выходить из трех каналов и четырех каналов. Трехкратный канал выстлан аминокислотами аспартатом (Asp) и глутаматом (Glu), а четыре канала — складчатый канал выстлан аминокислотой лейцином (Leu). По какому каналу Fe + с большей вероятностью покидает белок ферритин Объясните свой ответ.[Pg.901]
C HyNOi, α-аминокислота Аспарагиновая кислота W300 … [Pg.515]
Затем добавьте четыре боковые цепи в положения, отмеченные R, R2, Rz и Rj, чтобы получить окончательный структура пептида. Самая левая аминокислота, аспарагиновая кислота, находится на амино-конце. За аспарагиновой кислотой следуют метионин, валин и тирозин. Тирозин находится на конце карбоксила. Вот отдельные аминокислоты с выделенными их группами R … [Pg.947]
Результаты исследований вдыхания на животных предполагают, что сероводород может быть нейротоксикантом развития.Нейрохимические изменения (в частности, уровни нейромедиаторов гамма-аминомасляной кислоты, норэпинефрина и серотонина) и уровни аминокислот аспартата, глутамата и таурина наблюдались в различных областях мозга (Hannah et al. 1989, 1990 Skrajny et al. др. [Стр.108]
Связь дикарбоновых аминокислот, аспарагиновой и глутаминовой кислот с этим процессом также была изучена (106). Этому исследованию способствовал количественный метод определения (23) дегидрирования индикатор, резазурин, и продукт его восстановления, резоруфин.Использовались формы для разрушения древесины: Trameles cinnabarina и Lentinus lepideus. [Pg.75]
Открытие гомохиральности на такой планете, как Марс, могло бы стать отличным биомаркером и усилить аргументы в пользу жизни на Марсе. Если есть ВЭ в солнечной туманности, то на поверхности Марса должно быть ВЭ порядка 9 процентов, но остатки древней жизни на Марсе покажут больший избыток. Обмен энантиомерами происходит естественным образом в процессе, называемом рацемизацией, и для наиболее лабильной аминокислоты, аспарагиновой кислоты, период полураспада рацемизации составляет 800 лет при 300 К за 800 лет, половина небиотической аспарагиновой кислоты будет рацемизироваться и EE упадет до нуля.Однако в сухих условиях период полураспада намного больше, возможно, достигает 5 x 104 лет при 300 K. Экстраполяция скорости рацемизации до 215 K, экваториальной температуры Марса, увеличивает период полураспада до 3 x 1012 лет и 1027 лет при 150 К, марсианских полярных температурах. Следовательно, открытие значительного ЭЭ в марсианской почве было бы сильным индикатором древней марсианской жизни. [Pg.248]
Кристаллографические исследования подтвердили, что критическое различие в антиэстрогенном действии ралоксифена заключается во взаимодействии боковой цепи алкиламиноэтокси с аминокислотой аспартатом в положении 351.Своеобразная ориентация этой боковой цепи молекулы ралоксифена, важная детерминанта антиэстрогенных свойств препарата, как полагают, объясняет отсутствие у него эндометриальной активности (Clark et al., 1976, Grese et al., 1997, Bryant et al., 1998). . [Pg.283]
Sowden et al. [4] также провели подробный анализ аминокислот и аминосахаров в почвах из разных диматических регионов. Следующие аминокислоты были определены: кислые аминокислоты, аспарагиновая и глутаминовая кислоты, основные аминокислоты, аргинин, гистидин, лизин и орнитин, нейтральные аминокислоты, фенилаланин, тирозин, глицин, аланин, валин, лейдн, изолеудн, серин, треонин, пролин и гидроксипролин… [Pg.119]
Существует лишь небольшой набор небелковых аминокислот, которые содержат карбонильные группы в форме кетона, альдегида и фрагментов карбоновой кислоты как часть боковой цепи. Примеры, приведенные в таблице 6, представляют собой компоненты нерибосомальных пептидов, выделенных из бактерий или грибов, и сидерофоры из бактерий. Биосинтез этих аминокислот неясен, однако некоторые аминокислоты с боковыми цепями карбоновых кислот могут быть прослежены до L-a-аминокислот, аспарагиновой кислоты и глутаминовой кислоты.[Стр.32]
Аминокислоты, аспартат и глутамат, не извлекаются из крови, но синтезируются в головном мозге. Для этого требуется азот (для групп -Nh3), который получают из аминокислот с разветвленной цепью путем трансаминирования, как и в других тканях. [Pg.171]
Рассматриваемые аминокислоты представляют собой основные аминокислоты лизин, аргинин и гистидин, а также кислые аминокислоты аспарагиновой кислоты и глутаминовой кислоты. Функции боковой цепи этих аминокислот, ионизированные при pH 7 (см. Вставку 4.7), действуют как кислоты или основания. В обратной последовательности протоны можно приобретать или отдавать для регенерации конъюгированных кислот и конъюгированных оснований. [Pg.517]
Аминогруппа цистеамина связана с карбоксильной группой другого биогенного амина через амидную связь кислоты (-CO-NH-). [1-Аланин образуется в результате декарбоксилирования аспартата аминокислоты, но он также может образовываться в результате разложения пиримидиновых оснований (см. Стр. 186). [Стр.12]
Кислые аминокислоты, аспарагиновая кислота и глутаминовая кислота, имеют карбоксильные группы.[Pg.9]
Малат окисляется до оксалоацетата под действием малатдегидрогеназы (рис. 9.7). Эта реакция дает третий и последний НАДН цикла. [Примечание. Оксалоацетат также образуется путем трансаминирования аминокислоты, аспарагиновой кислоты.] … [Стр.111]
Атомы пуринового кольца представлены рядом соединений, включая аминокислоты (аспарагиновая кислота, глицин , и глутамин), CO2 и N10-формилтетрагидрофолат (рис. 22.5). Пуриновое кольцо построено серией реакций, в которых пожертвованные атомы углерода и азота добавляются к предварительно образованному рибозо-5-фосфату.(См. Стр. 145 для обсуждения синтеза рибозо-5-фосфата путем HMP.) … [Pg.291]
Атомы пурина вносят аминокислоты (аспарагиновая кислота, глутамин и глицин), CO2 и N10-формилтетрагидрофолиевая кислота. [Pg.494]
Из таблицы II видно, что в целом имеется хорошее согласие между отчетами различных лабораторий. Стоит отметить, что как Arens et al. (65) выяснили, что около 50% молекулы состоит всего из пяти аминокислот — аспарагиновой кислоты, треонина, аланина, валина и глицина.Еще предстоит выяснить, являются ли указанные различия результатом экспериментальных вариаций в анализах, реальных различий между штаммами или различных пропорций изоферментов в исследуемых ферментах. Как упоминалось в другом разделе, группа Байера (65) обнаружила … [Pg.111]
Из таблицы 3.3 следует отметить дополнительный момент. В то время как боковые цепи аминокислот (группы R), которые обычно заряжены при физиологическом pH, ограничены пятью аминокислотами (аспарагиновая кислота, глутаминовая кислота, лизин, аргинин и иногда гистидин), ряд потенциально ионизируемых групп R являются частью других аминокислоты.К ним относятся цистеин, серин, треонин и тирозин. Реакция ионизации -… [Pg.53]
РИСУНОК 11 Влияние концентрации фосфатного буфера (ионная сила) на хиральное разрешение (а) RF-эфедрина (), / -эфедрина (), (/ -норефедрина) () и / -ноэфедрин (O) и (b) дансиламинокислоты, аспарагиновая кислота (A), глутаминовая кислота (O), серин () и фенилаланин (V) на колонках / 1-CD (из ссылок. 65,70.) … [Pg.127]
.
Аминокислоты L-аспартат — Большая химическая энциклопедия
Существует множество других применений, в которых малеиновый ангидрид служит сырьем. Эти приложения доказывают универсальность этой молекулы. Популярный искусственный подсластитель аспартам [22839-47-0] представляет собой дипептид с одной аминокислотой (1-аспарагиновая кислота [56-84-8]), который получают из малеинового ангидрида в качестве исходного материала. Сообщалось о процессах производства поли (аспарагиновой кислоты) [26063-13-8] (184-186) с приложениями для этого биоразлагаемого полимера, предназначенными для моющих модифицирующих добавок, обработки воды и поли (акриловой кислоты) [9003-01-4 ] замена (184 187 188) (см. Моющие средства).[Pg.460]Оксалоацетат + α-аминокислота -> L-аспартат + α-кетокислота … [Pg.769]
Аспартам — общее название метилового эфира IV-ai-аспартил-L-фенилаланина. . Он состоит из двух аминокислот, L-аспарагиновой кислоты и L-фенилаланина, соединенных связью сложного метилового эфира. Он был открыт в 1965 году Дж. Шлаттером в лаборатории G.D. Searle. Это белый кристаллический продукт, и его растворимость в воде составляет 10 г / л при 20 ° C, этот показатель увеличивается при повышенных температурах и в кислых условиях (Ajinomoto Aspartame Technical Bulletin, 2003).Трудно растворим в других растворителях. [Pg.76]
Лиазы представляют собой привлекательную группу ферментов с коммерческой точки зрения, что было продемонстрировано их использованием во многих промышленных процессах240. Они катализируют расщепление CC, CN, CO и других связей другими способами, кроме гидролиза. , часто образуя двойные связи. Например, две хорошо изученные аммиаклиазы, аспартатаммиаклиаза (аспартаза) (EC 4.3.1.1) и фенилаланинаммиаклиаза (PAL) (EC 4.3.1.5), катализируют транс-элиминирование аммиака из аминокислот, l- аспартат и L-фенилаланин соответственно.Чаще всего в синтетическом режиме используется обратная реакция для получения L-аминокислот в тонном масштабе (схемы 19.30 и 19.31) .240 242 Эти реакции проводят при очень высоких концентрациях субстрата, так что равновесие смещается, что приводит к очень высокой конверсии в аминокислотные продукты. [Pg.379]
Другой пример, о котором также сообщили Уги и его сотрудники, — это комбинация пятицентровой 4-компонентной реакции Уги (U-5C-4CR) с Пассерини-3CR (Схема 16) [102] .Эта процедура с одним горшком использует a-аминокислоту (L-аспарагиновая кислота, 168) в качестве входного 2-центрального компонента, что объясняет происхождение U-5C-4CR. [Стр.120]
Алитам [L-a-аспартил-N- (2,2,4,4-тетраметил-3-тиетанил) -D-аланинамид] представляет собой подсластитель на основе аминокислоты. Это очень интенсивный подсластитель, обладающий подслащивающей способностью примерно в 2000 раз больше, чем сахароза. Он также демонстрирует чистый сладкий вкус, похожий на сахарозу. Хотя он метаболизируется, его нужно настолько мало, что его калорийность незначительна.Алитам получают из аминокислот, L-аспарагиновой кислоты, D-аламина и нового амина [9]. [Стр.194]
Тот факт, что примеси могут быть включены в результате роста на определенной поверхности, используется при легировании органических материалов для использования в электронике. Например, кристаллы триглицинсульфата легированы аланином по всей решетке за счет роста только на грани 010, удерживаемой в держателе кристаллов (White et al. 1976). Было обнаружено, что ряд аминокислот (L-аспарагиновая, L-валин, L-лейцин и L-фенилаланин) включается в решетку глутаминовой кислоты… [Pg.259]
Алитам [II] является питательным веществом, но из-за его сильной сладости используемые количества достаточно малы, чтобы его можно было рассматривать и классифицировать как непитательный подсластитель. Алитам образуется из аминокислот L-аспарагиновой кислоты и о-аланина с новым амидным фрагментом (образованным из 2,2,4,4-тетра-метилтиенаниламина). Алитам проявляет превосходную стабильность в различных условиях благодаря своей уникальной амидной группе. Alitame был одобрен … [Pg.4723]
L-треонин принадлежит к семейству аспарагиновых аминокислот.L-аспартат синтезируется из оксалоацетата, промежуточного продукта цикла TCA, аспартаттрансаминазой (таблица 14.1), которая кодируется геном aspC в E. coli (Fotheringham et al. 1986) и aspA в C. glutamicum (Marienhagen et al. . 2 (X) 5). На субстратах из углеводов, … [Pg.285]
Аспартам был открыт случайно Джимом Шлаттером, химиком из GD Searle в 1965 году. Джим Шлаттер работал над лекарствами для лечения язвы желудка, когда пролил немного аспартил- фенилаланин на руке.Позже он облизнул палец и заметил сладкий вкус соединения, которое позже стало аспартамом. Аспартам представляет собой метиловый эфир дипептида природных аминокислот L-аспарагиновой кислоты и L-фенилаланина. Существует четыре возможных диастереоизомера аспартама, но только аспартам обладает подслащивающими свойствами. Вкус аспартама нельзя было предсказать на основе его аминокислотных составляющих. [Стр.179]
Ферментативный процесс. Химически синтезированные субстраты могут быть преобразованы в соответствующие аминокислоты за счет каталитического действия фермента или микробных клеток в качестве источника фермента, t — производство аланина из L-аспарагиновой кислоты, производство L-аспарагиновой кислоты из фумаровой кислоты, производство L-цистеина из DL-2-аминотиазолин-4-катбоксильной кислоты, получение D-фенилглицина (и D — /> -гидтоксифенилглицина) из DL-фенилдантоина (и DL — /) — гидроксифенилгидантоина) и производство L-триптофана из индола и DL-серина были в эксплуатации как коммерческие процессы.Некоторые из других процессов, представленных в таблице 10, имеют достаточно высокий технический уровень, чтобы их можно было использовать в коммерческом производстве (24). Типичные химические реакции, используемые в ферментативном процессе, показаны на рис. 6. [Pg.291]
Это пептид, содержащий 27 аминокислотных остатков, содержащих аминокислоты L-гистидин (His) L-аспарагиновая кислота (Asp) L-серин. (Ser) глицин (Gly) L-треонин (Thr) L-фенилаланин (Phe) L-глутаминовая кислота (Glu) L-глутамин [Glu (NHj)] L-лейцин (Leu) L-аргинин (Arg) L -аланин (Ala) и L-валинамид (Va -NHj).[Pg.1371]
Удаление донора аминогруппы, L-аспарагиновой кислоты, привело к почти полному снижению активности. Ни проникновение клеток, ни добавление кофактора (пиридоксальфосфата) не были существенными для продукции L-фенилаланина. Максимальный выход конверсии имел место (100%, 22 г) при увеличении концентрации донора аминогруппы. Добавка аспарагиновой кислоты была лучшим донором аминогруппы по сравнению с добавкой глутаминовой кислоты. Использовали 35 г / л. [Pg.267]
Возможное объяснение превосходства донора аминогруппы, L-аспарагиновой кислоты, было получено в результате исследований, проведенных на мутантах E.coli, в которой присутствует только одна из трех трансаминаз, обнаруженных в E. coli. Считается, что в E. coli могут присутствовать трансаминаза с разветвленной цепью, ароматическая аминотрансаминаза и аспартатфенилаланин-аспартаза. Реакция каждого из этих мутантов с различными донорами аминогруппы дала результаты, которые показали, что трансминаза с разветвленной цепью и мутанты, содержащие ароматическую аминоаддтрансминазу, не способны достигать высоких уровней превращения фенилпировиноградной кислоты в L-фенилаланин.Однако мутанты, содержащие аспартатфенилаланинтрансаминазу, способны давать 98% конверсию на 100 ммоль 1 1 фенилпировиноградной кислоты. Объяснение этому, вероятно, состоит в том, что как трансаминаза с разветвленной цепью, так и трансминаза ароматических аминокислот ингибируются по обратной связи L-фенилаланином, тогда как аспартат-фенилаланин-трансаминаза не ингибируется L-фенилаланином. Кроме того, поскольку оксалоацетат, который образуется при использовании аспарагиновой кислоты в качестве донора аминогруппы, легко превращается в пировиноградную кислоту, ингибирования с участием оксалоацетата по обратной связи не происходит.Причиной низкого выхода конверсии некоторых штаммов E. coli может быть то, что эти штаммы E. cdi устойчивы к аспартатфенилаланинтрансаминазе. [Pg.268]
L-аспарагиназа, фермент, полученный из E. coli или Erwinia carotovora, использовался в химиотерапии рака, где его селективность зависит от существенной потребности некоторых опухолей в аминокислоте L-аспарагине. Нормальные ткани не нуждаются в этой аминокислоте, и поэтому фермент вводят с целью истощить опухолевые клетки аспарагина путем преобразования его в аспарагиновую кислоту и аммиак.Хотя L-аспарагиназа показала себя многообещающей при множестве экспериментально индуцированных опухолей, она применима только для людей для лечения острого лимфобластного лейкоза, хотя иногда ее применяют при миелоидном лейкозе. [Pg.476]
Аминокислота L-глутамат является основным возбуждающим нейротрансмиттером центральной нервной системы (Fonnum, 1984). Глутамат проявляет свое возбуждающее действие либо за счет активации нескольких метаботропных рецепторов глутамата, связанных с G-белком, либо за счет индукции ионных потоков различными классами ионотропных рецепторов.Рецептор NMDA — один из тех ионных каналов, управляемых глутаматом, который получил свое название от его селективного искусственного агониста NMDA (N-метил-D-аспартат) и который контролирует медленные, но постоянные потоки ионов Na +, K + и Ca2 + через клеточную мембрану. . [Pg.389]
Разделение трех аминокислот (1-валин, L-аланин и L-аспарагиновая кислота, 300 пМ) было обнаружено с использованием 0,5 мМ Ru (bpy) 2+ в рабочем буфере. Интенсивность излучения ECL можно увеличить, увеличив напряжение на электродах.Однако с плавающими электродами такое увеличение могло быть достигнуто только за счет увеличения разделяющего напряжения [725], … [Pg.206]
Подробности пути биосинтеза de novo показаны на рис. 15-16 . Аминокислота L-глутамин является субстратом, обеспечивающим атомы азота для реакций 1, 4 и 14, катализируемых амидофосфорибозилтрансферазой, FGAM-синтетазой и GMP-синтетазой соответственно. Глицин является субстратом в реакции 2, а L-аспартат — в реакциях 7 и 11. P-Rib-PP является субстратом и активатором амидофосфорибозилтрансферазы, которая ингибируется АМФ.IMP и GMP и полиглутаматные производные дигидрофолата. [Pg.440]
Также возможно преобразовать нехиральные легко доступные промышленные органические химические вещества в ценные хиральные природные аналоги. Это демонстрируется превращением ахиральной фумаровой кислоты в L (-) — яблочную кислоту с фумаразой в качестве активного фермента. Это же соединение превращается в аминокислоту L (-h) -аспарагиновую кислоту бактериями Escherichia, которые содержат фермент аспартазу. Если добавить бактерии pseudomonas, образуется еще одна аминокислота L-аланин (ур.9.10). [Pg.320]
Аспарагиназа — это фермент, который действует, расщепляя аминокислоту L-аспарагин до аспарагиновой кислоты и аммиака. Он препятствует росту злокачественных клеток, которые не могут синтезировать L-аспарагин. Сообщается, что его действие специфично для фазы Gi клеточного цикла. Он используется в основном для индукции ремиссии при остром лимфобластном лейкозе. [Стр.356]
.
Семейство аспартатных аминокислот — Большая химическая энциклопедия
Оба PAL / TAL принадлежат к семейству L-аминокислот аммиаклиазы, которая катализирует образование различных α, β-ненасыщенных кислот путем отщепления аммиака (иона аммония) от соответствующих L-ct-аминокислот. Это семейство белков включает аспартатаммиаклиазу (AAL), метиласпартатаммиаклиазу (MAL), HAL, … [Pg.557]Млекопитающие, грибы и высшие растения вырабатывают семейство протеолитических ферментов, известных как аспарагиновые протеазы.Эти ферменты активны при кислом (или иногда нейтральном) pH, и каждый из них имеет два остатка аспарагиновой кислоты в активном центре. Аспарагиновые протеазы выполняют множество функций (таблица 16.3), включая переваривание пепсина и эимозина), деградацию лизосомального белка (еатепсин D и E), а также регуляцию артериального давления. Ренин — аспарагиновая протеаза, участвующая в выработке отензина, гормона, который стимулирует сокращение гладких мышц и снижает выведение солей и жидкости). Аспарагиновые протеазы обладают разнообразной субстратной специфичностью, но обычно они наиболее активны в расщеплении пептидных связей между двумя гидрофобными аминокислотными остатками.Предпочтительные субстраты пепсина, например, содержат ароматические остатки по обе стороны от пептидной связи, которая должна быть расщеплена. [Pg.519]
Рецепторы V-метил-D-аспартата (NMDA) имеют множество регуляторных сайтов. На сегодняшний день идентифицированы три семейства субъединиц рецептора NMDA, одно из которых представлено одним геном (NR1, кодирующим белок из -900 аминокислот), … [Pg.276]
Аминокислотный биосинтез Семейство ароматических аминокислот Аспартат Семья Семейство глутаматов Семейство пирувата Семейство серинов Семейство гистидинов Другое… [Pg.385]
Помимо 0-метилирования аспартатных и глутаматных остатков, C-концевая карбоксильная группа GTPases метилирована. В семействе G-белков C-концевые цистеины пренилируются по последовательности CZZX, где Z представляет собой гидрофобную аминокислоту, а X представляет собой любой остаток. После того, как последовательность ZZX расщепляется специальной протеазой, изопренилцистеинкарбоксиметилтрансфераза (Icmt) метилирует C-концевую карбоксильную группу и эффективно создает более гидрофобный фермент…. [Pg.446]
Незаменимые аминокислоты — это те аминокислоты, которые возникают в результате трансаминирования из 2-оксокислот в промежуточном метаболизме. Они принадлежат к семейству глутамата (Glu, Gin, Pro, Arg, полученный из 2-оксоглутарата), семейству аспартата (только Asp и Asn в этой группе, полученному из оксалоацетата) и аланину, который может быть образован путем трансаминирования из пирувата. . Аминокислоты семейства серинов (Ser, Gly, Cys) и гистидин, которые возникают из промежуточных продуктов гликолиза, также могут синтезироваться человеческим организмом.[Pg.184]
Этот цинк-зависимый фермент [EC 3.4.17.1], член семейства пептидаз M14, катализирует гидролиз пептидных связей на С-конце полипептидов. Если С-концевой аминокислотой является аспартат, глутамат, аргинин, лизин или пролин, происходит слабое гидролитическое действие. Карбоксипептидаза A образуется из белка-предшественника, прокарбоксипептидазы A. [Pg.112]
Хотя L-фенилаланин является белковой аминокислотой и известен как белок-кислотный тип предшественника алкалоидов, его реальная роль в биосинтезе (обеспечение Атомы C и N) относится только к атомам углерода.L-фенилаланин является частью магии 20 (термин, использованный Криком в его обсуждении генетического кода), и именно по этой причине его следует также указать как белок-аминокислотный тип предшественника алкалоидов, хотя его функция в синтезе алкалоидов не связана с так же, как и другие белковые аминокислоты. Однако в отношении magic 20 необходимо отметить, что только часть этих аминокислот является хорошо известными предшественниками алкалоидов. Они образованы только из двух семейств аминокислот: гистидиновых и ароматических, а также из семейства аспартатов.[Стр.93]
Сульфат должен быть восстановлен до сульфида перед включением в аминокислоты Семейства аспартата и пирувата вносят свой вклад в синтез изолейцина … [Стр.487]
Аспартатное (оксалоацетатное) семейство аминокислот включает аспартат, аспарагин, метионин, лизин, треонин и изолейцин (см. рис. 21.1). Семейство пирувата включает аланин, валин, лейцин, а также лизин и изолейцин (см. Рис. 21.1). Треонин является предшественником изолейцина. Он превращается в изолейцин группой ферментов, которые также используются в синтезе валина (рис.21.10). [Стр.497]
Семейства аспартата и пирувата вместе содержат 11 аминокислот. Изолейцин считается членом обоих семейств из-за реакций, участвующих в его синтезе. Изолейцин и валин используют четыре общих фермента в своих биосинтетических путях. [Стр.506]
В ткани мозга низкие концентрации глутамата и аспартата действуют как нейротрансмиттеры, но при высокой концентрации эти аминокислоты действуют как нейротоксины. Основные успехи в области рецепторов возбуждающих аминокислот были достигнуты благодаря идентификации, характеристике и клонированию различных семейств рецепторов и транспортеров (Dingledine and McBain, 1999).Эти рецепторы и переносчики являются специализированными … [Стр.3]
.
20 аминокислот, входящих в состав белков | Улучшение жизни с помощью аминокислот | О нас | Глобальный веб-сайт Ajinomoto Group
В природе идентифицировано около 500 аминокислот, но только 20 аминокислот составляют белки, обнаруженные в организме человека. Узнайте об этих 20 аминокислотах.
Аминокислоты с разветвленной цепью (BCAA) представляют собой группу из трех аминокислот (валин, лейцин и изолейцин), которые имеют молекулярную структуру с разветвлением. BCAA богаты мышечными белками, стимулируют рост мышц в организме и обеспечивают энергию во время упражнений.
Глютамин — одна из самых распространенных аминокислот в организме. Глютамин защищает желудок и желудочно-кишечный тракт. В частности, глутамин используется для выработки энергии в желудочно-кишечном тракте. Глютамин способствует метаболизму алкоголя, защищая печень.
Аспартат — одна из аминокислот, наиболее пригодных для получения энергии. Аспартат — одна из аминокислот, наиболее близко расположенных к циклу трикарбоновых кислот (ТСА) в организме, который производит энергию.Цикл TCA подобен двигателю, который приводит в движение автомобили. Каждая клетка нашего тела производит энергию.
Бульон комбу, используемый в японской кулинарии, содержит глутамат. Глутамат является основой умами, а свободный глутамат содержится в комбу, помидорах и сыре. Внутри организма глутамат используется как важный источник незаменимых аминокислот.
Аргинин играет важную роль в открытии вен для улучшения кровотока. Оксид азота, который открывает вены, сделан из аргинина.Аргинин — полезная аминокислота для удаления избытка аммиака из организма. Аргинин повышает иммунитет.
Аланин поддерживает функцию печени. Аланин используется для производства глюкозы, необходимой организму. Аланин улучшает метаболизм алкоголя.
Пролин — одна из аминокислот, содержащихся в коллагене, который составляет ткань кожи. Пролин — одна из важнейших аминокислот естественного увлажняющего фактора (NMF), который сохраняет кожу влажной.
Цистеин уменьшает количество производимой черной пигментации меланина.Цистеина много в волосах на голове и теле. Истеин увеличивает количество желтого меланина, производимого вместо черного меланина.
Лизин — одна из наиболее часто упоминаемых незаменимых аминокислот. Такие продукты, как хлеб и рис, как правило, содержат мало лизина. Например, по сравнению с идеальным аминокислотным составом пшеница имеет низкое содержание лизина. Университет Организации Объединенных Наций провел исследование людей в развивающихся странах, которые зависят от пшеницы как источника белка, и обнаружил недостаток лизина в их рационе.Недостаток лизина и других аминокислот может привести к серьезным проблемам, таким как задержка роста и тяжелые заболевания.
Незаменимая аминокислота, которая используется для создания активного центра ферментов.
Аминокислота, обнаруженная из спаржи. И аспарагин, и аспартат расположены близко к циклу трикарбоновой кислоты (ТСА), который производит энергию.
Незаменимая аминокислота, которая используется для производства многих типов полезных аминов.
Аминокислота, используемая для производства фосфолипидов и глицериновой кислоты.
Незаменимая аминокислота, которая используется для производства множества различных веществ, необходимых организму.
Незаменимая аминокислота, вырабатываемая в организме. В организме много глицина. Он действует как передатчик в центральной нервной системе и помогает регулировать функции организма, такие как движение и сенсорное восприятие. Глицин составляет треть коллагена.
Тирозин используется для получения многих типов полезных аминов. Тирозин относится к группе ароматических аминокислот вместе с фенилаланином и триптофаном.
Незаменимая аминокислота, которая используется для производства гистамина.
Незаменимая аминокислота, используемая для производства многих типов полезных аминов.
.
