Исследование уровня общего кортизола в крови (автомат)
АНМО «Ставропольский краевой клинический консультативно-диагностический центр»:
355017, г. Ставрополь, ул. Ленина 304(8652) 951-951, (8652) 35-61-49 (факс)
(8652) 951-951, (8652) 31-51-51 (справочная служба)
Посмотреть подробнееОбособленное подразделение «Диагностический центр на Западном обходе»:
355029 г. Ставрополь, ул. Западный обход, 64(8652) 951-951, (8652) 31-51-51 (контактный телефон)
(8652) 31-68-89 (факс)
Посмотреть подробнееКлиника семейного врача:
355017 г. Ставрополь, пр. К. Маркса, 110 (за ЦУМом)(8652) 951-951, (8652) 31-51-51 (контактный телефон)
(8652) 31-50-60 (регистратура)
Посмотреть подробнееНевинномысский филиал:
357107, г. Невинномысск, ул. Низяева 1(86554) 95-777, 96-127, 95-873 (регистратура)
Посмотреть подробнееОбособленное структурное подразделение в г.
+7-988-700-81-06 (контактные телефоны)
Посмотреть подробнееОбособленное структурное подразделение в г. Элисте :
358000, г. Элиста, ул. Республиканская, 478(989) 735-42-07 (контактные телефоны)
Посмотреть подробнееЗАО «Краевой клинический диагностический центр»:
355017 г. Ставрополь, ул. Ленина 304(8652) 951-951, (8652) 35-61-49 (факс)
(8652) 951-951, (8652) 31-51-51 (справочная служба)
Посмотреть подробнееОбособленное структурное подразделение на ул. Доваторцев, 52А:
355037, г. Ставрополь, ул. Доваторцев, 52А8 (8652) 316-845 (контактный телефон)
Посмотреть подробнееОбособленное структурное подразделение на ул. Пригородная, 193:
355026, г. Ставрополь, ул. Пригородная, 193 8 (8652) 316-843 (контактный телефон)Посмотреть подробнееОбособленное структурное подразделение на ул.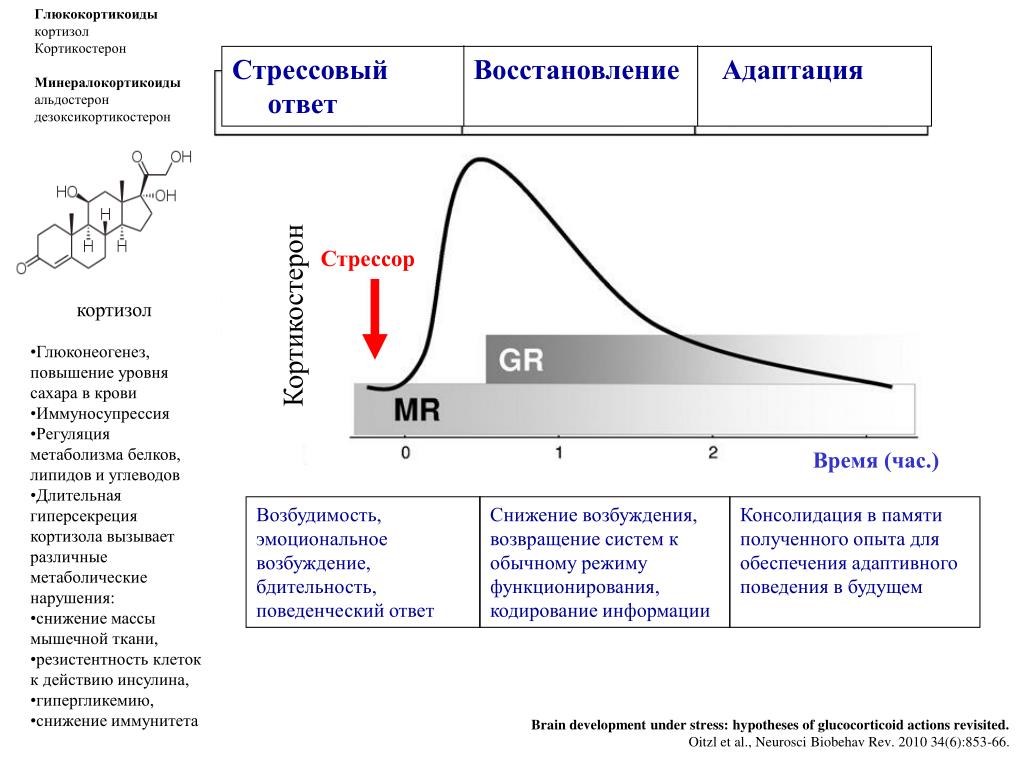 Савченко, 38 корп. 9:
Савченко, 38 корп. 9:
8 (8652) 316-847 (контактный телефон)
Посмотреть подробнееОбособленное структурное подразделение на ул. Чехова, 77 :
355000, г. Ставрополь, ул. Чехова, 778(8652) 951-943 (контактный телефон)
Посмотреть подробнееОбособленное структурное подразделение в г. Михайловске:
358000, г. Михайловск, ул. Ленина, 201 (в новом жилом районе «Акварель»).8(988) 099-15-55 (контактный телефон)
Посмотреть подробнееМаркеры нарушений гипофизарно-надпочечниковой системы — исследования, стоимость в Москве
Маркеры нарушений гипофизарно-надпочечниковой системы — исследования, стоимость в Москве | ФНКЦ ФМБА России- Главная страница
- org/ListItem»>Услуги и цены
- Анализы
- Маркеры нарушений гипофизарно-надпочечниковой системы
Адренокортикотропный гормон (АКТГ) выделяется передней долей гипофиза под влиянием регулирующих факторов гипоталамуса. Сильным стимулятором выделения является стресс. АКТГ — важнейший стимулятор гормонов коры надпочечников.
Кортизол – стероидный гормон, выделяемый корой надпочечников. Кортизол фильтруется в почечных клубочках и удаляется с мочой. У большинства пациентов нарушен нормальный суточный ритм колебания уровня кортизола в крови, но наиболее показательны концентрации, определяемые в 8 утра и 20 вечера. Содержание кортизола в крови может быть повышено у эмоциональных людей. При беременности может повышаться концентрация кортизола и нарушаться суточный ритм выделения.
Кортизол в моче отражает биологически активную форму циркулирующего в крови гормона. Определение кортизола в моче – основной тест при диагностике гиперфункции коры надпочечников. При нарушении метаболизма кортизола и почечной недостаточности количество выводимого с мочой кортизола может не отражать размеров его секреции. Ожирение и физическая нагрузка могут повышать количество кортизола, выводимого с мочой.
Определение кортизола в моче – основной тест при диагностике гиперфункции коры надпочечников. При нарушении метаболизма кортизола и почечной недостаточности количество выводимого с мочой кортизола может не отражать размеров его секреции. Ожирение и физическая нагрузка могут повышать количество кортизола, выводимого с мочой.
Альдостерон – стероидный гормон, синтезируется из холестерина в клетках клубочкового слоя коры надпочечников. Альдостерон участвует в процессах обмена калия, натрия и ионов водорода. Секреция альдостерона зависит от многих факторов: активности системы ренин-ангиотензин, содержания калия, АКТГ, магния и натрия в крови.
Диагностическое значение имеет повышение уровня АКТГ при болезни Иценко-Кушинга, болезни Адиссона, посттравматических и послеоперационных состояниях, синдроме Нельсона, приёме АКТГ, метопирона, инсулина, вазопрессина.
Снижение уровня АКТГ происходит при гиперфункции коры надпочечников, опухоли коры надпочечников, введении глюкокортикоидов, применении криптогептина.
Диагностическое значение имеет повышение уровня кортизола в крови при следующих заболеваниях: синдром Иценко-Кушинга, гипотиреоз, цирроз печени, декомпенсированный сахарный диабет, астматические состояния, острые инфекции, менингиты, акромегалия, артериальная гипертензия.
Снижение уровня кортизола в крови — при первичной гипофункции коры надпочечников, болезни Аддисона, нарушениях функции гипофиза.
Определение кортизола в моче имеет диагностическую ценность при синдроме и болезни Иценко-Кушинга, карциноме надпочечника.
Диагностическое значение имеет повышение уровня альдостерона при синдроме Крона (альдостерома, гиперплазия надпочечников), сердечной недостаточности, циррозе печени, нефротическом синдроме, синдроме Баретта, злокачественной ренальной гипертензии.
Снижение уровня альдостерона при: аддисоновой болезни, гипоальдостеронизме, сахарном диабете, алкогольной интоксикации, синдроме Лиддла.
Определение АКТГ, альдостерона, кортизола в моче с помощью иммуноферментного анализа. Определение кортизола в крови с помощью иммунохимического исследования на «Архитекте 2000».
ПодготовкаПеред проведением исследования сыворотки крови на АКТГ, альдостерон, кортизол необходимо воздержаться от физических нагрузок, приёма алкоголя и лекарств, изменений в питании в течение 24 часов до взятия крови. Рекомендуется сдавать кровь на исследование утром натощак (8-часовое голодание). В это время необходимо воздержаться от курения. Желательно утренний приём лекарственных средств провести после взятия крови (если это возможно). Не следует перед сдачей крови осуществлять следующие процедуры: инъекции, пункции, общий массаж тела, эндоскопию, биопсию, ЭКГ, рентгеновское исследование, особенно с введением контрастного вещества, диализ.
Если всё же была незначительная физическая нагрузка, нужно отдохнуть не менее 15 минут перед сдачей крови. Очень важно, чтобы точно соблюдались указанные рекомендации, так как только в этом случае будут получены достоверные результаты исследования крови.
Очень важно, чтобы точно соблюдались указанные рекомендации, так как только в этом случае будут получены достоверные результаты исследования крови.
Цель исследования – оценить функцию надпочечников.
Необходимо:· исключить приём алкоголя
· исключить физические нагрузки и стрессовые ситуации
· не курить!
Помните! На результаты исследования влияют некоторые лекарственные препараты. Информацию о влиянии конкретного лекарственного препарата Вы можете получить у лечащего врача. Для данного исследования необходимо собрать суточную мочу! (смотрите правила сбора суточной мочи). Обязательно указать суточный диурез! Очень важно, чтобы точно соблюдались указанные рекомендации, так как только в этом случае будут получены достоверные результаты исследования мочи.
Онлайн-консультации
Общение с врачом в формате видеоконференции и чата
Подробнее Записаться
Исследование уровня адренокортикотропного гормона в крови940 ₽
Исследование уровня альдостерона в крови1 060 ₽
Исследование уровня кортизола в суточной моче1 020 ₽
Исследование уровня общего кортизола в крови1 080 ₽
Прейскурант на все услуги нашего центра
В формате PDF В формате ExcelПрейскурант на профилактические медицинские осмотры
В формате PDF В формате ExcelОставьте заявку.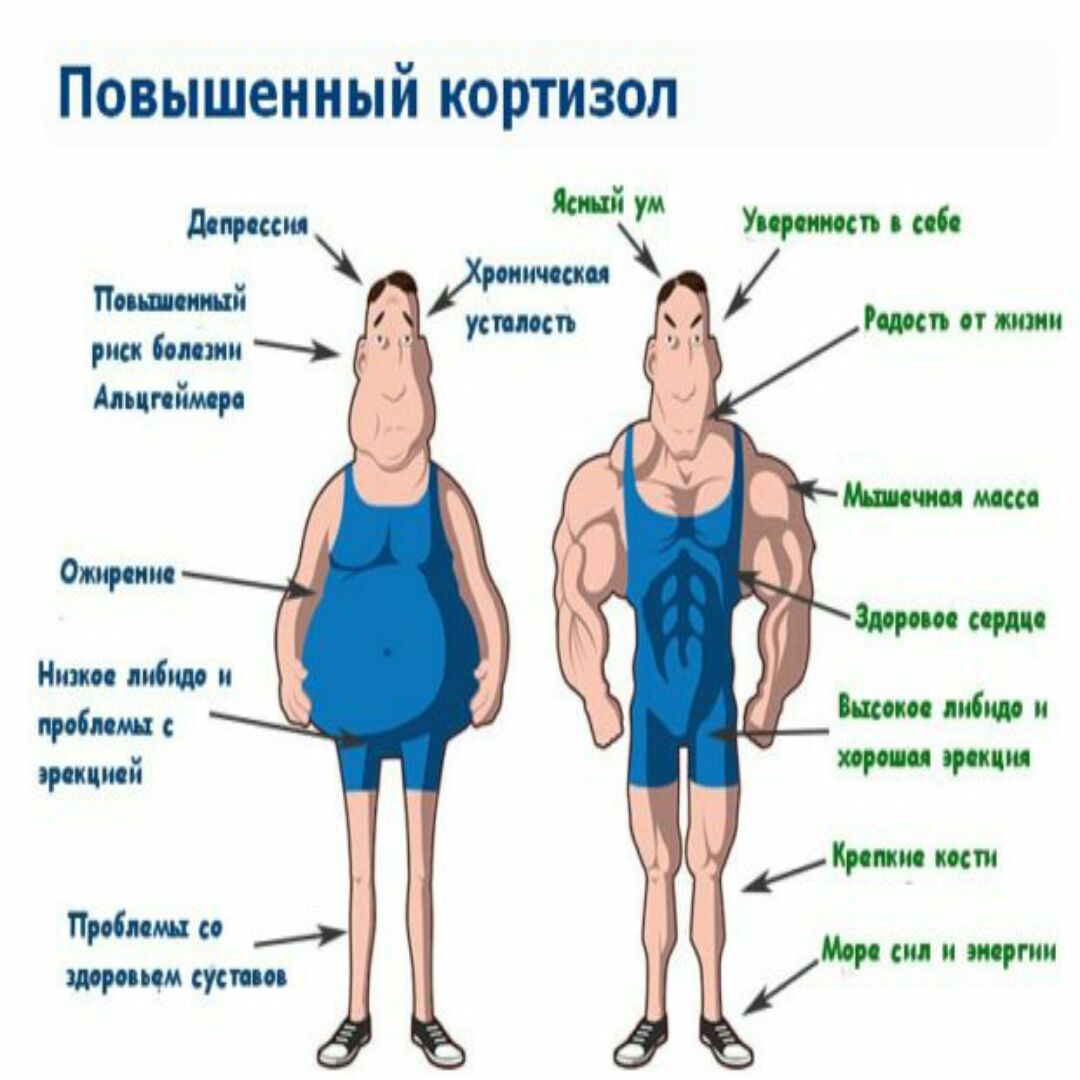 Мы вам перезвоним!
Мы вам перезвоним!
Телефон*
Ваше ФИО*
Нажимая на кнопку вы подтверждаете ознакомление с условиями обработки персональных данных и соглашаетесь с ними
* — поля, отмеченные звездочкой обязательны для заполнения
Эта форма защищена reCAPTCHA и Google, отправляя данные вы соглашаетесь с Политикой конфиденциальности и Условиями использования.Раздел лицензии Правовая информация
Физиология, кортизол — StatPearls — Книжная полка NCBI
Лорен Тау; Джаяшри Ганди; Сандип Шарма.
Информация об авторе и организацияхПоследнее обновление: 29 августа 2022 г.
Введение
Хотя кортизол широко известен как гормон стресса, он по-разному влияет на различные функции организма. Это основной глюкокортикоид, высвобождаемый из пучковой зоны коры надпочечников. Ось гипоталамус-гипофиз-надпочечники регулирует как выработку, так и секрецию кортизола.
Сотовый уровень
Кортизол, стероидный гормон, синтезируется из холестерина. Синтезируется в пучковой зоне коры надпочечников. Адренокортикотропный гормон (АКТГ), высвобождаемый передней долей гипофиза, увеличивает количество рецепторов ЛПНП и повышает активность холестериндесмолазы, которая превращает холестерин в прегненолон и является лимитирующей стадией синтеза кортизола.[1] Большинство глюкокортикоидов циркулируют в неактивной форме, связанной либо с кортикостероид-связывающим глобулином (КСГ), либо с альбумином.[2] Неактивная форма превращается в активную под действием 11-бета-гидроксистероиддегидрогеназы 1 (11-бета-HSD1) в большинстве тканей, в то время как 11-бета-HSD2 инактивирует кортизол обратно в кортизон в почках и поджелудочной железе.[2]
Вовлеченные системы органов
Глюкокортикоидные рецепторы присутствуют почти во всех тканях организма. Таким образом, кортизол способен воздействовать почти на все системы органов: 0002 Респираторная
Таким образом, кортизол способен воздействовать почти на все системы органов: 0002 Респираторная
Репродуктивная
Скелетно-мышечная
Покровная
Функция
Кортизол выполняет множество функций в организме человека, например, опосредует реакцию на стресс, регулирует обмен веществ, воспалительную реакцию и иммунную функцию.[4]
Иммунный ответ
Глюкокортикоиды оказывают ряд действий на иммунную систему. Например, они индуцируют апоптоз провоспалительных Т-клеток, подавляют выработку антител В-клетками и уменьшают миграцию нейтрофилов во время воспаления.[3]
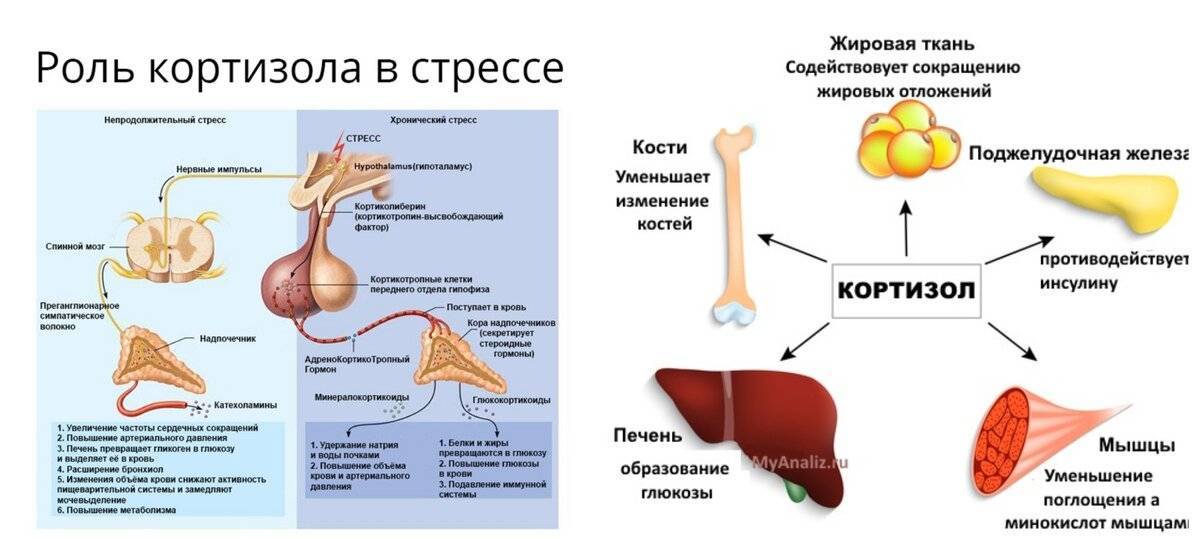
Реакция на стресс
Организм человека постоянно реагирует на внутренние и внешние факторы стресса. Организм обрабатывает стрессовую информацию и вызывает реакцию в зависимости от степени угрозы. Вегетативная нервная система организма делится на симпатическую нервную систему (СНС) и парасимпатическую нервную систему (ПНС).
Глюкозный и белковый гомеостаз
Уровень глюкозы в крови управляет ключевыми системными и внутриклеточными путями. Присутствие глюкокортикоидов, таких как кортизол, увеличивает доступ глюкозы крови к мозгу. Кортизол действует на печень, мышцы, жировую ткань и поджелудочную железу. В печени высокие уровни кортизола увеличивают глюконеогенез и снижают синтез гликогена.[7] Глюконеогенез представляет собой метаболический путь, который приводит к образованию глюкозы из глюкогенных аминокислот, лактата или глицерол-3-фосфата, содержащихся в триглицеридах. Глюконеогенез реверсирует гликолиз, цитоплазматический путь, используемый для превращения глюкозы в молекулы пирувата. Этот путь используется для высвобождения энергии посредством реакций фосфорилирования и окисления на уровне субстрата. В отличие от гликолиза, глюконеогенез становится активным, когда организм нуждается в энергии. Мышцы имеют собственный внутренний запас гликогена, что позволяет им быстро реагировать на изменения потребности в АТФ. В присутствии кортизола мышечные клетки снижают поглощение и потребление глюкозы и увеличивают расщепление белка; это обеспечивает глюконеогенез глюкогенными аминокислотами. В жировых тканях кортизол усиливает липолиз.
Кортизол действует на печень, мышцы, жировую ткань и поджелудочную железу. В печени высокие уровни кортизола увеличивают глюконеогенез и снижают синтез гликогена.[7] Глюконеогенез представляет собой метаболический путь, который приводит к образованию глюкозы из глюкогенных аминокислот, лактата или глицерол-3-фосфата, содержащихся в триглицеридах. Глюконеогенез реверсирует гликолиз, цитоплазматический путь, используемый для превращения глюкозы в молекулы пирувата. Этот путь используется для высвобождения энергии посредством реакций фосфорилирования и окисления на уровне субстрата. В отличие от гликолиза, глюконеогенез становится активным, когда организм нуждается в энергии. Мышцы имеют собственный внутренний запас гликогена, что позволяет им быстро реагировать на изменения потребности в АТФ. В присутствии кортизола мышечные клетки снижают поглощение и потребление глюкозы и увеличивают расщепление белка; это обеспечивает глюконеогенез глюкогенными аминокислотами. В жировых тканях кортизол усиливает липолиз.
Механизм
Высвобождение кортизола находится под контролем оси гипоталамус-гипофиз-надпочечники (ГГН). Кортикотропин-рилизинг-гормон (CRH) высвобождается паравентрикулярным ядром (PVN) гипоталамуса.[2] Затем он действует на переднюю долю гипофиза, высвобождая адренокортикотропный гормон (АКТГ), который впоследствии действует на кору надпочечников. В петле отрицательной обратной связи достаточное количество кортизола ингибирует высвобождение как АКТГ, так и КРГ. Ось HPA следует циркадному ритму. Таким образом, уровень кортизола будет высоким утром и низким ночью [2].
В петле отрицательной обратной связи достаточное количество кортизола ингибирует высвобождение как АКТГ, так и КРГ. Ось HPA следует циркадному ритму. Таким образом, уровень кортизола будет высоким утром и низким ночью [2].
Стероидные гормоны, такие как кортизол, являются первичными мессенджерами. Они могут проникать через цитоплазматическую мембрану благодаря своим жирорастворимым свойствам. Клеточные мембраны состоят из двойных слоев фосфолипидов; они предотвращают прохождение жиронерастворимых молекул. Как только кортизол проходит через клеточную мембрану и проникает в клетку, он связывается со специфическими рецепторами в цитоплазме. В отсутствие кортизола глюкокортикоидный рецептор связывается с белком-шапероном Hsp90 в цитозоле. Связывание кортизола с глюкокортикоидным рецептором диссоциирует Hsp9.0. Затем комплекс кортизол-рецептор проникает в ядро клетки и влияет на транскрипцию генов.
Связанные тесты
Считается, что уровни кортизола в слюне коррелируют с уровнями свободного кортизола в плазме и сыворотке. [6] Ночное измерение кортизола в слюне используется в качестве начального диагностического теста на синдром Кушинга, синдром избытка глюкокортикоидов.[6] Поскольку уровни кортизола должны быть высокими по утрам, одним из первоначальных диагностических тестов на болезнь Аддисона является проверка уровня кортизола в сыворотке рано утром.[9]]
[6] Ночное измерение кортизола в слюне используется в качестве начального диагностического теста на синдром Кушинга, синдром избытка глюкокортикоидов.[6] Поскольку уровни кортизола должны быть высокими по утрам, одним из первоначальных диагностических тестов на болезнь Аддисона является проверка уровня кортизола в сыворотке рано утром.[9]]
Клиническое значение
Уровень кортизола в организме постоянно контролируется для поддержания гомеостаза. Нерегулируемые уровни могут быть вредными.
Гиперкортицизм
Синдром Кушинга возникает, когда организм человека подвергается воздействию высоких уровней кортизола в течение длительного периода времени. Различные этиологии синдрома Кушинга можно разделить на АКТГ-зависимые и АКТГ-независимые. При АКТГ-зависимых подтипах наблюдается избыток АКТГ либо из-за опухоли гипофиза, либо из-за эктопического источника, такого как нейроэндокринная опухоль.[10] В обоих случаях перепроизводство АКТГ стимулирует надпочечники к выработке избыточного кортизола. В АКТГ-независимых подтипах есть эндогенная этиология и экзогенная этиология. Эндогенная причина обычно связана с опухолью надпочечников, что приводит к избыточной выработке кортизола. Экзогенная причина связана с чрезмерным использованием пероральных или инъекционных кортикостероидов. Пероральные кортикостероиды, такие как преднизолон, увеличивают количество кортизола в организме. Их назначают для облегчения симптомов, связанных с хроническими воспалительными заболеваниями, такими как системная эритематозная волчанка (СКВ) и ревматоидный артрит. Симптомы синдрома Кушинга зависят от того, насколько повышен уровень кортизола. Общие признаки и симптомы избытка кортизола включают увеличение веса (особенно на лице и животе), жировые отложения между лопатками, диабет, гипертонию, гирсутизм у женщин, слабость проксимальных мышц и остеопороз.[11] Лечение синдрома Кушинга зависит от причины. Чаще всего лечение проводится с помощью хирургического вмешательства. Однако антагонисты глюкокортикоидных рецепторов также могут применяться при наличии противопоказаний к хирургическому вмешательству.
В АКТГ-независимых подтипах есть эндогенная этиология и экзогенная этиология. Эндогенная причина обычно связана с опухолью надпочечников, что приводит к избыточной выработке кортизола. Экзогенная причина связана с чрезмерным использованием пероральных или инъекционных кортикостероидов. Пероральные кортикостероиды, такие как преднизолон, увеличивают количество кортизола в организме. Их назначают для облегчения симптомов, связанных с хроническими воспалительными заболеваниями, такими как системная эритематозная волчанка (СКВ) и ревматоидный артрит. Симптомы синдрома Кушинга зависят от того, насколько повышен уровень кортизола. Общие признаки и симптомы избытка кортизола включают увеличение веса (особенно на лице и животе), жировые отложения между лопатками, диабет, гипертонию, гирсутизм у женщин, слабость проксимальных мышц и остеопороз.[11] Лечение синдрома Кушинга зависит от причины. Чаще всего лечение проводится с помощью хирургического вмешательства. Однако антагонисты глюкокортикоидных рецепторов также могут применяться при наличии противопоказаний к хирургическому вмешательству.
Гипокортицизм
Первичная надпочечниковая недостаточность, также известная как болезнь Аддисона, чаще всего вызывается аутоиммунным адреналитом.[9] Другие причины включают злокачественное новообразование, инфекцию или кровоизлияние в надпочечники. Аутоиммунный адреналит возникает в результате того, что организм атакует кору надпочечников.[12] Вторичная недостаточность надпочечников связана с недостаточной продукцией АКТГ передней долей гипофиза. Это может быть вызвано заболеванием гипофиза, но наиболее частая причина связана с подавлением оси HPA из-за хронического приема экзогенных глюкокортикоидов. Третичная надпочечниковая недостаточность возникает из-за отсутствия высвобождения КРГ из гипоталамуса. Симптомы надпочечниковой недостаточности включают утомляемость, потерю веса, гипотонию и гиперпигментацию кожи.[14] Поскольку альдостерона также будет недостаточно, лабораторные результаты покажут гиперкалиемию. Заместительная терапия глюкокортикоидами, например гидрокортизоном, необходима для лечения симптомов гипокортицизма. Важно помнить об увеличении дозировки при острых стрессовых факторах, таких как болезнь или хирургическое вмешательство, чтобы избежать надпочечникового кризиса.[14]
Важно помнить об увеличении дозировки при острых стрессовых факторах, таких как болезнь или хирургическое вмешательство, чтобы избежать надпочечникового кризиса.[14]
Контрольные вопросы
Доступ к бесплатным вопросам с несколькими вариантами ответов по этой теме.
Комментарий к этой статье.
Ссылки
- 1.
Ангелуси А., Маргиорис А.Н., Цацанис С. Действие АКТГ на надпочечники. Пришли: Фейнгольд К.Р., Анавальт Б., Блэкман М.Р., Бойс А., Хрусос Г., Корпас Э., де Гердер В.В., Дхатария К., Дунган К., Хофланд Дж., Калра С., Кальцас Г., Капур Н., Кох К., Копп П., Корбонитс М. , Kovacs CS, Kuohung W, Laferrere B, Levy M, McGee EA, McLachlan R, New M, Purnell J, Sahay R, Shah AS, Singer F, Sperling MA, Stratakis CA, Trance DL, Wilson DP, редакторы. Эндотекст [Интернет]. MDText.com, Inc.; Южный Дартмут (Массачусетс): 13 июня 2020 г. [PubMed: 25905342]
- 2.
Рамамурти С., Сидловски Дж.
 А. Кортикостероиды: механизмы действия в норме и при заболевании. Реум Дис Клин Норт Ам. 2016 Feb;42(1):15-31, vii. [Бесплатная статья PMC: PMC4662771] [PubMed: 26611548]
А. Кортикостероиды: механизмы действия в норме и при заболевании. Реум Дис Клин Норт Ам. 2016 Feb;42(1):15-31, vii. [Бесплатная статья PMC: PMC4662771] [PubMed: 26611548]- 3.
Kadmiel M, Cidlowski JA. Сигнализация глюкокортикоидных рецепторов в норме и при патологии. Trends Pharmacol Sci. 2013 сен; 34 (9): 518-30. [Бесплатная статья PMC: PMC3951203] [PubMed: 23953592]
- 4.
Oakley RH, Cidlowski JA. Биология глюкокортикоидного рецептора: новые сигнальные механизмы в норме и при патологии. J Аллергия Клин Иммунол. 2013 ноябрь; 132(5):1033-44. [Бесплатная статья PMC: PMC4084612] [PubMed: 24084075]
- 5.
Хакамата Ю., Коми С., Моригути Ю., Изава С., Мотомура Ю., Сато Э., Мизуками С., Ким Ю., Ханакава Т., Иноуэ Ю., Тагая Х. Функциональная связность миндалевидного тела влияет на суточную концентрацию кортизола : предполагаемая связь с тревогой. Научный представитель 2017 г. 16 августа; 7 (1): 8313. [Бесплатная статья PMC: PMC5559590] [PubMed: 28814810]
- 6.

Lee DY, Kim E, Choi MH. Технические и клинические аспекты кортизола как биохимического маркера хронического стресса. Отчет BMB, апрель 2015 г.; 48 (4): 209-16. [Бесплатная статья PMC: PMC4436856] [PubMed: 25560699]
- 7.
Kuo T, McQueen A, Chen TC, Wang JC. Регуляция гомеостаза глюкозы глюкокортикоидами. Adv Exp Med Biol. 2015;872:99-126. [Бесплатная статья PMC: PMC6185996] [PubMed: 26215992]
- 8.
Exton JH. Регуляция глюконеогенеза глюкокортикоидами. Моногр Эндокринол. 1979; 12:535-46. [PubMed: 386091]
- 9.
Michels A, Michels N. Болезнь Аддисона: раннее выявление и принципы лечения. Ам семейный врач. 2014 01 апреля; 89(7): 563-8. [PubMed: 24695602]
- 10.
Рафф Х., Кэрролл Т. Синдром Кушинга: от физиологических принципов к диагностике и клиническому лечению. Дж. Физиол. 2015 01 февраля; 593 (3): 493-506. [Бесплатная статья PMC: PMC4324701] [PubMed: 25480800]
- 11.

Лила А.Р., Саратхи В., Джагтап В.С., Бандгар Т., Менон П., Шах Н.С. Синдром Кушинга: поэтапный подход к диагностике. Индийский J Endocrinol Metab. 2011 Октябрь; 15 Дополнение 4 (Приложение 4): S317-21. [Бесплатная статья PMC: PMC3230095] [PubMed: 22145134]
- 12.
Ниари Н., Ниман Л. Надпочечниковая недостаточность: этиология, диагностика и лечение. Curr Opin Endocrinol Diabetes Obes. 2010 июнь;17(3):217-23. [Бесплатная статья PMC: PMC2928659] [PubMed: 20375886]
- 13.
Войцик М., Русала А., Янус Д., Старжик Дж. Б. Вторичная надпочечниковая недостаточность вследствие внутрисуставных инъекций глюкокортикоидов. Индийский педиатр. 2019 15 марта; 56 (3): 242-243. [PubMed: 30954999]
- 14.
Александраки К.И., Санпавитаякул К., Гроссман А. Надпочечниковая недостаточность. Пришли: Фейнгольд К.Р., Анавальт Б., Блэкман М.Р., Бойс А., Хрусос Г., Корпас Э., де Гердер В.В., Дхатария К., Дунган К., Хофланд Дж.
 , Калра С., Кальцас Г., Капур Н., Кох К., Копп П., Корбонитс М. , Kovacs CS, Kuohung W, Laferrere B, Levy M, McGee EA, McLachlan R, New M, Purnell J, Sahay R, Shah AS, Singer F, Sperling MA, Stratakis CA, Trance DL, Wilson DP, редакторы. Эндотекст [Интернет]. MDText.com, Inc.; Южный Дартмут (Массачусетс): 7 ноября 2022 г. [PubMed: 25905309]
, Калра С., Кальцас Г., Капур Н., Кох К., Копп П., Корбонитс М. , Kovacs CS, Kuohung W, Laferrere B, Levy M, McGee EA, McLachlan R, New M, Purnell J, Sahay R, Shah AS, Singer F, Sperling MA, Stratakis CA, Trance DL, Wilson DP, редакторы. Эндотекст [Интернет]. MDText.com, Inc.; Южный Дартмут (Массачусетс): 7 ноября 2022 г. [PubMed: 25905309]
Раскрытие информации: Лорен Тау заявляет об отсутствии соответствующих финансовых отношений с неправомочными компаниями.
Раскрытие информации: Джаяшри Ганди заявляет об отсутствии соответствующих финансовых отношений с неправомочными компаниями.
Раскрытие информации: Сандип Шарма заявляет об отсутствии соответствующих финансовых отношений с неправомочными компаниями.
Физиология, кортизол — StatPearls — Книжная полка NCBI
Лорен Тау; Джаяшри Ганди; Сандип Шарма.
Информация об авторе и организациях Последнее обновление: 29 августа 2022 г.
Введение
Хотя кортизол широко известен как гормон стресса, он по-разному влияет на различные функции организма. Это основной глюкокортикоид, высвобождаемый из пучковой зоны коры надпочечников. Ось гипоталамус-гипофиз-надпочечники регулирует как выработку, так и секрецию кортизола. Потеря регуляции может привести к нарушениям избытка кортизола, таким как синдром Кушинга, или корковой недостаточности, такой как болезнь Аддисона.
Сотовый уровень
Кортизол, стероидный гормон, синтезируется из холестерина. Синтезируется в пучковой зоне коры надпочечников. Адренокортикотропный гормон (АКТГ), высвобождаемый передней долей гипофиза, увеличивает количество рецепторов ЛПНП и повышает активность холестериндесмолазы, которая превращает холестерин в прегненолон и является лимитирующей стадией синтеза кортизола.[1] Большинство глюкокортикоидов циркулируют в неактивной форме, связанной либо с кортикостероид-связывающим глобулином (КСГ), либо с альбумином.[2] Неактивная форма превращается в активную под действием 11-бета-гидроксистероиддегидрогеназы 1 (11-бета-HSD1) в большинстве тканей, в то время как 11-бета-HSD2 инактивирует кортизол обратно в кортизон в почках и поджелудочной железе. [2]
[2]
Вовлеченные системы органов
Глюкокортикоидные рецепторы присутствуют почти во всех тканях организма. Таким образом, кортизол способен воздействовать почти на все системы органов: 0002 Респираторная
Репродуктивная
Скелетно-мышечная
Покровная
Функция
Кортизол выполняет множество функций в организме человека, например, опосредует реакцию на стресс, регулирует обмен веществ, воспалительную реакцию и иммунную функцию.[4]
Иммунный ответ
Глюкокортикоиды оказывают ряд действий на иммунную систему. Например, они индуцируют апоптоз провоспалительных Т-клеток, подавляют выработку антител В-клетками и уменьшают миграцию нейтрофилов во время воспаления.[3]
Реакция на стресс
Организм человека постоянно реагирует на внутренние и внешние факторы стресса. Организм обрабатывает стрессовую информацию и вызывает реакцию в зависимости от степени угрозы. Вегетативная нервная система организма делится на симпатическую нервную систему (СНС) и парасимпатическую нервную систему (ПНС). Во время стресса активизируется СНС. СНС отвечает за реакцию «бей или беги», которая вызывает каскад гормональных и физиологических реакций. Миндалевидное тело отвечает за обработку страха, возбуждения и эмоциональных стимулов, чтобы определить соответствующую реакцию. При необходимости миндалевидное тело посылает сигнал стресса в гипоталамус.[5] Затем гипоталамус активирует СНС, а надпочечники выделяют большое количество катехоламинов, таких как адреналин. Это приводит к таким эффектам, как увеличение частоты сердечных сокращений и частоты дыхания. Поскольку тело продолжает воспринимать раздражители как угрозу, гипоталамус активирует ось HPA. Кортизол высвобождается из коры надпочечников и позволяет организму оставаться в состоянии повышенной готовности. В частности, катаболические механизмы кортизола обеспечивают организм энергией.[6]
Вегетативная нервная система организма делится на симпатическую нервную систему (СНС) и парасимпатическую нервную систему (ПНС). Во время стресса активизируется СНС. СНС отвечает за реакцию «бей или беги», которая вызывает каскад гормональных и физиологических реакций. Миндалевидное тело отвечает за обработку страха, возбуждения и эмоциональных стимулов, чтобы определить соответствующую реакцию. При необходимости миндалевидное тело посылает сигнал стресса в гипоталамус.[5] Затем гипоталамус активирует СНС, а надпочечники выделяют большое количество катехоламинов, таких как адреналин. Это приводит к таким эффектам, как увеличение частоты сердечных сокращений и частоты дыхания. Поскольку тело продолжает воспринимать раздражители как угрозу, гипоталамус активирует ось HPA. Кортизол высвобождается из коры надпочечников и позволяет организму оставаться в состоянии повышенной готовности. В частности, катаболические механизмы кортизола обеспечивают организм энергией.[6]
Глюкозный и белковый гомеостаз
Уровень глюкозы в крови управляет ключевыми системными и внутриклеточными путями. Присутствие глюкокортикоидов, таких как кортизол, увеличивает доступ глюкозы крови к мозгу. Кортизол действует на печень, мышцы, жировую ткань и поджелудочную железу. В печени высокие уровни кортизола увеличивают глюконеогенез и снижают синтез гликогена.[7] Глюконеогенез представляет собой метаболический путь, который приводит к образованию глюкозы из глюкогенных аминокислот, лактата или глицерол-3-фосфата, содержащихся в триглицеридах. Глюконеогенез реверсирует гликолиз, цитоплазматический путь, используемый для превращения глюкозы в молекулы пирувата. Этот путь используется для высвобождения энергии посредством реакций фосфорилирования и окисления на уровне субстрата. В отличие от гликолиза, глюконеогенез становится активным, когда организм нуждается в энергии. Мышцы имеют собственный внутренний запас гликогена, что позволяет им быстро реагировать на изменения потребности в АТФ. В присутствии кортизола мышечные клетки снижают поглощение и потребление глюкозы и увеличивают расщепление белка; это обеспечивает глюконеогенез глюкогенными аминокислотами.
Присутствие глюкокортикоидов, таких как кортизол, увеличивает доступ глюкозы крови к мозгу. Кортизол действует на печень, мышцы, жировую ткань и поджелудочную железу. В печени высокие уровни кортизола увеличивают глюконеогенез и снижают синтез гликогена.[7] Глюконеогенез представляет собой метаболический путь, который приводит к образованию глюкозы из глюкогенных аминокислот, лактата или глицерол-3-фосфата, содержащихся в триглицеридах. Глюконеогенез реверсирует гликолиз, цитоплазматический путь, используемый для превращения глюкозы в молекулы пирувата. Этот путь используется для высвобождения энергии посредством реакций фосфорилирования и окисления на уровне субстрата. В отличие от гликолиза, глюконеогенез становится активным, когда организм нуждается в энергии. Мышцы имеют собственный внутренний запас гликогена, что позволяет им быстро реагировать на изменения потребности в АТФ. В присутствии кортизола мышечные клетки снижают поглощение и потребление глюкозы и увеличивают расщепление белка; это обеспечивает глюконеогенез глюкогенными аминокислотами. В жировых тканях кортизол усиливает липолиз. Липолиз — это катаболический процесс, в результате которого высвобождается глицерин и свободные жирные кислоты. Эти свободные жирные кислоты могут использоваться для окисления B и в качестве источника энергии для других клеток, поскольку они продолжают производить глюкозу. Наконец, кортизол действует на поджелудочную железу, снижая уровень инсулина и увеличивая уровень глюкагона. Глюкагон представляет собой пептидный гормон, секретируемый альфа-клетками поджелудочной железы для усиления гликогенолиза в печени, глюконеогенеза в печени, кетогенеза в печени, липолиза, а также для снижения липогенеза. Кортизол усиливает активность глюкагона, адреналина и других катехоламинов.
В жировых тканях кортизол усиливает липолиз. Липолиз — это катаболический процесс, в результате которого высвобождается глицерин и свободные жирные кислоты. Эти свободные жирные кислоты могут использоваться для окисления B и в качестве источника энергии для других клеток, поскольку они продолжают производить глюкозу. Наконец, кортизол действует на поджелудочную железу, снижая уровень инсулина и увеличивая уровень глюкагона. Глюкагон представляет собой пептидный гормон, секретируемый альфа-клетками поджелудочной железы для усиления гликогенолиза в печени, глюконеогенеза в печени, кетогенеза в печени, липолиза, а также для снижения липогенеза. Кортизол усиливает активность глюкагона, адреналина и других катехоламинов.
Механизм
Высвобождение кортизола находится под контролем оси гипоталамус-гипофиз-надпочечники (ГГН). Кортикотропин-рилизинг-гормон (CRH) высвобождается паравентрикулярным ядром (PVN) гипоталамуса.[2] Затем он действует на переднюю долю гипофиза, высвобождая адренокортикотропный гормон (АКТГ), который впоследствии действует на кору надпочечников. В петле отрицательной обратной связи достаточное количество кортизола ингибирует высвобождение как АКТГ, так и КРГ. Ось HPA следует циркадному ритму. Таким образом, уровень кортизола будет высоким утром и низким ночью [2].
В петле отрицательной обратной связи достаточное количество кортизола ингибирует высвобождение как АКТГ, так и КРГ. Ось HPA следует циркадному ритму. Таким образом, уровень кортизола будет высоким утром и низким ночью [2].
Стероидные гормоны, такие как кортизол, являются первичными мессенджерами. Они могут проникать через цитоплазматическую мембрану благодаря своим жирорастворимым свойствам. Клеточные мембраны состоят из двойных слоев фосфолипидов; они предотвращают прохождение жиронерастворимых молекул. Как только кортизол проходит через клеточную мембрану и проникает в клетку, он связывается со специфическими рецепторами в цитоплазме. В отсутствие кортизола глюкокортикоидный рецептор связывается с белком-шапероном Hsp90 в цитозоле. Связывание кортизола с глюкокортикоидным рецептором диссоциирует Hsp9.0. Затем комплекс кортизол-рецептор проникает в ядро клетки и влияет на транскрипцию генов.
Связанные тесты
Считается, что уровни кортизола в слюне коррелируют с уровнями свободного кортизола в плазме и сыворотке.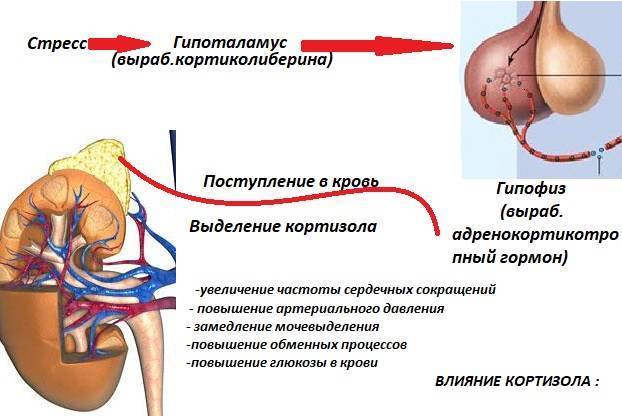 [6] Ночное измерение кортизола в слюне используется в качестве начального диагностического теста на синдром Кушинга, синдром избытка глюкокортикоидов.[6] Поскольку уровни кортизола должны быть высокими по утрам, одним из первоначальных диагностических тестов на болезнь Аддисона является проверка уровня кортизола в сыворотке рано утром.[9]]
[6] Ночное измерение кортизола в слюне используется в качестве начального диагностического теста на синдром Кушинга, синдром избытка глюкокортикоидов.[6] Поскольку уровни кортизола должны быть высокими по утрам, одним из первоначальных диагностических тестов на болезнь Аддисона является проверка уровня кортизола в сыворотке рано утром.[9]]
Клиническое значение
Уровень кортизола в организме постоянно контролируется для поддержания гомеостаза. Нерегулируемые уровни могут быть вредными.
Гиперкортицизм
Синдром Кушинга возникает, когда организм человека подвергается воздействию высоких уровней кортизола в течение длительного периода времени. Различные этиологии синдрома Кушинга можно разделить на АКТГ-зависимые и АКТГ-независимые. При АКТГ-зависимых подтипах наблюдается избыток АКТГ либо из-за опухоли гипофиза, либо из-за эктопического источника, такого как нейроэндокринная опухоль.[10] В обоих случаях перепроизводство АКТГ стимулирует надпочечники к выработке избыточного кортизола.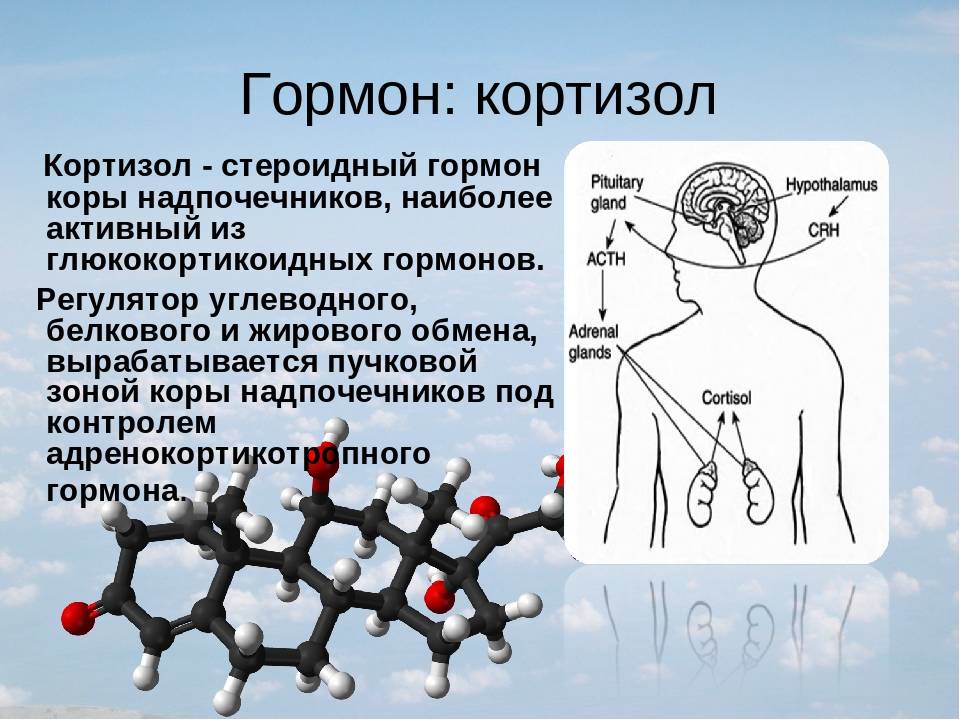 В АКТГ-независимых подтипах есть эндогенная этиология и экзогенная этиология. Эндогенная причина обычно связана с опухолью надпочечников, что приводит к избыточной выработке кортизола. Экзогенная причина связана с чрезмерным использованием пероральных или инъекционных кортикостероидов. Пероральные кортикостероиды, такие как преднизолон, увеличивают количество кортизола в организме. Их назначают для облегчения симптомов, связанных с хроническими воспалительными заболеваниями, такими как системная эритематозная волчанка (СКВ) и ревматоидный артрит. Симптомы синдрома Кушинга зависят от того, насколько повышен уровень кортизола. Общие признаки и симптомы избытка кортизола включают увеличение веса (особенно на лице и животе), жировые отложения между лопатками, диабет, гипертонию, гирсутизм у женщин, слабость проксимальных мышц и остеопороз.[11] Лечение синдрома Кушинга зависит от причины. Чаще всего лечение проводится с помощью хирургического вмешательства. Однако антагонисты глюкокортикоидных рецепторов также могут применяться при наличии противопоказаний к хирургическому вмешательству.
В АКТГ-независимых подтипах есть эндогенная этиология и экзогенная этиология. Эндогенная причина обычно связана с опухолью надпочечников, что приводит к избыточной выработке кортизола. Экзогенная причина связана с чрезмерным использованием пероральных или инъекционных кортикостероидов. Пероральные кортикостероиды, такие как преднизолон, увеличивают количество кортизола в организме. Их назначают для облегчения симптомов, связанных с хроническими воспалительными заболеваниями, такими как системная эритематозная волчанка (СКВ) и ревматоидный артрит. Симптомы синдрома Кушинга зависят от того, насколько повышен уровень кортизола. Общие признаки и симптомы избытка кортизола включают увеличение веса (особенно на лице и животе), жировые отложения между лопатками, диабет, гипертонию, гирсутизм у женщин, слабость проксимальных мышц и остеопороз.[11] Лечение синдрома Кушинга зависит от причины. Чаще всего лечение проводится с помощью хирургического вмешательства. Однако антагонисты глюкокортикоидных рецепторов также могут применяться при наличии противопоказаний к хирургическому вмешательству.
Гипокортицизм
Первичная надпочечниковая недостаточность, также известная как болезнь Аддисона, чаще всего вызывается аутоиммунным адреналитом.[9] Другие причины включают злокачественное новообразование, инфекцию или кровоизлияние в надпочечники. Аутоиммунный адреналит возникает в результате того, что организм атакует кору надпочечников.[12] Вторичная недостаточность надпочечников связана с недостаточной продукцией АКТГ передней долей гипофиза. Это может быть вызвано заболеванием гипофиза, но наиболее частая причина связана с подавлением оси HPA из-за хронического приема экзогенных глюкокортикоидов. Третичная надпочечниковая недостаточность возникает из-за отсутствия высвобождения КРГ из гипоталамуса. Симптомы надпочечниковой недостаточности включают утомляемость, потерю веса, гипотонию и гиперпигментацию кожи.[14] Поскольку альдостерона также будет недостаточно, лабораторные результаты покажут гиперкалиемию. Заместительная терапия глюкокортикоидами, например гидрокортизоном, необходима для лечения симптомов гипокортицизма. Важно помнить об увеличении дозировки при острых стрессовых факторах, таких как болезнь или хирургическое вмешательство, чтобы избежать надпочечникового кризиса.[14]
Важно помнить об увеличении дозировки при острых стрессовых факторах, таких как болезнь или хирургическое вмешательство, чтобы избежать надпочечникового кризиса.[14]
Контрольные вопросы
Доступ к бесплатным вопросам с несколькими вариантами ответов по этой теме.
Комментарий к этой статье.
Ссылки
- 1.
Ангелуси А., Маргиорис А.Н., Цацанис С. Действие АКТГ на надпочечники. Пришли: Фейнгольд К.Р., Анавальт Б., Блэкман М.Р., Бойс А., Хрусос Г., Корпас Э., де Гердер В.В., Дхатария К., Дунган К., Хофланд Дж., Калра С., Кальцас Г., Капур Н., Кох К., Копп П., Корбонитс М. , Kovacs CS, Kuohung W, Laferrere B, Levy M, McGee EA, McLachlan R, New M, Purnell J, Sahay R, Shah AS, Singer F, Sperling MA, Stratakis CA, Trance DL, Wilson DP, редакторы. Эндотекст [Интернет]. MDText.com, Inc.; Южный Дартмут (Массачусетс): 13 июня 2020 г. [PubMed: 25905342]
- 2.
Рамамурти С., Сидловски Дж.
 А. Кортикостероиды: механизмы действия в норме и при заболевании. Реум Дис Клин Норт Ам. 2016 Feb;42(1):15-31, vii. [Бесплатная статья PMC: PMC4662771] [PubMed: 26611548]
А. Кортикостероиды: механизмы действия в норме и при заболевании. Реум Дис Клин Норт Ам. 2016 Feb;42(1):15-31, vii. [Бесплатная статья PMC: PMC4662771] [PubMed: 26611548]- 3.
Kadmiel M, Cidlowski JA. Сигнализация глюкокортикоидных рецепторов в норме и при патологии. Trends Pharmacol Sci. 2013 сен; 34 (9): 518-30. [Бесплатная статья PMC: PMC3951203] [PubMed: 23953592]
- 4.
Oakley RH, Cidlowski JA. Биология глюкокортикоидного рецептора: новые сигнальные механизмы в норме и при патологии. J Аллергия Клин Иммунол. 2013 ноябрь; 132(5):1033-44. [Бесплатная статья PMC: PMC4084612] [PubMed: 24084075]
- 5.
Хакамата Ю., Коми С., Моригути Ю., Изава С., Мотомура Ю., Сато Э., Мизуками С., Ким Ю., Ханакава Т., Иноуэ Ю., Тагая Х. Функциональная связность миндалевидного тела влияет на суточную концентрацию кортизола : предполагаемая связь с тревогой. Научный представитель 2017 г. 16 августа; 7 (1): 8313. [Бесплатная статья PMC: PMC5559590] [PubMed: 28814810]
- 6.

Lee DY, Kim E, Choi MH. Технические и клинические аспекты кортизола как биохимического маркера хронического стресса. Отчет BMB, апрель 2015 г.; 48 (4): 209-16. [Бесплатная статья PMC: PMC4436856] [PubMed: 25560699]
- 7.
Kuo T, McQueen A, Chen TC, Wang JC. Регуляция гомеостаза глюкозы глюкокортикоидами. Adv Exp Med Biol. 2015;872:99-126. [Бесплатная статья PMC: PMC6185996] [PubMed: 26215992]
- 8.
Exton JH. Регуляция глюконеогенеза глюкокортикоидами. Моногр Эндокринол. 1979; 12:535-46. [PubMed: 386091]
- 9.
Michels A, Michels N. Болезнь Аддисона: раннее выявление и принципы лечения. Ам семейный врач. 2014 01 апреля; 89(7): 563-8. [PubMed: 24695602]
- 10.
Рафф Х., Кэрролл Т. Синдром Кушинга: от физиологических принципов к диагностике и клиническому лечению. Дж. Физиол. 2015 01 февраля; 593 (3): 493-506. [Бесплатная статья PMC: PMC4324701] [PubMed: 25480800]
- 11.

Лила А.Р., Саратхи В., Джагтап В.С., Бандгар Т., Менон П., Шах Н.С. Синдром Кушинга: поэтапный подход к диагностике. Индийский J Endocrinol Metab. 2011 Октябрь; 15 Дополнение 4 (Приложение 4): S317-21. [Бесплатная статья PMC: PMC3230095] [PubMed: 22145134]
- 12.
Ниари Н., Ниман Л. Надпочечниковая недостаточность: этиология, диагностика и лечение. Curr Opin Endocrinol Diabetes Obes. 2010 июнь;17(3):217-23. [Бесплатная статья PMC: PMC2928659] [PubMed: 20375886]
- 13.
Войцик М., Русала А., Янус Д., Старжик Дж. Б. Вторичная надпочечниковая недостаточность вследствие внутрисуставных инъекций глюкокортикоидов. Индийский педиатр. 2019 15 марта; 56 (3): 242-243. [PubMed: 30954999]
- 14.
Александраки К.И., Санпавитаякул К., Гроссман А. Надпочечниковая недостаточность. Пришли: Фейнгольд К.Р., Анавальт Б., Блэкман М.Р., Бойс А., Хрусос Г., Корпас Э., де Гердер В.В., Дхатария К., Дунган К., Хофланд Дж.


