Биохимия мочи: сдать анализ по доступной цене
Фосфор считается одним из базовых микроэлементов человеческого организма. Он необходим для формирования молекул АТФ, обеспечивающих энергией все процессы, синтеза кислот ДНК и РНК, образования клеточных мембран и костной ткани.
Где можно сдать:В клинике
На дому
МатериалМоча
Фосфор является одним из базовых микроэлементов. Он является компонентом клеточных мембран (в составе фосфолипидов), костной ткани, ДНК и РНК, а также молекулы АТФ, которая является основным источником энергии в организме.
Срок выполнения1-2 дня
Где можно сдать:В клинике
На дому
МатериалМоча
С-пептид – это вещество, являющееся побочным продуктом синтеза инсулина. Этот белок выступает в роли связующего звена между альфа- и бета-пептидными цепями, которые образуют молекулу проинсулина. Это неактивный предшественник гормона.
Срок выполнения1-2 дня
Где можно сдать:В клинике
На дому
МатериалМоча
Ежедневно почки человека фильтруют сотни литров крови. Сначала жидкость вместе с растворенными в ней веществами проходит через нефроны (структурные элементы почки) с образованием первичной мочи.
Сначала жидкость вместе с растворенными в ней веществами проходит через нефроны (структурные элементы почки) с образованием первичной мочи.
1-2 дня
Где можно сдать:В клинике
На дому
МатериалМоча
Осмолярность мочи – это концентрация всех растворенных в ней веществ. В отличие от удельного веса, она зависит только от числа частиц, тогда как плотность определяется не только количеством, но и особенностями строения примесей.
Срок выполнения1-2 дня
Где можно сдать:В клинике
На дому
МатериалМоча
Оксалаты – это производные щавелевой кислоты, которые образуются в организме при распаде глицина и аскорбиновой кислоты, а также поступают с пищей. В норме эти вещества выводятся с мочой.
Срок выполнения1-2 дня
Где можно сдать:В клинике
На дому
МатериалМоча
Общий белок – это один из базовых показателей работы почек. В норме крупные молекулы не проходят через почечный фильтр, а относительно небольшие соединения проходят в первичную мочу и затем подвергаются реабсорбции.
В норме крупные молекулы не проходят через почечный фильтр, а относительно небольшие соединения проходят в первичную мочу и затем подвергаются реабсорбции.
1-2 дня
Где можно сдать:В клинике
На дому
МатериалМоча
Мочевина – азотсодержащее химическое соединение, конечный продукт обмена белков в человеческом организме. Азот входит в состав любого белка. При распаде белковой молекулы азот высвобождается, образуя токсичное вещество – аммиак.
Срок выполнения1-2 дня
Где можно сдать:В клинике
На дому
МатериалМоча
Мочевина – конечный продукт белкового обмена, соединение, содержащее азот. Являясь обязательным компонентом любой аминокислоты и белковой молекулы человеческого организма, образует при их распаде свободный азот.
1-2 дня
Где можно сдать:В клинике
На дому
МатериалМоча
Мочевая кислота образуется в организме после расщепления пуриновых оснований (пуринов). Они входят в состав большинства органов и тканей, где образуют ДНК и РНК.
Они входят в состав большинства органов и тканей, где образуют ДНК и РНК.
1-2 дня
Где можно сдать:В клинике
На дому
МатериалМоча
Мочевая кислота – это вещество, которое образуется в результате метаболизма пуринов. Они, в свою очередь, являются основным компонентом ДНК и РНК.
Срок выполнения1-2 дня
Где можно сдать:В клинике
На дому
МатериалМоча
Магний – это один из микроэлементов, принимающих участие в большинстве биохимических реакций в организме, в том числе, в энергетическом обмене.
Срок выполнения1-2 дня
Где можно сдать:В клинике
На дому
МатериалМоча
Креатинин – это вещество, которое образуется в ходе обмена азотистых соединений. Это, в первую очередь, различные виды белков, нуклеиновые кислоты, некоторые витамины и гормоны.
Срок выполнения1-2 дня
Где можно сдать:В клинике
На дому
МатериалМоча
Креатинин – это соединение, которое образуется при распаде креатинфосфата. Этот процесс происходит, в основном, в мышечной ткани, которая требует значительного количества энергии для сокращения.
Этот процесс происходит, в основном, в мышечной ткани, которая требует значительного количества энергии для сокращения.
1-2 дня
В клинике
На дому
МатериалМоча
Кальций – один из важнейших минералов. Он обеспечивает прочность костей и зубной эмали, участвует в каскаде реакций, необходимых для передачи нервного импульса и мышечных сокращений, поддерживает способность крови к свертыванию.
Срок выполнения1-2 дня
Где можно сдать:В клинике
На дому
МатериалМоча
Желчные пигменты представляют собой продукты распада гемоглобина. В норме они в небольшом количестве циркулируют в крови, а затем подвергаются ряду химическим превращениям в печени.
Срок выполнения1-2 дня
Где можно сдать:В клинике
На дому
МатериалМоча
Бета-2-микроглобулин – это специфический белок, который входит в состав клеточных мембран.
1-2 дня
Где можно сдать:В клинике
На дому
МатериалМоча
Амилаза – фермент, вырабатывающийся клетками преимущественно поджелудочной железы, входящий в состав панкреатического сока. Ее функция – расщеплять в кишечнике сложные углеводы до моно- и дисахаридов.
Срок выполнения1-2 дня
Где можно сдать:В клинике
На дому
МатериалМоча
Альфа-амилаза – фермент, секретируемый клетками поджелудочной и слюнных желез, выполняющий функцию расщепления сложных углеводов на моно- и дисахара. Панкреатическая амилаза вырабатывается экзокринными панкреатоцитами поджелудочной железы и через протоки выделяется в полость двенадцатиперстной кишки.
Срок выполнения1-2 дня
Где можно сдать:В клинике
На дому
МатериалМоча
Альбумины – это растворимые белки, которые синтезируются в печени и участвуют в транспортировке питательных и биологически активных веществ, а также некоторых лекарственных препаратов.
1-2 дня
Где можно сдать:В клинике
На дому
МатериалМоча
Альбумин – это один из основных белков, находящихся в плазме крови. Он принимает участие в транспортировке витаминов, гормонов, билирубина, кальция, натрия, лекарственных препаратов, жирных кислот и других веществ.
Срок выполнения1-2 дня
Где можно сдать:В клинике
На дому
МатериалМоча
Показать все
Лицензии
Перейти в раздел лицензииПерейти в раздел правовая информация
Физики не смогли объяснить энергетическую неэффективность кинезина
Японские физики измерили с помощью оптического пинцета, какая часть энергии АТФ расходуется на движение «шагающего белка» кинезина и нагрев окружающей среды. Оказалось, что «полезная работа» составляет менее 20 процентов от химической энергии АТФ. После этого ученые разработали теоретическую модель и воспроизвели экспериментальные данные, однако так и не смогли найти качественное объяснение для таких высоких потерь. Статья опубликована в Physical Review Letters, кратко о ней сообщает Physics, препринт работы выложен на сайте arXiv.org.
Статья опубликована в Physical Review Letters, кратко о ней сообщает Physics, препринт работы выложен на сайте arXiv.org.
Моторные белки играют очень важную роль в биологических процессах, превращая химическую энергию в энергию движения (поэтому их часто называют биологическими моторами). Благодаря этим белкам делятся клетки, сокращаются мускулы, синтезируются новые белки и аминокислоты. Один из самых важных моторных белков — это кинезин-1, который «шагает» по поверхности внутриклеточных микротрубочек и перетаскивает мембранные пузырьки с грузом. Каждые несколько миллисекунд кинезин отрывает одну из своих «ног» от поверхности трубочки, переставляет ее и прикрепляет в следующей точке — из-за этого его иногда называют «шагающим белком». За секунду кинезин успевает сделать более сотни шагов. Благодаря кинезину клетка может участвовать в митозе и мейозе (то есть делиться на части), а отдельные ее органоиды — митохондрии или везикулы — перемещаются между различными частями клетки. Подробнее про работу кинезина и других биологических моторов можно прочитать в материалах «Машина из пробирки» и «Нанороботы внутри нас».
Подробнее про работу кинезина и других биологических моторов можно прочитать в материалах «Машина из пробирки» и «Нанороботы внутри нас».
Каждый раз, когда кинезин делает шаг и заново прикрепляется к подложке, он должен затратить энергию, поэтому для работы моторного белка необходимо своеобразное «топливо». В качестве такого «топлива» выступает молекула аденозинтрифосфат (АТФ), который окисляется до аденозиндифосфата (АДФ) и выделяет около 8,5×10−20 джоулей энергии. Наблюдения за движением кинезина показывают, что на каждый шаг белок тратит одну молекулу АТФ. В среднем, длина шага составляет около восьми нанометров, а максимальная тяга, которую может создать белок, не превышает семи пиконьютонов. Таким образом, для перемещения кинезина было бы достаточно 7×8 пиконьютон на нанометр, то есть всего 5,6×10−20 джоулей энергии. Получается, что около половины химической энергии расходуется «в никуда». Более того, обычно кинезин не шагает в одном направлении — при больших нагрузках белок часто делает шаги в обратную сторону, и его эффективная скорость сильно снижается.
Группа ученых под руководством Такаюки Арига (Takayuki Ariga) установила, на какие процессы кинезин расходует энергию АТФ. Чтобы корректно разделить энергии и упростить себе задачу, исследователи рассматривали только низкие нагрузки, при которых кинезин практически не делает шагов в обратную сторону. Для этого ученые прикрепляли к свободному концу кинезина наночастицу размером около 490 нанометров и тянули ее с помощью оптического пинцета — сфокусированного лазерного пучка, который действует на частицу с помощью градиентной силы. Более подробно про оптический пинцет можно прочитать в материале «Скальпель и пинцет». Чтобы измерить отклик кинезина на внешнее воздействие, физики тянули его с постоянной силой около двух пиконьютон и накладывали на нее колебания, амплитуда которых составляла примерно 20 процентов от постоянной силы. По этому отклику ученые могли не только измерить тягу белка, но и определить его положение на подложке.
После этого ученые измерили корреляции между скоростями движения кинезина при различных концентрациях АТФ в окружающей жидкости. Используя равенство Харада—Саса (Harada-Sasa equality) и дополняя его соотношением между флуктуациями и откликом (fluctuation-response relation), ученые рассчитали, какая часть энергии идет на совершение полезной работы, преодоления сопротивления вязкости жидкости или нагревание белка. Оказалось, что и в случае низкой, и в случае высокой концентрации АТФ на движение тратится около 20 процентов энергии, на нагревание — около 80 процентов, а потерями на вязкое трение можно пренебречь. Таким образом, кинезин — очень неэффективный мотор, особенно в сравнении с такими белками, как АТФ-синтаза (F1-ATPase), которая превращает в полезную работу около ста процентов химической энергии
Используя равенство Харада—Саса (Harada-Sasa equality) и дополняя его соотношением между флуктуациями и откликом (fluctuation-response relation), ученые рассчитали, какая часть энергии идет на совершение полезной работы, преодоления сопротивления вязкости жидкости или нагревание белка. Оказалось, что и в случае низкой, и в случае высокой концентрации АТФ на движение тратится около 20 процентов энергии, на нагревание — около 80 процентов, а потерями на вязкое трение можно пренебречь. Таким образом, кинезин — очень неэффективный мотор, особенно в сравнении с такими белками, как АТФ-синтаза (F1-ATPase), которая превращает в полезную работу около ста процентов химической энергии
Затем физики попытались разработать теоретическую модель, которая объясняет высокий уровень потерь. Для этого ученые описали кинезин марковской моделью с двумя состояниями и тремя возможными путями перехода между состояниями. Решая возникающие уравнения движения, физики рассчитали корреляционную функцию между скоростями и связали ее с параметрами кинезина, найденными из опыта. Оказалось, что теория довольно хорошо сходится с практикой. Тем не менее, интерпретировать эти уравнения ученые не смогли. Несмотря на то, что получившаяся модель несимметрична, списать потери энергии на эту особенность нельзя — в эксперименте кинезин практически не делал обратных шагов, но все равно продолжал нагреваться. Кроме того, нагрев нельзя объяснить мягкостью подложки, то есть «увязанием» белка. Хотя отношение «полезной» и «потерянной» энергии в этом предположении совпадают, отклик белка совпадает с экспериментально измеренной зависимостью только на низких частотах. Поэтому авторы заключают, что об энергии АТФ можно сказать только то, что она теряются внутри белка, а не расходуется на его движение.
Оказалось, что теория довольно хорошо сходится с практикой. Тем не менее, интерпретировать эти уравнения ученые не смогли. Несмотря на то, что получившаяся модель несимметрична, списать потери энергии на эту особенность нельзя — в эксперименте кинезин практически не делал обратных шагов, но все равно продолжал нагреваться. Кроме того, нагрев нельзя объяснить мягкостью подложки, то есть «увязанием» белка. Хотя отношение «полезной» и «потерянной» энергии в этом предположении совпадают, отклик белка совпадает с экспериментально измеренной зависимостью только на низких частотах. Поэтому авторы заключают, что об энергии АТФ можно сказать только то, что она теряются внутри белка, а не расходуется на его движение.
В ноябре 2015 года исследователи из Германии и Польши обнаружили, что в определенных условиях и вязкости среды кинезин останавливает свое движение при сопротивлении в 70 000 раз меньшем, чем максимальная нагрузка, которую он может нести. Это указывает на то, что движение кинезина скорее хаотично, чем упорядоченно. В том же месяце американские ученые разработали наноразмерную «машину», которая умеет двигаться в любом направлении по неровной поверхности. В отличие от природных «машин», таких как кинезин, эта молекула не изменяет состав субстрата, по которому шагает.
В том же месяце американские ученые разработали наноразмерную «машину», которая умеет двигаться в любом направлении по неровной поверхности. В отличие от природных «машин», таких как кинезин, эта молекула не изменяет состав субстрата, по которому шагает.
Дмитрий Трунин
Нашли опечатку? Выделите фрагмент и нажмите Ctrl+Enter.
Переходное состояние молекулы аденозинтрифосфата
Переходное состояние молекулы аденозинтрифосфатаАманда Гарейс, Джеремайя Кимбалл, Шонтэ Макнайт
- Цель проекта
- Научная база
- Вычислительный подход
- Результаты
- Ссылки
Цель проекта
Цель этого проекта заключалась в изучении уникального аспекта процесса превращения молекулы АТФ (аденозинтрифосфата) в молекулу АДФ (аденозиндифосфата) и неорганической фосфатной группы. Мы создали переходное состояние для этой реакции (конверсии) с помощью вычислительной модели частичной молекулы АТФ, чтобы лучше понять механизм реакции и определить ее энергию активации.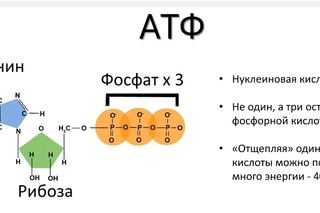
Вернуться к началу
Научное обоснование
Все клетки человеческого тела расщепляют пищу, которую мы едим, чтобы высвободить энергию для функций организма. АТФ [аденозинтрифосфат (3 фосфата)] представляет собой молекулу, которая хранит эту энергию. АТФ является эндергонической молекулой, то есть для ее образования требуется энергия. Около 95% энергии, используемой нашим телом, поступает из АТФ. АТФ состоит из аденина (азотистое основание в ДНК человека), рибозы (сахара) и трех фосфатных групп.Энергия хранится в ковалентных связях между каждой фосфатной группой, которые составляют хвост молекулы. Последняя фосфатная связь содержит наибольшую энергию (около 7 ккал/моль). Она называется пирофосфатной связью. Чтобы высвободить свою энергию в организме, АТФ распадается на АДФ [аденозиндифосфат (2 фосфата)] и неорганическую фосфатную группу и высвобождает энергию из пирофосфатной связи.
АДФ является экзэргонической молекулой, что означает, что при образовании она выделяет энергию. Когда АДФ реагирует, вступает в контакт с достаточным количеством энергии и неорганическим фосфатом (PO 4 ) становится АТФ и снова накапливает энергию. Чтобы снова стать АТФ, АДФ получает энергию и свой третий фосфат от дыхания. Больше АТФ образуется при аэробном дыхании (дыхании при наличии воздуха), чем при анаэробном дыхании (дыхании при отсутствии воздуха), потому что в этом участвует больше энергии. (Для тех, кто не знает, дыхание — это процесс, при котором организм использует кислород и пищу для обеспечения организма энергией.) Анаэробное дыхание обеспечивает организм прибл. 2 молекулы АТФ противостоят 38 молекулам АТФ при аэробном дыхании. Как видите, аэробное дыхание более эффективно.
Когда АДФ реагирует, вступает в контакт с достаточным количеством энергии и неорганическим фосфатом (PO 4 ) становится АТФ и снова накапливает энергию. Чтобы снова стать АТФ, АДФ получает энергию и свой третий фосфат от дыхания. Больше АТФ образуется при аэробном дыхании (дыхании при наличии воздуха), чем при анаэробном дыхании (дыхании при отсутствии воздуха), потому что в этом участвует больше энергии. (Для тех, кто не знает, дыхание — это процесс, при котором организм использует кислород и пищу для обеспечения организма энергией.) Анаэробное дыхание обеспечивает организм прибл. 2 молекулы АТФ противостоят 38 молекулам АТФ при аэробном дыхании. Как видите, аэробное дыхание более эффективно.
Переход между АТФ и АДФ постоянно происходит в организме, поскольку нашему телу постоянно нужна энергия для выполнения различных функций организма, поддерживающих жизнь.
АТФ= АДФ+неорганический фосфат+энергия
АДФ+неорганический фосфат+энергия= АТФ
Вернуться к началу
Вычислительный подход
Мы начали наш эксперимент, используя Power Macintosh 5400/200 с MacSpartan, приложением для моделирования вычислительной химии, но из-за размера и сложности молекул, которые мы выбрали для работы, мы были вынуждены использовать компьютер Silicon Graphics Indigo 2 с UNIXSpartan.
На протяжении всего эксперимента мы решили использовать AM1 в качестве нашей теории для нашего базового набора. По сути, мы сделали это, потому что это уменьшило количество процессорного времени. Полуэмпирический метод, такой как AM1, был более экономичным в вычислительном отношении, чем метод ab initio. Метод ab initio, такой как уровень теории базисного набора 6-31G*, был бы более желателен, потому что его подход, основанный только на математике, дает большую точность, но полуэмпирический метод был более эффективным в вычислительном отношении, чем аббревиатурный. инциальный метод.
Сначала мы построили часть молекулы АТФ, содержащую участок концевой связи. Мы не строили модель всей молекулы АТФ, потому что это было бы слишком сложно и слишком затратно в вычислительном отношении, чтобы сделать это за отведенное время. Затем мы построили модель АДФ, разорвав терминальную связь между двумя последними фосфатными группами, что можно сделать, ограничив длину связи между атомом кислорода и последней фосфатной группой.
Затем мы построили модель АДФ, разорвав терминальную связь между двумя последними фосфатными группами, что можно сделать, ограничив длину связи между атомом кислорода и последней фосфатной группой.
После построения и оптимизации геометрии этих молекул с помощью полуэмпирической теории базисного набора AM1 мы запросили поиск перехода, чтобы найти переходное состояние реакции. Чтобы определить, было ли найдено или рассчитано переходное состояние для реакции, вы должны запустить частотное сканирование молекулы, полученной в результате поиска перехода.
Переходное состояние указывается, когда в результате частотного сканирования обнаруживается одна и только одна мнимая частота.
Определив, что у нас есть одна и только одна мнимая частота и, следовательно, мы нашли переходное состояние нашей части молекулы АТФ, мы инициировали одноточечное сканирование энергии в каждой молекуле.
Сканирование энергии в одной точке используется для прогнозирования энергии и связанных с ней свойств молекулы во время реакции. Обычно, когда реагенты химической реакции объединяются, их энергетические уровни имеют тенденцию к резкому увеличению, потому что им нужно иметь достаточно энергии, чтобы преодолеть энергетический барьер. Разность энергетических уровней переходного состояния и реагентов называется энергией активации. Когда мы составили схему и график результатов трех молекулярно-точечных энергетических сканирований (SPE), мы обнаружили, что наша реакция не имеет энергетического барьера для пересечения и, следовательно, энергии активации или катализатора.
Обычно, когда реагенты химической реакции объединяются, их энергетические уровни имеют тенденцию к резкому увеличению, потому что им нужно иметь достаточно энергии, чтобы преодолеть энергетический барьер. Разность энергетических уровней переходного состояния и реагентов называется энергией активации. Когда мы составили схему и график результатов трех молекулярно-точечных энергетических сканирований (SPE), мы обнаружили, что наша реакция не имеет энергетического барьера для пересечения и, следовательно, энергии активации или катализатора.
Наверх
Результаты
Наше частотное сканирование выявило только одну воображаемую частоту, что означает, что мы нашли правильное переходное состояние. Результаты нашего одноточечного энергетического сканирования (SPE) нас удивили. Согласно нашему расчетному графику СПС, энергетического барьера не было вовсе. (Поскольку не было энергетического барьера, не было ни энергии активации, ни катализатора.) На графике среднего сканирования ТФЭ энергетический барьер был бы совершенно очевиден.
Вернуться к началу
Ссылки
Книги: Биддл, Верн., Химия: точность и дизайн. Издательство Бека Бук. (1986): 346-346.Грэм, Кит. Хикс, Лорел. Шиммен, Долорес. Томсон, Джордж. Биология: Живое творение Бога. Издательство Бека Бук. (1986): 137, 139, 141, 189, 221, 567, 576.
Хендриксон, Джеймс Б., Крам, Дональд Дж., Хаммонд, Джордж С. Органическая химия. Книжная компания McGraw-Hill. (1970): 1040,1042,1043,1045,1047,1048.
Лаундон, Марк Г. Органическая химия, второе издание. The Benjamin/Cummings Publishing Company, Inc. (1988): 1237, 1238.
Личное общение: Готвалс, Роберт, персональные инструкции, 18–22 августа 1997 г. Тиссен, Энн, персональные инструкции, 18–22 августа 1997 г. веб-страница BIO 181: Общая биология (специальности) I: Дыхание. Общественный колледж Пима, Тусон, Аризона. http://west.cscwc.pima.edu/~achristensen/respiration.html
М. Дж. Фараби. АТФ и биологическая энергия. http://www.emc.maricopa.edu/Bio/BIO181/bio181.html
http://www.emc.maricopa.edu/Bio/BIO181/bio181.html
Вводный модуль биохимии: Молекулы энергетической валюты. http://www.prm.unisa.edu.au/h&p1ener.htm#atp
Вернуться к началу
Что такое АТФ — Biology Wise
Нравится это? Поделиться!
АТФ является основным источником энергии в нашем организме, но знаете ли вы, что такое АТФ? Найдите ответ на этот вопрос с подробностями о функциях и производстве АТФ в этой статье.
Наше тело полностью зависит от энергии, получаемой из пищи, которую мы едим. Пища подвергается многим процессам, а затем, наконец, высвобождает АТФ. АТФ или аденозинтрифосфат является энергетической единицей клетки. Это один из самых важных и основных источников энергии тела. Он используется почти во всех функциях и производится двумя основными процессами: гликолизом и циклом лимонной кислоты (циклом Кребса).
Но прежде чем понять производство этих молекул, вам необходимо понять структуру и состав молекулы АТФ.
Структура молекулы АТФ
Молекула АТФ состоит из пуринового основания, пентозного сахара и фосфатной группы. Пуриновое основание, аденин, присоединено к 1′ атому углерода рибозы, которая представляет собой пентозный сахар. Три фосфатные группы присоединены к пентозе в положении 5′-атома углерода. Ниже приведена структура молекулы АТФ с ее составляющими.
Пуриновое основание, аденин, присоединено к 1′ атому углерода рибозы, которая представляет собой пентозный сахар. Три фосфатные группы присоединены к пентозе в положении 5′-атома углерода. Ниже приведена структура молекулы АТФ с ее составляющими.
Энергия запасается в P-P-P или фосфатной связи, которая высвобождается, когда связь разрывается и АТФ превращается в АДФ в процессе гидролиза, который также известен как дефосфорилирование.
АТФ + H 2 O → АДФ + Pi + энергия (30,6 кДж/моль)
В приведенной выше реакции АДФ представляет собой аденозиндифосфат, а Pi представляет собой неорганический фосфат. Реакция показывает расщепление АТФ и выделение энергии. Реакция также может быть обращена вспять, и АДФ может быть преобразован в АТФ, но для этого потребуется такое же количество энергии, которое высвобождается во время процесса, то есть 30,6 кДж. Этот процесс известен как конденсация или фосфорилирование. Это происходит потому, что молекула АТФ очень нестабильна и очень быстро подвергается гидролизу. Связи между фосфатной группой в молекуле АТФ слабее, чем в молекуле АДФ. Следовательно, мы можем сказать, что присутствие одной фосфатной группы может иметь значение в производстве и потреблении энергии молекулой.
Связи между фосфатной группой в молекуле АТФ слабее, чем в молекуле АДФ. Следовательно, мы можем сказать, что присутствие одной фосфатной группы может иметь значение в производстве и потреблении энергии молекулой.
Производство АТФ
АТФ вырабатывается на уровне клеточного дыхания. Он вырабатывается и потребляется при анаэробном и аэробном дыхании. Производство АТФ состоит из трех основных путей, а именно гликолиза, цикла Кребса или цикла лимонной кислоты и фосфорилирования переноса электронов или бета-окисления. Гликолиз и цикл лимонной кислоты осуществляются при клеточном дыхании. Давайте подробно разберем схему клеточного дыхания и три пути.
Гликолиз
Это первый путь дыхания человека. В этом процессе одна молекула глюкозы превращается в две молекулы пирувата, который используется в качестве основного компонента в следующем пути. При этом высвобождаются 2 молекулы АТФ, которые считаются тяжелыми молекулами, так как обладают большой энергией. Эта энергия сохраняется и используется организмом позже.
Цикл Кребса или цикл лимонной кислоты
После гликолиза следующим путем является цикл Кребса или цикл лимонной кислоты. Две молекулы пирувата, образовавшиеся в результате гликолиза, окисляются в этом процессе с выделением CO 9 .0040 2 . Молекулы АТФ высвобождаются в виде побочных продуктов и поглощаются митохондриями, которые затем поставляют энергию для выполнения различных задач. Этот процесс также производит молекулы 2ATP.
Электронно-транспортное фосфорилирование
Электроны, переносимые через НАДН, образующийся в ходе гликолиза и цикла лимонной кислоты, и ФАДН 2 , образующийся в цикле лимонной кислоты, используются для фосфорилирования переноса электронов. В этом процессе образуется 32 молекулы АТФ.
Следовательно, общее количество АТФ, образующееся при аэробном дыхании, равно 2 + 2 + 32 = 36.
Молекула АТФ используется для многих целей. АТФ является важной молекулой в метаболизме, так как содержит много энергии, которая используется во многих метаболических процессах.