ЛЕЦИТИН СОЕВЫЙ® Стимулятор мозговой активности, 100 шт.
Лецитин оказывает стимулирующее действие на иммунную систему, память, мыслительную деятельность и органы пищеварения. Это ценный строительный материал для клеток сердца, мозга, нервной системы. Нехватка лецитина приводит к истончению этой оболочки и ведет к повышенной раздражительности, усталости, бессоннице, нервному истощению, депрессии и ухудшению памяти.
Лецитин используется для профилактики хронических холециститов и дискинезий желчных путей, играет существенную роль в предупреждении и комплексной терапии таких заболеваний, как атеросклероз, сахарный диабет II типа, жировой гепатоз, цирроз печени, заболевания нервной системы, болезнь Альцгеймера, травматические и инфекционные поражения нервной системы, рассеянный склероз, паркинсонизм, псориаз и многие другие.
Также лецитин полезен для беременных, так как он может значительно улучшить условия созревания плода и облегчить протекание родов. Беременным и кормящим перед приемом препарата следует проконсультироваться с врачом!
Беременным и кормящим перед приемом препарата следует проконсультироваться с врачом!
Фармакологическое действие
- Укрепляет нервную систему;
- Стимулирует функции мозга;
- Поддерживает работу сердца;
- Нормализует уровень холестерина и сахара в крови;
- Предотвращает отложение жиров в печени.
Применение
Взрослым 1 капсуле в день предпочтительно во время еды или по назначению специалиста. Курс приема: 2-3 месяца 1-2 раза в год или по рекомендации специалиста
Важное
• Нутрицевтик (БАД) – не является лекарственным средством
• Номер свидетельства: KZ.16.01.79.003.E.000176.02.19
• Отпускается без рецепта врача
• Хранить при комнатной температуре, в сухом, недоступном для детей месте
• Срок годности 3 года
• На рынке с 2019 года
• Во время беременности и лактации проконсультироваться с врачом
• Производство: США
• Производитель: Earth’s Creation
• Организация, принимающая претензии в РК: ТОО «OZON LIFE CARE»
Название и серия
Оригинальное название
Natural Soya Lecithin
Упаковка
Страна производитель
США
Объем
100 шт.
Тип продукта
Капсулы
Состав
Основной компонент
Соевый лицетин
Назначение
Показания
Атеросклероз
Отзывы
5/ 5
средний рейтинг товара
Галина
01.06.2020
Спасибо большое за продукцию и внимательное квалифицированное обслуживание Марии. Приятно что продукция Столетие здоровья не осталась без внимания и Гриновеа взялась за их продукцию. Продукт Лецитин всегда на страже моего здоровьяГанна Владимировна
01.06.2020
Уже 10 лет пью соевый лецитин. В моем возрасте есть склероз, в моей возрасте и нарушение сердечно сосудистой системы. У меня была операция на головной мозг, удаление гематомы. Принимаю препарат осенью и весной 2 раза в год. Я чувствую как он хорошо помогает.
Надежда
12.05.2020
Маме 72 года и у нее начались проблемы со сном и памятью. Читала в интернете что эти проблемы решает Лицетин. Я остановила свой выбор именно на Соевом Лицетине потому что: 1. Он представлен в жидкой форме, что дает лучшее усвоение. 2. Удобство применения (1 раз в день) 3. Производитель.
2. Удобство применения (1 раз в день) 3. Производитель.
Результат превзошел мои ожидания! Даже не буду описывать на сколько он оказался эффективен — это надо будет много писать. Просто рекомендую!
Галина Б
12.05.2020
Достоинства
Отличный лецитин
Недостатки
Нет
Ольга
12.05.2020
Достоинства!
Лецитин очень полезен для работы мозга, нервной системы, пищеварения- в общем для всего организма.
Купила подростку на период сдачи экзаменов — попробовать в действии -за 3 недели приема дочь стала меньше уставать, перестала реагировать на метеоусловия. Общее самочувствие улучшилось. Эффект понравился.
Данный БАД я очень рекомендую к приему.
Нет вопросов о данном товаре, станьте первым и задайте свой вопрос.
Ум человека улучшили с помощью стимуляции мозга
03 ноября 2021 16:46 Ольга Мурая
Учёные обнаружили область мозга, отвечающую за контроль над мыслями и поведением.
Фото Robina Weermeijer/Unsplash.
Новый метод электростимуляции мозга работает под управлением искусственного интеллекта. Учёные ожидают, что он поможет справиться с симптомами многих расстройств поведения.
Учёные из Медицинской школы Университета Миннесоты и Массачусетской больницы общего профиля показали в пробном исследовании с участием людей, что определённые функции человеческого мозга, связанные с самоконтролем и гибкостью ума, можно улучшить.
Достичь этого интригующего результата удалось, объединив возможности искусственного интеллекта и прицельной электрической стимуляции мозга.
Исследование проводилось с участием 12 пациентов, перенёсших операцию на головном мозге из-за эпилепсии. Во время этой процедуры им внедрили в мозг сотни крошечных электродов. Они размещаются по всему мозгу для регистрации его активности и определения места возникновения судорожного очага.
Учёные определили область мозга, улучшающую при стимуляции слабым током психические функции пациентов. Эта часть мозга — внутренняя капсула — отвечает за когнитивный контроль, процесс перехода от одного образа мышления или поведения к другому, который нарушается при большинстве психических заболеваний.
«Примером может быть человек с депрессией, который не может избавиться от «застрявшей» в голове негативной мысли. Поскольку [когнитивный контроль] играет ключевую роль в психических заболеваниях, поиск способа его улучшения может стать новым действенным методом лечения этих болезней», – сообщил ведущий автор работы доктор Алик Видж (Alik Widge) из Университета Миннесоты.
Исследовательская группа разработала алгоритмы, отслеживающие способности пациентов к когнитивному контролю, как по их действиям, так и непосредственно по их мозговой активности.
Когда пациенты хуже выполняли лабораторные тесты на когнитивный контроль, искусственный интеллект считывал это и усиливал электрическую стимуляцию их мозга.
«Эта система может считывать активность мозга и расшифровывать её. Когда у пациента возникают трудности, она применяет небольшой электрический импульс к мозгу, чтобы помочь ему преодолеть эту трудность, – объясняет Видж. – Я часто использую аналогию с электрическим велосипедом. Когда кто-то крутит педали, но делает это с трудом, велосипед это считывает и «помогает» человеку. Мы создали аналог такой системы для психических функций человека».
Это исследование впервые показало, что:
- Определённая психическая функция человека, связанная с психическим заболеванием, может быть надёжно улучшена с помощью точно направленной электрической стимуляции;
- В структуре внутренней капсулы мозга есть определённые участки, которые особенно эффективны с точки зрения улучшения когнитивных функций;
- Алгоритм с обратной связью, используемый в качестве контролёра, был вдвое эффективнее, чем периодическая стимуляция в случайные моменты времени.

Некоторые пациенты помимо эпилепсии имели сильную тревожность. Это неудивительно, учитывая, какие сложности порождает их основное заболевание.
Когда пациенты получали стимулирующую когнитивную стимуляцию, они сообщали, что их тревожность уменьшалась. Им было легче отвлечься от своих переживаний и сосредоточиться на том, чего они хотели.
Авторы работы говорят, что этот метод в будущем можно будет использовать для лечения пациентов с тяжёлой и устойчивой к лекарствам тревожностью, депрессией или другими расстройствами.
«Это может быть совершенно новый подход к лечению психических заболеваний. Вместо того чтобы пытаться подавить симптомы, мы могли бы дать пациентам инструмент, который позволял им управлять своим собственным сознанием, – добавил доктор Видж. – Мы могли бы вернуть их на место «пилота» и позволить им ощутить новое чувство контроля над своим сознанием».
Сейчас исследователи готовятся к клиническим испытаниям нового метода. Они отмечают, что это исследование может быть выполнено с помощью уже существующих инструментов и устройств. Это значит, что после официального одобрения испытаний системы на пациентах, перевод этого вида помощи в современную медицинскую практику будет быстрым.
Они отмечают, что это исследование может быть выполнено с помощью уже существующих инструментов и устройств. Это значит, что после официального одобрения испытаний системы на пациентах, перевод этого вида помощи в современную медицинскую практику будет быстрым.
Стоит отметить, что испытания нового метода усиления умственных способней получили грант Армейской исследовательской организации США. Это говорит о том, что перспектива искусственного улучшения внимания и гибкости ума интересна не только в качестве «лекарства» для нуждающихся, но и как потенциальная военная технология, улучшающая способности солдат.
Работа американских исследователей была опубликована в издании Nature Biomedical Engineering.
Ранее мы писали о том, что электрическая стимуляция мозга помогла невыспавшимся солдатам решать сложные задачи, а также о том, что стимуляция обоняния поможет справиться с болезнями Паркинсона и Альцгеймера.
Больше новостей из мира науки и медицины вы найдёте в разделах «Наука» и «Медицина» на медиаплатформе «Смотрим».
наука мозг психиатрия способности стимуляция общество новости медицина
Ранее по теме
Заядлые поклонники чистоты и порядка нездоровы?
Прорыв: новый антидепрессант действует уже через два часа после приёма
Найдена необычная причина нервного состояния многих людей
Дневной сон вреден для людей с тревожностью и эмоциональными травмами?
Всего один звук спасает людей от ночных кошмаров
Общение с собаками улучшает работу мозга людей
Влияние стимуляторов на функцию мозга при синдроме дефицита внимания/гиперактивности: систематический обзор и метаанализ
1. Американская психиатрическая ассоциация. 4-е изд. Американская психиатрическая ассоциация; Вашингтон, округ Колумбия: 2000. Диагностическое и статистическое руководство по психическим расстройствам. [Google Scholar]
Американская психиатрическая ассоциация. 4-е изд. Американская психиатрическая ассоциация; Вашингтон, округ Колумбия: 2000. Диагностическое и статистическое руководство по психическим расстройствам. [Google Scholar]
2. Рубиа К. «Холодная» нижняя лобно-стриарная дисфункция при синдроме дефицита внимания/гиперактивности (СДВГ) по сравнению с «горячей» вентромедиальной орбитофронтолимбической дисфункцией при расстройстве поведения: обзор. Биол психиатрия. 2011;69: e69–e87. [PubMed] [Google Scholar]
3. Кубильо А., Халари Р., Смит А., Джампьетро В., Тейлор Э., Рубиа К. Фронто-кортикальные и лобно-подкорковые аномалии головного мозга у детей и взрослых с СДВГ: Обзор и доказательства лобно-стриарных дисфункций у взрослых с СДВГ, наблюдаемых с детства во время мотивации и внимания. кора. 2012;48:194–215. [PubMed] [Google Scholar]
4. Рубиа К., Халари Р., Кристаку А., Тейлор Э. Импульсивность как нарушение синхронизации: нейрокогнитивные нарушения при синдроме дефицита внимания с гиперактивностью во время временных процессов и нормализация с помощью метилфенидата. Philos Trans R Soc Lond B Biol Sci. 2009 г.;364:1919–1931. [Бесплатная статья PMC] [PubMed] [Google Scholar]
Philos Trans R Soc Lond B Biol Sci. 2009 г.;364:1919–1931. [Бесплатная статья PMC] [PubMed] [Google Scholar]
5. Норейка В., Фальтер К., Рубиа К. Дефицит времени у пациентов с СДВГ. Нейропсихология. 2012; 51: 235–266. [PubMed] [Google Scholar]
6. Харт Х., Радуа Дж., Матайкс Д., Рубиа К. Метаанализ исследований фМРТ временных функций при СДВГ. Neurosci Biobehav Rev. 2012; 36: 2248–2256. [PubMed] [Google Scholar]
7. Cortese S., Kelly C., Chabernaud C., Proal E., Di Martino A., Milham M.P., Castellanos F.X. К системной нейронауке СДВГ: метаанализ 55 исследований фМРТ. Am J Психиатрия. 2012;169: 1038–1055. [Бесплатная статья PMC] [PubMed] [Google Scholar]
8. Nakao T., Radua C., Rubia K., Mataix-Cols D. Аномалии объема серого вещества при СДВГ и эффекты стимулирующих препаратов: метаданные на основе вокселей. -анализ. Am J Психиатрия. 2011; 168:1154–1163. [PubMed] [Google Scholar]
9. Конрад К., Эйкхофф С.Б. Мозг СДВГ устроен по-другому? Обзор структурных и функциональных связей при синдроме дефицита внимания и гиперактивности. Hum Brain Map. 2010;31:904–916. [Бесплатная статья PMC] [PubMed] [Google Scholar]
Hum Brain Map. 2010;31:904–916. [Бесплатная статья PMC] [PubMed] [Google Scholar]
10. Валера Э.М., Фараоне С.В., Мюррей К.Е., Сейдман Л.Дж. Метаанализ результатов структурной визуализации при синдроме дефицита внимания/гиперактивности. Биол психиатрия. 2007; 61: 1361–1369. [PubMed] [Google Scholar]
11. Виленс Т.Е. Влияние метилфенидата на катехоламинергическую систему при синдроме дефицита внимания/гиперактивности. J Clin Psychopharmacol. 2008; 28:S46–S53. [PubMed] [Google Scholar]
12. Hanwella R., Senanayake M., de Silva V. Сравнительная эффективность и переносимость метилфенидата и атомоксетина при лечении синдрома дефицита внимания с гиперактивностью у детей и подростков: метаанализ. БМС Психиатрия. 2011;11:176. [Бесплатная статья PMC] [PubMed] [Google Scholar]
13. Волков Н.Д., Фаулер Дж.С., Дин Ю.С., Ван Г.Дж., Гэтли С.Дж. Радиолиганды позитронно-эмиссионной томографии для переносчиков дофамина и исследования на человеке и приматах. Adv Pharmacol. 1998;42:211–214. [PubMed] [Google Scholar]
1998;42:211–214. [PubMed] [Google Scholar]
14. Fusar-Poli P., Rubia K., Rossi G., Sartori G., Ballotin U. Изменения транспортера дофамина при СДВГ: патофизиология или адаптация к психостимуляторам? Метаанализ. Am J Психиатрия. 2012; 169: 264–272. [PubMed] [Академия Google]
15. Hannestad J., Gallezot J.D., Planeta-Wilson B., Lin S.F., Williams W.A., van Dyck C.H. Клинически значимые дозы метилфенидата значительно занимают переносчики норадреналина у человека in vivo. Биол психиатрия. 2010; 68: 854–860. [Бесплатная статья PMC] [PubMed] [Google Scholar]
16. Рубиа К., Халари Р., Кубильо А., Мохаммад М., Тейлор Э. Метилфенидат нормализует дефицит активации и функциональной связи в сетях внимания и мотивации при приеме лекарств. наивные дети с СДВГ во время непрерывного задания с вознаграждением. Нейрофармакология. 2009 г.;57:640–652. [PubMed] [Google Scholar]
17. Рубиа К., Халари Р., Кубильо А., Смит А., Мохаммад М., Браммер М., Тейлор Э. Метилфенидат нормализует лобно-полосатую недостаточность во время интерференционного торможения при приеме лекарств. наивные мальчики. Нейропсихофармакология. 2011;36:1575–1586. [Бесплатная статья PMC] [PubMed] [Google Scholar]
наивные мальчики. Нейропсихофармакология. 2011;36:1575–1586. [Бесплатная статья PMC] [PubMed] [Google Scholar]
18. Рубиа К., Халари Р., Тейлор Э., Браммер М. Метилфенидат нормализует лобно-поясную недостаточность во время обработки ошибок у детей с синдромом дефицита внимания и гиперактивности. Биол психиатрия. 2011;70:255–262. [Бесплатная статья PMC] [PubMed] [Google Scholar]
19. Познер Дж., Майя Т.В., Фейр Д., Петерсон Б.С., Сонуга-Барке Э.Дж., Нагель Б.Дж. Ослабление дисфункциональной эмоциональной обработки с помощью стимуляторов: исследование подростков с СДВГ с помощью фМРТ. Психиатрия рез. 2011; 193:151–160. [Бесплатная статья PMC] [PubMed] [Google Scholar]
20. Петерсон Б.С., Потенца М.Н., Ван З., Чжу Х., Мартин А., Марш Р. МРТ-исследование эффектов психостимуляторов на обработку в режиме по умолчанию во время выполнения заданий Струпа у юношей с СДВГ. Am J Психиатрия. 2009 г.;166:1286–1294. [PMC free article] [PubMed] [Google Scholar]
21. Кобель М. , Бехтель Н., Вебер П., Шпехт К., Клархофер М., Шеффлер К. Влияние метилфенидата на функционирование рабочей памяти у детей с вниманием синдром дефицита/гиперактивности. Eur J Paediatr Neurol. 2009; 13: 516–523. [PubMed] [Google Scholar]
, Бехтель Н., Вебер П., Шпехт К., Клархофер М., Шеффлер К. Влияние метилфенидата на функционирование рабочей памяти у детей с вниманием синдром дефицита/гиперактивности. Eur J Paediatr Neurol. 2009; 13: 516–523. [PubMed] [Google Scholar]
22. Кубильо А., Смит А., Баррат Н., Джампиетро В., Браммер М., Симмонс А., Рубиа К. Лекарственно-специфические эффекты латеральности на активацию атомоксетина в лобных долях и метилфенидат у мальчиков с СДВГ во время рабочей памяти. Психомед. 2013;19: 1–14. [PubMed] [Google Scholar]
23. Кубильо А., Смит А.Б., Барретт Н., Джампьетро В., Браммер М.Дж., Симмонс А., Рубиа К. Общие и специфические эффекты атомоксетина и метилфенидата на ингибиторную дисфункцию головного мозга у мальчиков с СДВГ, ранее не принимавших лекарства [опубликовано онлайн до печати 9 октября] Cortex Cereb. 2012 г.: 10.1093/cercor/bhs296. [PMC free article] [PubMed] [Google Scholar]
24. Smith A., Cubillo A., Barrett N., Giampietro V., Simmons A., Brammer M., Rubia K. Нейрофункциональные эффекты метилфенидата и атомоксетина при мальчики с СДВГ во время дискриминации во времени. Биол психиатрия. 2013;74:615–622. [PubMed] [Академия Google]
Нейрофункциональные эффекты метилфенидата и атомоксетина при мальчики с СДВГ во время дискриминации во времени. Биол психиатрия. 2013;74:615–622. [PubMed] [Академия Google]
25. Вайдья С.Дж., Остин Г., Киркорян Г., Ридлехубер Х.В., Десмонд Дж.Е., Гловер Г.Х., Габриэли Д.Д. Избирательные эффекты метилфенидата при синдроме дефицита внимания и гиперактивности: функциональное магнитно-резонансное исследование. Proc Natl Acad Sci U S A. 1998; 95:14494–14499. [Бесплатная статья PMC] [PubMed] [Google Scholar]
26. Эпштейн Дж. Н., Кейси Б. Дж., Тонев С. Т., Дэвидсон М. К., Рейсс А. Л., Гарретт А. Эффекты активации мозга, связанные с СДВГ и лекарствами, в парах родитель-ребенок, связанных с СДВГ. с СДВГ. J Детская психологическая психиатрия. 2007;48:899–913. [PubMed] [Google Scholar]
27. Friston K.J., Rotshtein P., Geng J.J., Sterzer P., Henson R.N. Критика функциональных локализаторов. Нейроизображение. 2006;30:1077–1087. [PubMed] [Google Scholar]
28. Волков Н. , Ван Г., Фаулер Дж., Логан Дж., Ангрист Б., Хитцеманн Р. Влияние метилфенидата на региональный метаболизм глюкозы в головном мозге у людей: связь с дофаминовыми рецепторами D2 . Am J Психиатрия. 1997; 154:50–55. [PubMed] [Google Scholar]
, Ван Г., Фаулер Дж., Логан Дж., Ангрист Б., Хитцеманн Р. Влияние метилфенидата на региональный метаболизм глюкозы в головном мозге у людей: связь с дофаминовыми рецепторами D2 . Am J Психиатрия. 1997; 154:50–55. [PubMed] [Google Scholar]
29. Волков Н.Д., Фаулер Дж.С., Ван Г., Дин Ю., Гэтли С.Дж. Механизм действия метилфенидата: данные исследований ПЭТ. Джей Аттен Расстройство. 2002; 6 (прил. 1): S31–S43. [PubMed] [Академия Google]
30. Волков Н.Д., Ван Г.Дж., Фаулер Дж.С., Гэтли С.Дж., Логан Дж., Дин Ю.С. Занятость переносчика дофамина внутривенным метилфенидатом: последствия для его усиливающих эффектов. Abstr Soc Neurosci. 1998;24:778. [Google Scholar]
31. Буллмор Э., Лонг К., Саклинг Дж., Фадили Дж., Калверт Г., Селайя Ф. Цветной шум и вычислительный вывод в нейрофизиологическом (фМРТ) анализе временных рядов: методы повторной выборки во времени и вейвлет домены. Hum Brain Map. 2001; 12:61–78. [Бесплатная статья PMC] [PubMed] [Google Scholar]
32. Браммер М. Дж., Буллмор Э.Т., Симмонс А., Уильямс С.К., Грасби П.М., Ховард Р.Дж. Общее картирование активации мозга при функциональной магнитно-резонансной томографии: непараметрический подход. Mag Reson Imaging. 1997; 15: 763–770. [PubMed] [Google Scholar]
Дж., Буллмор Э.Т., Симмонс А., Уильямс С.К., Грасби П.М., Ховард Р.Дж. Общее картирование активации мозга при функциональной магнитно-резонансной томографии: непараметрический подход. Mag Reson Imaging. 1997; 15: 763–770. [PubMed] [Google Scholar]
33. Talairach J., Tournoux P. Thieme; Нью-Йорк: 1988. Копланарный стереотаксический атлас мозга. [Google Scholar]
34. Bullmore E.T., Brammer M.J., Rabe-Hesketh S., Curtis V.A., Morris R.G., Williams S.C.R. Методы диагностики и лечения коррелированного со стимулом движения в общих исследованиях активации мозга с использованием фМРТ. Hum Brain Map. 1999;7:38–48. [Бесплатная статья PMC] [PubMed] [Google Scholar]
35. Bullmore ET, Suckling J., Overmeyer S., Rabe-Hesketh S., Taylor E., Brammer MJ Глобальные, воксельные и кластерные тесты, по теории и перестановка, для различия между двумя группами структурных МР-изображений головного мозга. IEEE Trans Med Imaging. 1999; 18:32–42. [PubMed] [Google Scholar]
36. Строуп Д. Ф., Берлин Дж.А., Мортон С.К., Олкин И., Уильямсон Г.Д., Ренни Д. Мета-анализ обсервационных исследований в эпидемиологии: предложение для отчета. Группа метаанализа обсервационных исследований в эпидемиологии (MOOSE). ДЖАМА. 2000;293:2008–2012. [PubMed] [Google Scholar]
Ф., Берлин Дж.А., Мортон С.К., Олкин И., Уильямсон Г.Д., Ренни Д. Мета-анализ обсервационных исследований в эпидемиологии: предложение для отчета. Группа метаанализа обсервационных исследований в эпидемиологии (MOOSE). ДЖАМА. 2000;293:2008–2012. [PubMed] [Google Scholar]
37. Харт Х., Радуа Дж., Матайкс Д., Рубиа К. Мета-анализ исследований торможения и внимания при СДВГ с помощью фМРТ: изучение эффектов стимулирующих препаратов и возраста при специфических задачах. Джама Психиатрия. 2013;70:185–198. [PubMed] [Google Scholar]
38. Radua J., Mataix-Cols D. Воксельный метаанализ изменений серого вещества при обсессивно-компульсивном расстройстве. Бр Дж. Психиатрия. 2009; 195: 393–402. [PubMed] [Google Scholar]
39. Radua J., Mataix-Cols D. Неоднородность метаанализа данных нейровизуализации на основе координат: пример из исследований OCD Reply. Бр Дж. Психиатрия. 2010;197:77. [PubMed] [Google Scholar]
40. Radua J., Mataix-Cols D., Phillips M.L., El-Hage W. , Kronhaus D.M., Cardoner N., Surguladze S. Новый метааналитический метод нейровизуализационных исследований, объединяет зарегистрированные координаты пиков и статистические параметрические карты. Европейская психиатрия. 2012;27:605–611. [PubMed] [Google Scholar]
, Kronhaus D.M., Cardoner N., Surguladze S. Новый метааналитический метод нейровизуализационных исследований, объединяет зарегистрированные координаты пиков и статистические параметрические карты. Европейская психиатрия. 2012;27:605–611. [PubMed] [Google Scholar]
41. Radua J., van den Heuvel O.A., Surguladze S., Mataix-Cols D. Метааналитическое сравнение исследований морфометрии на основе вокселов при обсессивно-компульсивном расстройстве и других тревожных расстройствах. Арх генерал психиатрия. 2010;67:701–711. [PubMed] [Академия Google]
42. Radua J., Via E., Catani M., Mataix-Cols D. Основанный на вокселах метаанализ региональных различий объема белого вещества при расстройствах аутистического спектра по сравнению со здоровыми людьми. Психомед. 2011;41:1539–1550. [PubMed] [Google Scholar]
43. Урожденная Д.Э., Вейгер Т.Д., Джонидес Дж. Разрешение интерференции: результаты метаанализа задач нейровизуализации. Cogn Affect Behav Neurosci. 2007; 7:1–17. [PubMed] [Google Scholar]
44. Simmonds D.J., Pekar J.J., Mostofsky S.H. Мета-анализ задач «годен / не годен», демонстрирующий, что активация фМРТ, связанная с торможением ответа, зависит от задачи. Нейропсихология. 2008; 46: 224–232. [Бесплатная статья PMC] [PubMed] [Google Scholar]
Simmonds D.J., Pekar J.J., Mostofsky S.H. Мета-анализ задач «годен / не годен», демонстрирующий, что активация фМРТ, связанная с торможением ответа, зависит от задачи. Нейропсихология. 2008; 46: 224–232. [Бесплатная статья PMC] [PubMed] [Google Scholar]
45. Wager T.D., Jonides J., Reading S. Нейровизуализационные исследования переключения внимания: метаанализ. Нейроизображение. 2004; 22:1679–1693. [PubMed] [Google Scholar]
46. Буксбаум Б.Р., Грир С., Чанг В.Л., Берман К.Ф. Мета-анализ нейровизуализационных исследований задачи сортировки карт в Висконсине и процессов компонентов. Hum Brain Map. 2005; 25:35–45. [Бесплатная статья PMC] [PubMed] [Google Scholar]
47. Чемберс К.Д., Беллгроув М.А., Гулд И.К., Инглиш Т., Гараван Х., Макнот Э. Диссоциативные механизмы когнитивного контроля в префронтальной и премоторной коре. J Нейрофизиол. 2007;98:3638–3647. [PubMed] [Google Scholar]
48. Чемберс К.Д., Беллгроув М.А., Стоукс М.Г., Хендерсон Т.Р., Гараван Х., Робертсон И. Х. Исполнительный «отказ тормоза» после деактивации лобной доли человека. J Cogn Neurosci. 2006; 18: 444–455. [PubMed] [Google Scholar]
Х. Исполнительный «отказ тормоза» после деактивации лобной доли человека. J Cogn Neurosci. 2006; 18: 444–455. [PubMed] [Google Scholar]
49. Хуан С.-Х., Магглтон Н.Г. Стимуляция мозга и тормозной контроль. Мозговой стимул. 2012;5:63–69. [PubMed] [Google Scholar]
50. Арон А.Р., Флетчер П.С., Буллмор Э.Т., Саакян Б.Дж., Роббинс Т.В. Торможение стоп-сигнала нарушено из-за повреждения правой нижней лобной извилины у человека. Нат Нейроски. 2003; 6: 115–116. [PubMed] [Академия Google]
51. Рубиа К., Смит А. Нейронные корреляты когнитивного управления временем: обзор. Acta Neurobiol Exp (Wars) 2004; 64: 329–340. [PubMed] [Google Scholar]
52. Wiener M., Turkeltaub P., Coslett H.B. Образ времени: воксельный метаанализ. Нейроизображение. 2010;49:1728–1740. [PubMed] [Google Scholar]
53. Корбетта М., Патель Г., Шульман Г.Л. Система переориентации человеческого мозга: от среды к теории разума. Нейрон. 2008; 58: 306–324. [Бесплатная статья PMC] [PubMed] [Google Scholar]
54. Шульман Г.Л., Астафьев С.В., Франке Д., Поуп Д.Л.В., Снайдер А.З., МакЭвой М.П., Корбетта М. Взаимодействие стимул-обусловленной переориентации и ожидания в вентральных и дорсальных лобно-теменных и базальных ганглиозно-корковых сетях. Дж. Нейроски. 2009; 29: 4392–4407. [Бесплатная статья PMC] [PubMed] [Google Scholar]
Шульман Г.Л., Астафьев С.В., Франке Д., Поуп Д.Л.В., Снайдер А.З., МакЭвой М.П., Корбетта М. Взаимодействие стимул-обусловленной переориентации и ожидания в вентральных и дорсальных лобно-теменных и базальных ганглиозно-корковых сетях. Дж. Нейроски. 2009; 29: 4392–4407. [Бесплатная статья PMC] [PubMed] [Google Scholar]
55. Derrfuss J., Brass M., Neumann J., von Cramon D.Y. Участие нижнего лобного перехода в когнитивном контроле: метаанализ переключения и исследования Струпа. Hum Brain Map. 2005; 25:22–34. [Бесплатная статья PMC] [PubMed] [Google Scholar]
56. Хэмпшир А., Чемберлен С.Р., Монти М.М., Дункан Дж., Оуэн А.М. Роль правой нижней лобной извилины: торможение и контроль внимания. Нейроизображение. 2010;50:1313–1319. [Бесплатная статья PMC] [PubMed] [Google Scholar]
57. Сили В.В., Менон В., Шацберг А.Ф., Келлер Дж., Гловер Г.Х., Кенна Х. Диссоциируемые внутренние сети связи для обработки значимости и исполнительного контроля. Дж. Нейроски. 2007; 27: 2349–2356. [Бесплатная статья PMC] [PubMed] [Google Scholar]
[Бесплатная статья PMC] [PubMed] [Google Scholar]
58. Willcutt E.G., Doyle A.E., Nigg J.T., Faraone S.V., Pennington B.F. Обоснованность теории исполнительных функций синдрома дефицита внимания/гиперактивности: метааналитический обзор. Биол психиатрия. 2005; 57: 1336–1346. [PubMed] [Google Scholar]
59. Lijffijt M., Kenemans JL, Verbaten M.N., van Engeland H. Метааналитический обзор эффективности остановки при синдроме дефицита внимания/гиперактивности: недостаточный тормозной двигательный контроль? J Abnorm Psychol. 2005; 114: 216–222. [PubMed] [Академия Google]
60. Дикштейн С.Г., Бэннон К., Кастелланос Ф.Х., Милхэм М.П. Нейронные корреляты синдрома дефицита внимания и гиперактивности: метаанализ ALE. J Детская психологическая психиатрия. 2006;47:1051–1062. [PubMed] [Google Scholar]
61. Рубиа К., Халари Р., Смит А.Б., Мохаммад М., Скотт С., Браммер М.Дж. Общие и специфичные для расстройств префронтальные аномалии у мальчиков с чистым синдромом дефицита внимания/гиперактивности в сравнении мальчикам с чистым КР при интерференционном торможении и распределении внимания. J Детская психологическая психиатрия. 2009 г.;50:669–678. [PubMed] [Google Scholar]
J Детская психологическая психиатрия. 2009 г.;50:669–678. [PubMed] [Google Scholar]
62. Смит А.Б., Тейлор Э., Браммер М., Халари Р., Рубиа К. Снижение активации в правой латеральной префронтальной коре и передней поясной извилине у подростков с синдромом дефицита внимания и гиперактивности, ранее не получавших медикаментозное лечение. во время временной дискриминации. J Детская психологическая психиатрия. 2008; 49: 977–985. [PubMed] [Google Scholar]
63. Рубиа К., Халари Р., Смит А.Б., Мохаммед М., Скотт С., Джампиетро В. Диссоциированные функциональные мозговые аномалии торможения у мальчиков с чистым расстройством поведения и у мальчиков с чистым расстройством поведения. Синдром дефицита внимания и гиперактивности. Am J Психиатрия. 2008;165:889–897. [PubMed] [Google Scholar]
64. Rubia K., Overmeyer S., Taylor E., Brammer M., Williams S.C., Simmons A., Bullmore E.T. Гипофронтальность при синдроме дефицита внимания с гиперактивностью во время контроля моторики высшего порядка: исследование с помощью функциональной МРТ. Am J Психиатрия. 1999; 156: 891–896. [PubMed] [Google Scholar]
Am J Психиатрия. 1999; 156: 891–896. [PubMed] [Google Scholar]
65. Рубиа К., Смит А.Б., Браммер М.Дж., Тун Б., Тейлор Э. Аномальная активация мозга во время торможения и обнаружение ошибок у подростков с СДВГ, ранее не получавших лекарств. Am J Психиатрия. 2005; 162:1067–1075. [PubMed] [Академия Google]
66. Rubia K., Cubillo A., Smith A.B., Woolley J., Heyman I., Brammer M.J. Специфическая для расстройства дисфункция в правой нижней префронтальной коре во время выполнения двух задач на торможение у мальчиков с синдромом дефицита внимания с гиперактивностью по сравнению с мальчиками с обсессивно-компульсивное расстройство. Hum Brain Map. 2010; 31: 287–299. [Бесплатная статья PMC] [PubMed] [Google Scholar]
67. Рубиа К., Кубильо А., Вулли Дж., Браммер М.Дж., Смит А.Б. Специфические для расстройства дисфункции у пациентов с синдромом дефицита внимания/гиперактивности по сравнению с пациентами с обсессивно-компульсивным расстройством при интерференционном торможении и распределении внимания. Hum Brain Map. 2011;32:601–611. [Бесплатная статья PMC] [PubMed] [Google Scholar]
Hum Brain Map. 2011;32:601–611. [Бесплатная статья PMC] [PubMed] [Google Scholar]
68. Rubia K., Halari R., Cubillo A., Mohammad A., Scott S., Brammer M. Специфическая для расстройства нижняя лобная дисфункция у мальчиков с чистым синдромом дефицита внимания/гиперактивности по сравнению с мальчиками с чистым CD во время когнитивная гибкость. Hum Brain Map. 2010; 31:1823–1833. [Бесплатная статья PMC] [PubMed] [Google Scholar]
69. Balcioglu A., Ren J.Q., McCarthy D., Spencer T.J., Biederman J., Bhide P.G. Концентрации терапевтических доз метилфенидата в плазме и головном мозге и их влияние на содержание моноаминов в головном мозге у мышей. Нейрофармакология. 2009 г.;57:687–693. [Бесплатная статья PMC] [PubMed] [Google Scholar]
70. Berridge CW, Devilbiss DM, Andrzejewski ME, Arnsten AF, Kelley AE, Schmeichel B. Метилфенидат предпочтительно увеличивает нейротрансмиссию катехоламинов в префронтальной коре при низких дозах, которые улучшают когнитивную функцию. . Биол психиатрия. 2006;60:1111–1120. [PubMed] [Google Scholar]
2006;60:1111–1120. [PubMed] [Google Scholar]
71. Арнстен А., Рубиа К. Нейробиологические цепи, регулирующие внимание, движение и эмоции, и их нарушения при психоневрологических расстройствах у детей. J Am Acad Детская подростковая психиатрия. 2012; 51: 356–367. [PubMed] [Академия Google]
72. Prehn-Kristensen A., Krauel K., Hinrichs H., Fischer J., Malecki U., Schuetze H. Метилфенидат не улучшает контроль помех во время задания на рабочую память у молодых пациентов с синдромом дефицита внимания и гиперактивности. Мозг Res. 2011;1388:56–68. [PubMed] [Google Scholar]
Влияние метилфенидата на нервные системы внимания при синдроме дефицита внимания и гиперактивности. Am J Психиатрия. 2004;161:1990–1997. [PubMed] [Google Scholar]
74. Лиддл Э.Б., Холлис С., Бэтти М.Дж., Грум М.Дж., Тотман Дж.Дж., Лиотти М. Связанная с заданием модуляция сети режима по умолчанию и ингибирующий контроль при СДВГ: эффекты мотивации и метилфенидата. J Детская психологическая психиатрия. 2011;52:761–771. [Бесплатная статья PMC] [PubMed] [Google Scholar]
2011;52:761–771. [Бесплатная статья PMC] [PubMed] [Google Scholar]
75. Шеридан М.А., Хиншоу С., Д’Эспозито М. Эффективность префронтальной коры во время рабочей памяти при синдроме дефицита внимания/гиперактивности. J Am Acad Детская подростковая психиатрия. 2007; 46: 1357–1366. [PubMed] [Академия Google]
76. Конрад К., Нойфанг С., Финк Г.Р., Герперц-Дальманн Б. Долгосрочные эффекты метилфенидата на нейронные сети, связанные с исполнительным вниманием у детей с СДВГ: результаты продольного функционального МРТ исследования. J Am Acad Детская подростковая психиатрия. 2007; 46: 1633–1641. [PubMed] [Google Scholar]
77. Буш Г., Спенсер Т.Дж., Холмс Дж., Шин Л.М., Валера Э.М., Сейдман Л.Дж. Функциональная магнитно-резонансная томография метилфенидата и плацебо при синдроме дефицита внимания/гиперактивности во время исследования с несколькими источниками интерференционная задача. Арх генерал психиатрия. 2008; 65: 102–114. [PubMed] [Академия Google]
78. Frodl T. , Skokauskas N. Метаанализ структурных МРТ-исследований у детей и взрослых с синдромом дефицита внимания и гиперактивности указывает на эффективность лечения. Acta Psychiatr Scand. 2012; 125:114–126. [PubMed] [Google Scholar]
, Skokauskas N. Метаанализ структурных МРТ-исследований у детей и взрослых с синдромом дефицита внимания и гиперактивности указывает на эффективность лечения. Acta Psychiatr Scand. 2012; 125:114–126. [PubMed] [Google Scholar]
79. Castellanos F.X., Lee P.P., Sharp W., Jeffries N.O., Greenstein D.K., Clasen L.S. Траектории развития аномалий объема головного мозга у детей и подростков с синдромом дефицита внимания/гиперактивности. ДЖАМА. 2002; 288:1740–1748. [PubMed] [Академия Google]
80. Шоу П., Шарп В.С., Моррисон М., Экстранд К., Гринштейн Д.К., Класен Л.С. Психостимуляторная терапия и развивающаяся кора головного мозга при синдроме дефицита внимания с гиперактивностью. Am J Психиатрия. 2009; 166: 58–63. [Бесплатная статья PMC] [PubMed] [Google Scholar]
81. Собель Л.Дж., Бансал Р., Майя Т.В., Санчес Дж., Маццоне Л., Дуркин К. Морфология поверхности базальных ганглиев и эффекты стимулирующих препаратов у молодежи с Синдром дефицита внимания и гиперактивности. Am J Психиатрия. 2010;167:977–986. [PMC free article] [PubMed] [Google Scholar]
2010;167:977–986. [PMC free article] [PubMed] [Google Scholar]
82. Иванов И., Бансал Р., Хао X.J., Чжу Х.Т., Келлендонк С., Миллер Л. Морфологические аномалии таламуса у подростков с синдромом дефицита внимания и гиперактивности. Am J Психиатрия. 2010; 167: 397–408. [Бесплатная статья PMC] [PubMed] [Google Scholar]
83. Pliszka S.R., Lancaster J., Liotti M., Semrud-Clikeman M. Различия объемной МРТ у детей с СДВГ, ранее не получавших лечения, и детей, получавших хроническое лечение. Неврология. 2006; 67: 1023–1027. [PubMed] [Академия Google]
84. Бледсо Дж., Семруд-Кликеман М., Плишка С.Р. Магнитно-резонансная томография червя мозжечка у хронически леченных и ранее не получавших лечения детей с синдромом дефицита внимания/гиперактивности комбинированного типа. Биол психиатрия. 2009; 65: 620–624. [Бесплатная статья PMC] [PubMed] [Google Scholar]
85. Schnoebelen S., Semrud-Clikeman M., Pliszka S.R. Анатомия мозолистого тела у хронически леченных и не получавших стимуляторов СДВГ. Джей Аттен Расстройство. 2010; 14: 256–266. [PubMed] [Академия Google]
Джей Аттен Расстройство. 2010; 14: 256–266. [PubMed] [Академия Google]
86. Ван Г.Дж., Волков Н.Д., Вигал Т., Коллинз С., Ньюкорн Дж., Теланг Ф. Хроническое лечение метилфенидатом увеличивает плотность переносчиков дофамина у пациентов с гиперактивным синдромом дефицита внимания. Дж Нукл Мед. 2009;50:1283. [Google Scholar]
87. Волков Н.Д., Ван Г.-Дж., Томаси Д., Коллинз С.Х., Вигал Т.Л., Ньюкорн Дж.Х. Повышение дофамина, вызванное метилфенидатом, в вентральном полосатом теле связано с долгосрочным улучшением симптомов у взрослых с синдромом дефицита внимания и гиперактивности. Дж. Нейроски. 2012; 32:841–849. [Бесплатная статья PMC] [PubMed] [Google Scholar]
88. Шульц К.П., Фан Дж., Бедард А.-К.В., Клеркин С.М., Иванов И., Тан С.Ю. Общие и уникальные терапевтические механизмы стимулирующих и нестимулирующих методов лечения синдрома дефицита внимания/гиперактивности. Арх генерал психиатрия. 2012;69:952–961. [PubMed] [Google Scholar]
89. Ан Л., Цао С.Х., Цао К. , Сунь Л., Ян Л., Цзоу К.Х. Метилфенидат нормализует мозговую дисфункцию в состоянии покоя у мальчиков с синдромом дефицита внимания и гиперактивности. Нейропсихофармакология. 2013;38:1287–1295. [Бесплатная статья PMC] [PubMed] [Google Scholar]
, Сунь Л., Ян Л., Цзоу К.Х. Метилфенидат нормализует мозговую дисфункцию в состоянии покоя у мальчиков с синдромом дефицита внимания и гиперактивности. Нейропсихофармакология. 2013;38:1287–1295. [Бесплатная статья PMC] [PubMed] [Google Scholar]
90. Орру Г., Петтерссон-Йео В., Маркванд А.Ф., Сартори Г., Мечелли А. Использование метода опорных векторов для идентификации визуализирующих биомаркеров неврологических и психиатрических Болезнь: критический обзор. Neurosci Biobehav Rev. 2012; 36:1140–1152. [PubMed] [Google Scholar]
91. Познер Дж., Нагель Б.Дж., Майя Т.В., Мехлинг А., О М., Ван З., Петерсон Б.С. Аномальная активация и связь миндалевидного тела у подростков с синдромом дефицита внимания/гиперактивности. J Am Acad Детская подростковая психиатрия. 2011;50:828–837. е3. [Бесплатная статья PMC] [PubMed] [Google Scholar]
Изменят ли лекарства от СДВГ мозг моего ребенка?
Если у вашего ребенка диагностирован синдром дефицита внимания и гиперактивности (СДВГ), вы можете столкнуться с необходимостью принимать лекарства. Неоднократно было показано, что стимуляторы являются наиболее эффективным средством лечения симптомов СДВГ, помогая детям обращать внимание, концентрироваться, управлять своими импульсами и избегать рискованного поведения. Около 80 процентов детей, которые пробуют стимуляторы для лечения СДВГ, обнаруживают, что они оказывают положительное влияние на симптомы. Чтобы представить это в перспективе, нет другого лекарства от психического расстройства, которое имеет такой высокий уровень ответа. Но у вас могут быть опасения по поводу лекарств, влияющих на работу мозга вашего ребенка. И если лекарство принимается в течение нескольких лет, оказывает ли оно долгосрочное воздействие на мозг?
Неоднократно было показано, что стимуляторы являются наиболее эффективным средством лечения симптомов СДВГ, помогая детям обращать внимание, концентрироваться, управлять своими импульсами и избегать рискованного поведения. Около 80 процентов детей, которые пробуют стимуляторы для лечения СДВГ, обнаруживают, что они оказывают положительное влияние на симптомы. Чтобы представить это в перспективе, нет другого лекарства от психического расстройства, которое имеет такой высокий уровень ответа. Но у вас могут быть опасения по поводу лекарств, влияющих на работу мозга вашего ребенка. И если лекарство принимается в течение нескольких лет, оказывает ли оно долгосрочное воздействие на мозг?
Как действуют стимуляторы
Когда ребенок принимает стимуляторы для лечения СДВГ, они изменяют уровень химического вещества в мозге, называемого дофамином, который является нейротрансмиттером, играющим важную роль во внимании и концентрации. Когда вы принимаете риталин, аддерол или любой другой стимулирующий препарат для лечения СДВГ, это помогает повысить уровень дофамина в вашем мозгу до оптимального уровня — уровня, сравнимого с уровнем в мозге человека, у которого нет СДВГ.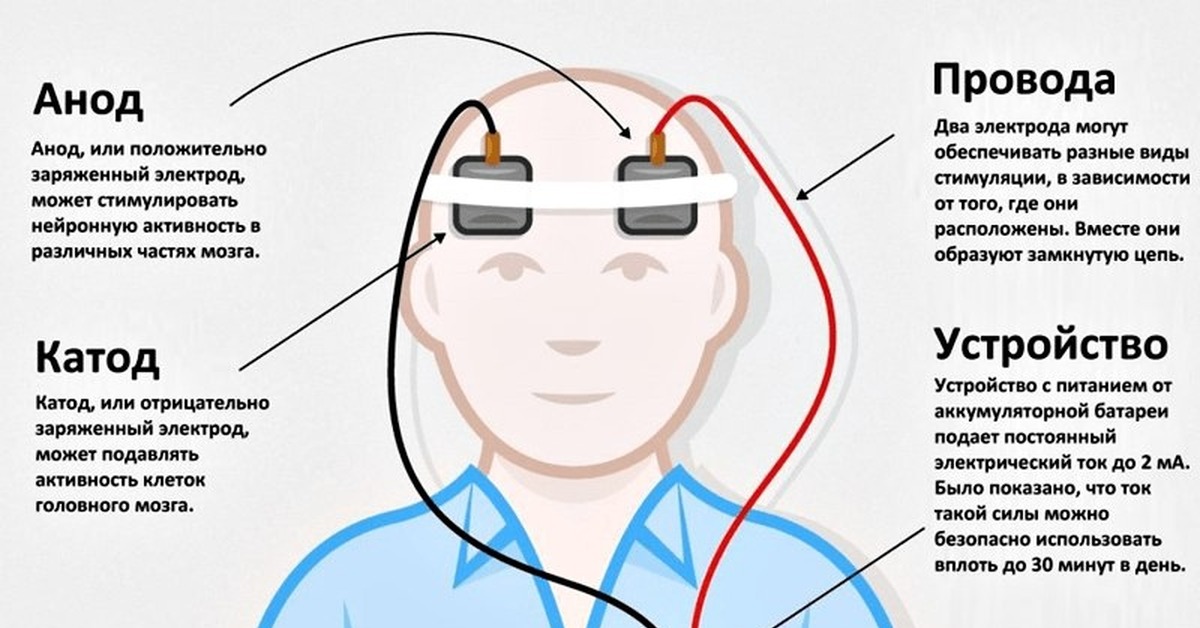 Он делает это, блокируя действие так называемого переносчика дофамина, молекулы, которая удаляет дофамин из нервных путей. Таким образом, изменение уровня дофамина в мозге определенно меняет то, как он функционирует, пока вы принимаете лекарство, и в этом весь смысл его приема. На уровне, который они назначают при СДВГ, эти лекарства не повышают уровень дофамина достаточно высоко, чтобы вызвать эйфорию, и они не считаются вызывающими привыкание.
Он делает это, блокируя действие так называемого переносчика дофамина, молекулы, которая удаляет дофамин из нервных путей. Таким образом, изменение уровня дофамина в мозге определенно меняет то, как он функционирует, пока вы принимаете лекарство, и в этом весь смысл его приема. На уровне, который они назначают при СДВГ, эти лекарства не повышают уровень дофамина достаточно высоко, чтобы вызвать эйфорию, и они не считаются вызывающими привыкание.
Изменяют ли они личность ребенка?
Лекарства от СДВГ не должны изменять личность ребенка. Если ребенок, принимающий стимулятор, кажется успокоенным или похожим на зомби, плачущим и раздражительным, это обычно означает, что доза слишком высока, и врачу необходимо скорректировать рецепт, чтобы подобрать правильную дозу. Если ребенок принимает самую низкую возможную дозу, которая эффективна для него, и все еще становится капризным или раздражительным, следует попробовать какой-либо другой вид лечения. Есть небольшая группа детей, которые реагируют таким образом, и обычно это происходит сразу же, как только они начинают принимать лекарство, и сразу же исчезает, как только они перестают его принимать.
Препараты короткого действия
Эффекты стимулирующих препаратов быстро начинаются и прекращаются, поскольку эти препараты быстро метаболизируются. Они не остаются в организме в течение длительного периода времени. Существует несколько различных составов лекарств от СДВГ, рассчитанных на действие от 4 часов (немедленное высвобождение) до 12 часов (отсроченное высвобождение). Но все они по существу вне системы ребенка, когда он просыпается утром. Любые возможные побочные эффекты, такие как потеря аппетита или проблемы со сном, также прекращаются, когда ребенок перестает принимать лекарство.
Есть ли долгосрочные последствия?
За более чем 50 лет использования стимулирующих препаратов для противодействия симптомам СДВГ и сотен исследований не наблюдалось никаких негативных последствий приема лекарств в течение нескольких лет. В последние годы Нора Волков, директор Национального института по борьбе со злоупотреблением наркотиками, и ее коллеги провели ряд визуализационных исследований, чтобы лучше понять, как СДВГ и лекарства, используемые для его лечения, влияют на мозг. В 2013 году они сравнили мозг детей с СДВГ до и после года лечения стимулирующими препаратами. Исследования показали увеличение плотности переносчиков дофамина — тех молекул, которые выводят дофамин из строя — в мозге после лечения. Это говорит о том, что увеличение дофамина, стимулированное лекарством, могло побудить мозг вырабатывать больше передатчиков дофамина, чтобы избавиться от него. Как долго это изменение может длиться, неясно, поскольку уровень транспортеров в мозгу колеблется. Но это может привести к тому, отмечают исследователи в своем заключении, что лекарство не будет работать так же хорошо, как должно было уменьшать симптомы в долгосрочной перспективе.
В 2013 году они сравнили мозг детей с СДВГ до и после года лечения стимулирующими препаратами. Исследования показали увеличение плотности переносчиков дофамина — тех молекул, которые выводят дофамин из строя — в мозге после лечения. Это говорит о том, что увеличение дофамина, стимулированное лекарством, могло побудить мозг вырабатывать больше передатчиков дофамина, чтобы избавиться от него. Как долго это изменение может длиться, неясно, поскольку уровень транспортеров в мозгу колеблется. Но это может привести к тому, отмечают исследователи в своем заключении, что лекарство не будет работать так же хорошо, как должно было уменьшать симптомы в долгосрочной перспективе.
Становится ли лекарство со временем менее эффективным?
Это предмет разногласий между клиницистами и исследователями. Для многих детей одна и та же доза (с поправкой на рост) продолжает действовать в течение многих лет. Но у других детей лекарство не работает так же хорошо после первых нескольких месяцев, и им нужно увеличить дозировку, чтобы продолжать получать те же результаты. Хотя увеличение дозы является скромным, оно является не только результатом роста детей. В крупнейшем долгосрочном исследовании лечения СДВГ под названием MTA (Исследование мультимодального лечения детей с СДВГ) первый месяц исследования был посвящен титрованию — корректировке дозы до тех пор, пока не была достигнута оптимальная доза для каждого ребенка. Но в течение следующих 13 месяцев дозировка многих детей была изменена, чтобы продолжать получать полную пользу от лекарства.8 детей, которые принимали метилфенидат в конце периода титрования, 81 (41%) доза была увеличена для поддержания эффективности. Средняя прибавка на единицу массы тела составила 12,4%. Но еще 36 (18%) уменьшили дозировку, чтобы избежать негативных побочных эффектов, и (29%) продолжали принимать ту же дозировку. Дети, которые начали с низкой дозы, скорее всего (61%), нуждались в увеличении дозы, в то время как те, кто начал с высокой дозы, скорее всего, остались на той же дозе (33%) или уменьшили дозу (37%). Остальные 24 ребенка (12%) были переведены либо на другой препарат, либо на другое лечение.
Хотя увеличение дозы является скромным, оно является не только результатом роста детей. В крупнейшем долгосрочном исследовании лечения СДВГ под названием MTA (Исследование мультимодального лечения детей с СДВГ) первый месяц исследования был посвящен титрованию — корректировке дозы до тех пор, пока не была достигнута оптимальная доза для каждого ребенка. Но в течение следующих 13 месяцев дозировка многих детей была изменена, чтобы продолжать получать полную пользу от лекарства.8 детей, которые принимали метилфенидат в конце периода титрования, 81 (41%) доза была увеличена для поддержания эффективности. Средняя прибавка на единицу массы тела составила 12,4%. Но еще 36 (18%) уменьшили дозировку, чтобы избежать негативных побочных эффектов, и (29%) продолжали принимать ту же дозировку. Дети, которые начали с низкой дозы, скорее всего (61%), нуждались в увеличении дозы, в то время как те, кто начал с высокой дозы, скорее всего, остались на той же дозе (33%) или уменьшили дозу (37%). Остальные 24 ребенка (12%) были переведены либо на другой препарат, либо на другое лечение.
Разные исследователи интерпретируют эти данные по-разному, одни видят доказательства того, что у детей развилась толерантность к лекарству, другие нет. Автор исследования 2001 года, Бенедетто Витиелло, доктор медицинских наук, написал: «Эти данные не предполагают толерантности к терапевтическим эффектам MPH». Он добавил, что тот факт, что в течение 13-месячного периода происходила смена лекарств, указывает на «необходимость длительного непрерывного наблюдения». Это отражает опыт многих клиницистов.
Рой Буради, доктор медицинских наук, детский и подростковый психиатр в Институте детского разума, говорит, что часто увеличивает дозировку в течение первых нескольких лет лечения ребенка. «Когда я лечу ребенка, скажем, с семилетнего возраста, я обнаруживаю, что мне нужно увеличить дозу, может быть, на 20%, чтобы вернуть положительный эффект. Но после 15 или 16 лет я обнаружил, что детям нужно меньше, а не больше». Доктор Буради отмечает, что это может быть результатом ослабления симптомов СДВГ, как это часто бывает, в позднем подростковом возрасте, а также того, что по мере созревания печени подростков они могут более эффективно метаболизировать лекарство.
Но не все клиницисты сообщают об одном и том же эффекте, и некоторые отмечают, что могут быть и другие причины увеличения дозы с годами, не подразумевающие толерантности: По мере взросления ребенок сталкивается с повышенными ожиданиями в школе, более высокой потребностью в концентрации . Ребенок лучше понимает, что делает лекарство, и может хотеть больше этого ощущения. «Вполне вероятно, что со временем толерантность развивается очень медленно, — говорит Стивен Хиншоу, доктор философии, один из авторов исследования MTA. — Мы просто не знаем. Доктор Хиншоу, профессор психологии Калифорнийского университета в Беркли, отмечает, что иногда после многих лет эффективного лечения пациенту с СДВГ необходимо перейти на лекарство на основе другого стимулятора, скажем, с Концерты на Аддерол, чтобы поддерживать эффект.
Приводят ли лекарства от СДВГ к зависимости?
Большую озабоченность по поводу лекарств от СДВГ вызывает опасение, что дети, которые их принимают, будут подвергаться более высокому риску злоупотребления психоактивными веществами, когда станут старше. Но несколько исследований не показали никакой корреляции. Самые последние исследования показали, что хотя подростки и молодые люди с СДВГ подвержены более высокому риску злоупотребления психоактивными веществами, чем другие дети, лечение их стимулирующими препаратами не увеличивает и не снижает риск. Новое исследование показывает, что риск связан с расстройством, а не с лечением. Национальный институт по борьбе со злоупотреблением наркотиками отмечает, что зависимость представляет собой риск, когда этими стимуляторами злоупотребляют, т. е. принимают в дозах и способами, отличными от предписанных (т. е. их измельчают, вдыхают или вводят инъекционно). Затем они производят эйфорию и, как следствие, повышают риск привыкания. Следовательно, история злоупотребления психоактивными веществами будет важным фактором при рассмотрении вопроса о том, является ли подросток хорошим кандидатом на лечение СДВГ.
Но несколько исследований не показали никакой корреляции. Самые последние исследования показали, что хотя подростки и молодые люди с СДВГ подвержены более высокому риску злоупотребления психоактивными веществами, чем другие дети, лечение их стимулирующими препаратами не увеличивает и не снижает риск. Новое исследование показывает, что риск связан с расстройством, а не с лечением. Национальный институт по борьбе со злоупотреблением наркотиками отмечает, что зависимость представляет собой риск, когда этими стимуляторами злоупотребляют, т. е. принимают в дозах и способами, отличными от предписанных (т. е. их измельчают, вдыхают или вводят инъекционно). Затем они производят эйфорию и, как следствие, повышают риск привыкания. Следовательно, история злоупотребления психоактивными веществами будет важным фактором при рассмотрении вопроса о том, является ли подросток хорошим кандидатом на лечение СДВГ.
Часто задаваемые вопросы
Как действуют лекарства от СДВГ? Лекарства от СДВГ, такие как Adderall и Ritalin, работают, повышая уровень дофамина в мозге до уровня, который был бы у человека без СДВГ.

