128.Стероидные и нестероидные анаболические средства.
АHАБОЛИЧЕСКИЕ СТЕРОИДЫ
(на основе андрогенов. Андрогены к анаболическому эффекту дают еще и другие эффекты, а у анаболиков их мало).
Феноболин, ретаболил (инъекционный маслянный раствор в/м), метандростенолон (в рот в таблетках).
Механизмы: 1). Повышают синтез ДHК, РHК, структурных белков и ферментов.
2). Активируется система цитохромов
3). Повышается синтез СТГ в передней доли гипофиза
4). Процесс биосинтеза преобладает над распадом
5). Задержка N,P,S в организме
6). Повышение массы тела за счет скелетной мускулатуры.
Развитие эффекта через 1-2 дня. Длительность действия
2 нед для феноболина, 3 нед для ретаболила.
Применение: истощение, кахексия
(туберкулез), тяжелые травмы, операции
и ожоги, плохо срастающиеся переломы,
после цитостатиков, при длительном
применении глюкокортикоидов.
NB! Понижают эффекты ГК — может быть обострение основного заболевания. Хорошо сочетать с минеральными и витаминными добавками, белково-аминокислотными смесями.
Противопоказания: рак простаты, простатит, беременность, лактация, печеночная недостаточность.
Применяются с немедицинскими целями в бодибилдинге, однако вызывают в данном случае к 30 годам жизни смертельный исход
в результате перераспределения белков, миокардиодистрофии,
печеночной недостаточности, импотенции.
ЭСТРОГЕHЫ
Синтезируются в яичниках (эстрадиол) путем ароматозной реакции из андрогенов. В плаценте — эстриол. Hебольшое количество в надпочечниках (из андрогенов).
1). Стероидного строения: эстрон, эстрадиоло-дипропионат, этинилэстрадиол
2). Hестероидные вещества с эстрогенной активностью (влияют на рецепторы): синестрол
Механизм: 1). Повышение чувствительность
к окситоцину
Повышение чувствительность
к окситоцину
2). В матке — усиление развития, пролиферация эндометрия, маточной трубы и влагалища
3). Гипохолестеринемическое действие — у женщин до менопаузы уровень холестерина меньше, чем у мужчин, поэтому ниже и уровень атеросклероза.
Применение: недоразвитие матки и молочных желез, нарушение менструаций, после удаления яичников, подавление лактации, слаюость родовой деятельности, перенашивание беременности, угревидная сыпь (местно)., опухоль простаты.
Побочные явления: феминизация у мужчин
Противопоказания: беременность, опухоли женских половых органов, молочных желез, мастопатия, воспалительные заболевания женских половых органов, склонность к маточным кровотечениям.
КЛАССИФИКАЦИЯ.
Средства, влияющие на эритропоэз.
Средства, стимулирующие эритропоэз
1. Применяемые при гипохромной анемии
А. При железодефицитной анемии
При железодефицитной анемии
а) Препараты железа: Железа закисного сульфат Феррум Лек Ферковен
б) Препараты кобальта: Коамид
Б. При анемии, возникающей при некоторых хронических заболеваниях: Эпоэтин альфа
2. Применяемые при гиперхромнои анемии: Цианокобаламин Кислота фолиевая
Средства, угнетающие эритропоэз: Раствор натрия фосфата, меченного фосфором-32
Средства, влияющие на лейкопоэз
Средства, стимулирующие лейкопоэз:Натрия нуклеинат Пентоксил Молграмостим Филграстим
Средства, угнетающие лейкопоэз
: Новэмбихин Миелосан Меркаптопурин Допан ТиофосфамидСРЕДСТВА, ВЛИЯЮЩИЕ НА ЭРИТРОПОЭЗ
Из стимуляторов эритропоэза, применяемых при гипохромной анемии, основную роль играют препараты железа.
Железо содержится в организме в количестве
2—5 г. Основная его часть (2/3) входит в
состав гемоглобина. Остальная часть
находится в тканевых депо (в костном
мозге, печени, селезенке). Железо входит
также в состав миоглобина и ряда
ферментов.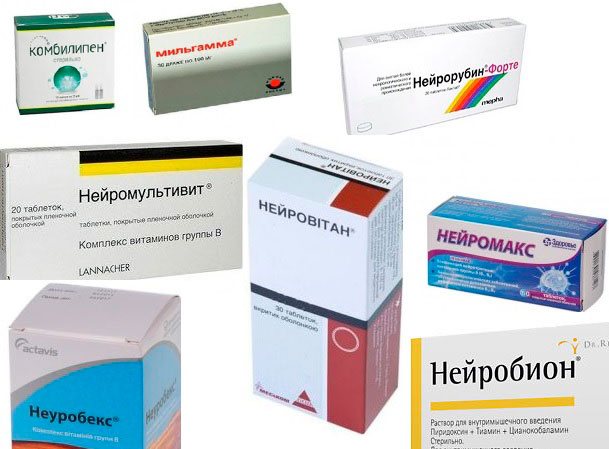
Фармококинетика:Из желудочно-кишечного тракта всасывается только ионизированное железо, причем лучше всего в виде двухвалентного иона (схема 18.1). В связи с этим наличие хлористоводородной кислоты (переводит молекулярное железо в ионизированную форму) и аскорбиновой кислоты (восстанавливает трехвалентное железо в двухвалентное) способствует всасыванию железа из пищеварительного тракта.
Выводится железо пищеварительным трактом (невсосавшаяся часть; с эпителием слизистой оболочки, который подвергается десквамации; с желчью), почками и потовыми железами.
При железодифицитной гипохромной анемии – железа закисного сульфат.
При гипохромной – препараты кобальта.
При гиперхромной – цианокобаламин и кислоту фолиевую.
Цианокобаламин (витамин В]2) назначают при злокачественной (пернициозной) анемии.
При дефиците цианокобаламина эритропоэз протекает по мегалобластическому типу: эритробласт -» гиперхромный мегалобласт —> мегалоцит.
Возникновение пернициозной анемии
связано с нарушением всасывания
цианокобаламина, поскольку у таких
больных отсутствует внутренний фактор
Касла (по химической структуре —
гликопротеин). В обычных условиях он
вырабатывается слизистой оболочкой
желудка и обеспечивает всасывание
цианокобаламина в тонкой кишке.
В обычных условиях он
вырабатывается слизистой оболочкой
желудка и обеспечивает всасывание
цианокобаламина в тонкой кишке.
Цианокобаламин при злокачественной анемии нормализует картину крови, а также устраняет или ослабляет неврологические нарушения и поражения слизистой оболочки языка. Ахлоргидрия желудочного сока сохраняется.
Кислоту фолиевую(витамин Вс) назначают при макроцитарной анемии.
При дефиците кислоты фолиевой образуются макроциты: эритробласт -> гиперхромный макронормобласт —» макроцит. В организме кислота фолиевая превращается в фолиниевую, которая и обладает физиологической активностью.
СРЕДСТВА, ВЛИЯЮЩИЕ НА ЛЕЙКОПОЭЗ.
Натрия нуклеинат— это натриевая соль нуклеиновой кислоты, получаемое из дрожжей. Применяют для стимуляции образования костным мозгом лейкоцитов. Вводят внутрь и внутримышечно.
Пентоксил. Стимулирует лейкопоэз,
ускорягг заживление ран, обладает
противовоспалительным эффектом.
Принимают ere внутрь.
Факторы роста, регулирующие лейкопоэз: рекомбинантный человеческий гранулоцитарно-макрофагальный колоние-стимулирующий фактор (GM-CSF)— молграмостим (лейкомакс).
Он является гликопротеином. Образуется в Т-лимфоцитах, -йлотелиальных клетках, фибробластах, макрофагах. Стимулирует пролиферацию, дифференцировку и функцию гранулоцитов и моноцитов/макрофагов
Показания:при угнетении лейкопоэза, связанном с химиотерапией опухолей, при миелодиспластическом синдроме, апластической анемии, лейкопении. вызванной различными инфекциями, при пересадке костного мозга, в комплексной терапии СПИДа. Вводят внутривенно.
Возможные побочные эффекты: тошнота, рвота, анорексия, диарея, гипертермия. кожные высыпания и другие аллергические реакции, мышечно-скелетные боли и пр.
Рекомбинантный человеческий гранулоцитарный колоние-стимулирующий фактор (G-CSF
). — филграстим (нейпоген). Он является гликопротеином. Продуцируется
моноцитами, фибробластами и клетками
эндотелия. Стимулирует пролиферацию и
дифферен-дировку предшественников
гранулоцитов и активность (хемотаксическую
и фагоцитарную) зрелых гранулоцитов
(нейтрофилов).
Продуцируется
моноцитами, фибробластами и клетками
эндотелия. Стимулирует пролиферацию и
дифферен-дировку предшественников
гранулоцитов и активность (хемотаксическую
и фагоцитарную) зрелых гранулоцитов
(нейтрофилов).Показания:при угнетении лейкопоэза, связанном с химиотерапией опухолей, при миелодиспластическом синдроме, апластической анемии, лейкопении. вызванной различными инфекциями, при пересадке костного мозга, в комплексной терапии СПИДа. Вводят препарат внутривенно и подкожно.
Показания:при лейкозах и лимфогранулематозе.
Отдельные группы лекарственных средств, прием которых ассоциирован с развитием лекарственно-индуцированной фибрилляции предсердий | Остроумова
1. Hindricks G., Potpara T., Dagres N., et al. 2020 ESC Guidelines for the diagnosis and management of atrial fibrillation developed in collaboration with the European Association of Cardio-Thoracic Surgery (EACTS). European heart journal. 2020; 612. https://doi.org/10.1093/eurheartj/ehaa612.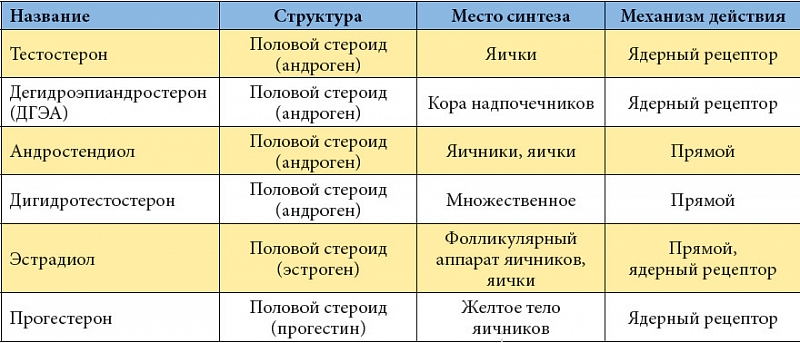
2. van der Hooft C.S., Heeringa J., van Herpen G., et al. Drug-induced atrial fibrillation. Journal of the American College of Cardiology. 2004; 44 (11): 2117-24. https://doi.org/10.1016/j.jacc.2004.08.053.
3. Kaakeh Y., Overholser B. R., Lopshire J. C., Tisdale J. E. Drug-induced atrial fibrillation. Drugs. 2012; 72 (12): 1617-30. https://doi.org/10.2165/11633140-000000000-00000.
4. Tamargo J., Caballero R., Delpón E. Drug-induced atrial fibrillation. Expert opinion on drug safety. 2012; 11 (4): 615-34. https://doi.org/10.1517/14740338.2012.698609.
5. Tisdale J. E., Miller D. A. Drug Induced Diseases: Prevention, Detection, and Management. 3rd ed. Bethesda, Md.: American Society of Health-System Pharmacists; 2018.
6. Остроумова О.Д., Черняева М.С., Комарова А.Г., и другие. Лекарственно-индуцированная фибрилляция предсердий, ассоциированная с приемом сердечно-сосудистых лекарственных средств. Сибирское медицинское обозрение. 2020; (6): 5-13. https://doi.org/10. 20333/2500136-2020-6-5-13. Ostroumova O.D., Cherniaeva M.S., Komarova A.G., et al. Drug-induced atrial fibrillation associated with admission of cardiovascular medications. Siberian Medical Review. 2020; (6): 5-13. https://doi.org/10.20333/2500136-2020-6-5-13
20333/2500136-2020-6-5-13. Ostroumova O.D., Cherniaeva M.S., Komarova A.G., et al. Drug-induced atrial fibrillation associated with admission of cardiovascular medications. Siberian Medical Review. 2020; (6): 5-13. https://doi.org/10.20333/2500136-2020-6-5-13
7. Остроумова О. Д., Черняева М. С., Кочетков А. И., и другие. Лекарственно-индуцированная фибрилляция предсердий, ассоциированная с применением противоопухолевых лекарственных средств. Безопасность и риск фармакотерапии. 2020; 8 (4): 178-190. https://doi.org/10.30895/2312-7821- 2020-8-4-178-190. Ostroumova O.D., Chernyaeva M.S., Kochetkov A.I., et al. Atrial fibrillation associated with anticancer drugs. Safety and Risk of Pharmacotherapy. 2020; 8 (4): 178-190. https://doi.org/10.30895/2312-7821-2020-8-4-178-190
8. Black D.M., Delmas P.D., Eastell R., et al. Once-yearly zoledronic acid for treatment of postmenopausal osteoporosis. The New England journal of medicine. 2007; 356: 1809-22. https://doi.org/10.1056/NEJMoa067312.
9. Lyles K.W., Colon-Emeric C.S., Magaziner J.S., et al. Zoledronic acid and clinical fractures and mortality after hip fracture. The New England journal of medicine. 2007; 357 (18): 1799-809. https://doi.org/10.1056/NEJMoa074941.
10. Black D.M., Reiss T.F., Nevitt M.C., et al. Design of the Fracture Intervention Trial. Osteoporosis international: a journal established as result of cooperation between the European Foundation for Osteoporosis and the National Osteoporosis Foundation of the USA. 1993; 3 (3): S29-S39. https://doi.org/10.1007/BF01623005.
11. Cummings S.R., Schwartz A.V., Black D.M. Alendronate and atrial fibrillation. The New England journal of medicine. 2007; 356 (18): 1895-6. https://doi.org/10.1056/NEJMc076132.
12. Karam R., Camm J., McClung M. Yearly zoledronic acid in postmenopausal osteoporosis. The New England journal of medicine. 2007; 357: 712-3.
13. http://www.fda.gov/Drugs/DrugSafety/PostmarketDrugSafetyInformationforPtientsandProviders/DrugSafetyInformationHeathcareProfessionals/ucm136201. htm (accessed 2017 Now 3)
htm (accessed 2017 Now 3)
14. Grosso A., Douglas I., Hingorani A., et al. Oral Bisphosphonates and Risk of Atrial Fibrillation and Flutter in Women: A Self-Controlled Case-Series Safety Analysis. PLoSOne. 2009; 4 (3): e4720. https://doi.org/10.1371/journal.pone.0004720.
15. Abrahamsen B., Eiken P., Brixen K. Atrial Fibrillation in Fracture Patients Treated with Oral Bisphosphonates. Journal of internal medicine. 2009; 265 (5): 581-92. https://doi.org/10.1111/j.1365-2796.2008.02065.x.
16. Erichsen R.1, Christiansen C.F., Frøslev T., et al. Intravenous Bisphosphonate Therapy and Atrial Fibrillation/Flutter Risk in Cancer Patients: A Nationwide Cohort Study. British journal of cancer. 2011; 105 (7): 881-3. https://doi.org/10.1038/bjc.2011.338.
17. Gregg S., Wilkinson I., Baillargeon J., et al. Atrial Fibrillation and Stroke Associated with Intravenous Bisphosphonate Therapy in Older Patients with Cancer. Journal of clinical oncology: official journal of the American Society of Clinical Oncology. 2010; 28 (33): 4898-905. https://doi.org/10.1200/JCO.2010.28.7524.
2010; 28 (33): 4898-905. https://doi.org/10.1200/JCO.2010.28.7524.
18. Herrera L., Leal I., Lapi F., et al. Risk of Atrial Fibrillation Among Bisphosphonate Users: A Multicenter, Population-Based, Italian Study. Osteoporosis international: a journal established as result of cooperation between the European Foundation for Osteoporosis and the National Osteoporosis Foundation of the USA. 2015; 26 (5): 1499-506. https://doi.org/10.1007/s00198-014-3020-y.
19. Yoon Kong Loke, Jeevanantham V., Singh S. Bisphosphonates and Atrial Fibrillation: Systematic Review and Meta-Analysis. Drug Safety. 2009; 32 (3): 219-28. https://doi.org/10.2165/00002018-200932030-00004.
20. Bhuriya R., Singh M., Molnar J., et al. Bisphosphonate Use in Women and the Risk of Atrial Fibrillation: A Systematic Review and Meta-Analysis. International journal of cardiology. 2010; 142 (3): 213-7. https://doi.org/10.1016/j.ijcard.2009.11.041.
21. Sharma A., Chatterjee S., Arbab-Zadeh A., et al. Risk of Serious Atrial Fibrillation and Stroke with Use of Bisphosphonates: Evidence from a Meta-Analysis. Chest. 2013; 144 (4): 1311-22. https://doi.org/10.1378/chest.13-0675.
Chest. 2013; 144 (4): 1311-22. https://doi.org/10.1378/chest.13-0675.
22. Sharma A., Einstein A.J., Vallakati A. Risk of Atrial Fibrillation with Use of Oral and Intravenous Bisphosphonates. The American journal of cardiology. 2014; 113 (11): 1815-21. https://doi.org/10.1016/j.amjcard.2014.03.008.
23. Kim D.H., Rogers J.R., Fulchino L.A., et al. Bisphosphonates and Risk of Cardiovascular Events: A Meta-Analysis. PLoS One. 2015; 10 (4): e0122646. https://doi.org/10.1371/journal.pone.0122646.
24. Cummings S.R., Schwartz A.V., Black D.M. Alendronate and Atrial Fibrillation. The New England journal of medicine. 2007; 356 (18): 1895-6. https://doi.org/10.1056/NEJMc076132.
25. Hewitt R. E., Lissina A., Green A. E., et al. The Bisphosphonate Acute Phase Response: Rapid and Copious Production of Proinflammatory Cytokines by Peripheral Blood Gd T Cells in Response to Aminobisphosphonates Is Inhibited by Statins. Clinical and experimental immunology. 2005; 139 (1): 101-11. https://doi.org/10.1111/j.1365-2249.2005.02665.x.
https://doi.org/10.1111/j.1365-2249.2005.02665.x.
26. Aviles R.J., Martin D.O., Apperson-Hansen C., et al. Inflammation as a Risk Factor for Atrial Fibrillation. Circulation. 2003; 108 (24): 3006-10. https://doi.org/10.1161/01.CIR.0000103131.70301.4F.
27. Tisdale J. E., Allen M. R., Overholser B.R., et al. Influence of Zoledronic Acid on Atrial Electrophysiological Parameters and Electrocardiographic Measurements. Journal of cardiovascular electrophysiology. 2015; 26 (6): 671-7. https://doi.org/10.1111/jce.12641
28. McLuckie A.E., Savage R. W. Atrial fibrillation following pulse methylprednisolone therapy in an adult. Chest. 1993; 104: 622-3. https://doi.org/10.1378/chest.104.2.622.
29. Moretti R., Torre P., Antonello R.M., et al Recurrent atrial fibrillation associated with pulse administration of high doses of methylprednysolone: a possible prophylactic treatment. European journal of neurology. 2000; 7: 130. https://doi.org/10.1046/j.1468-1331.2000.00026.x.
30. Ueda N., Yoshikawa T., Chihara M., et al. Atrial fibrillation following methylprednisolone pulse therapy. Pediatric Nephrology. 1988; 2: 29-31. https://doi.org/10.1007/BF00870376.
Ueda N., Yoshikawa T., Chihara M., et al. Atrial fibrillation following methylprednisolone pulse therapy. Pediatric Nephrology. 1988; 2: 29-31. https://doi.org/10.1007/BF00870376.
31. Yamamura K., Ohga S., Nishiyama K., et al. Recurrent atrial fibrillation after high- dose methylprednisolone therapy in a girl with lupus-associated hemophagocytic syndrome. Lupus. 2011; 20: 871-5. https://doi.org/10.1177/0961203310392429.
32. Aslam A.K., Vasavada B.C., Sacchi T.J., Khan I.A. Atrial fibrillation associated with systemic lupus erythematosus and use of methylprednisolone. American journal of therapeutics. 2001; 8: 303-5. https://doi.org/10.1097/00045391-200107000-00013.
33. Dogukan A., Ilkay E., Poyrazoglu O.K., et al. Atrial fibrillation due to oral methylprednisolone in a patient with membranoproliferative glomerulonephritis. Acta Medica (Hradec Kralove). 2008; 51: 63-4. https://doi.org/10.14712/18059694.2017.34.
34. Iqbal F.M., Beeharilal P.S., Sadat K., et al. Steroid induced atrial fibrillation. Comprehensive therapy. 2008; 34: 111-4.
Comprehensive therapy. 2008; 34: 111-4.
35. van der Hooft C.S., Heeringa J., Brusselle G.G., et al. Corticosteroids and the risk of atrial fibrillation. Archives of internal medicine. 2006; 166: 1016-20. https://doi.org/10.1001/archinte.166.9.1016.
36. De C.R., Ruigomez A., Rodriguez LA. Long-term use of anti-inflammatory drugs and risk of atrial fibrillation. Archives of internal medicine. 2010; 170: 1450-5. https://doi.org/10.1001/archinternmed.2010.305.
37. Oteri A., Bussolini A., Sacchi M., et al. A case of atrial fibrillation induced by inhaled fluticasone propionate. Pediatrics. 2010; 126 (5): e1237-41. https://doi.org/10.1542/peds.2010-0419. Epub 2010 Oct 18.
38. Baker W. L., White C. M. Post-cardiothoracic surgery atrial fibrillation: a review of preventive strategies. The Annals of pharmacotherapy. 2007; 41: 587-98. https://doi.org/10.1345/aph.1H594.
39. Halonen J., Halonen P., Jarvinen O., et al. Corticosteroids for the prevention of atrial fibrillation after cardiac surgery: a randomized controlled trial. JAMA. 2007; 297: 1562-7 https://doi.org/10.1001/jama.297.14.1562.
JAMA. 2007; 297: 1562-7 https://doi.org/10.1001/jama.297.14.1562.
40. Marik P.E., Fromm R. The efficacy and dosage effect of corticosteroids for the prevention of atrial fibrillation after cardiac surgery: a systematic review. Journal of critical care. 2009; 24: 458-63. https://doi.org/10.1016/j.jcrc.2008.10.016.
41. Prasongsukarn K., Abel J. G., Jamieson W. R., et al. The effects of steroids on the occurrence of postoperative atrial fibrillation after coronary artery bypass grafting surgery: a prospective randomized trial. The Journal of thoracic and cardiovascular surgery. 2005; 130: 93-8. https://doi.org/10.1016/j.jtcvs.2004.09.014.
42. Shiroshita-Takeshita A., Brundel B.J., Lavoie J., et al. Prednisone prevents atrial fibrillation promotion by atrial tachycardia remodeling in dogs. Cardiovascular research. 2006; 69: 865-75. https://doi.org/10.1016/j.cardiores.2005.11.028.
43. Fujimoto S., Kondoh H., Yamamoto Y., et al. Holter electrocardiogram monitoring in nephrotic patients during methylprednisolone pulse therapy. American journal of nephrology. 1990; 10: 231-6. https://doi.org/10.1159/000168087.
American journal of nephrology. 1990; 10: 231-6. https://doi.org/10.1159/000168087.
44. Ozen S., Tokgozoglu L., Saatci U. Are late potentials operative in arrhythmias following methylprednisolone pulse therapy. International journal of cardiology. 1992; 36: 234-5. https://doi.org/10.1016/0167-5273(92)90014-t.
45. Schmidt M., Christiansen C.F., Mehnert F., et al. Non-steroidal Anti-Inflammatory Drug Use and Risk of Atrial Fibrillation or Flutter: Population Based Case-Control Study. BMJ. 2011; 343: d3450. https://doi.org/10.1136/bmj.d3450.
46. Liu G., Yan Y., Zheng X., et al. Meta-analysis of Nonsteroidal Anti-Inflammatory Drug Use and Risk of Atrial Fibrillation. The American journal of cardiology. 2014; 114 (10): 1523-9. https://doi.org/10.1016/j.amjcard.2014.08.015.
47. 47.De Caterina R., Ruigómez A., Rodríguez L.A. Long-term use of anti-inflammatory drugs and risk of atrial fibrillation. Archives of internal medicine. 2010; 170: 1450e-1455. https://doi.org/10. 1001/archinternmed.2010.305.
1001/archinternmed.2010.305.
48. Chao T.F., Liu C.J., Chen S.J., et al. The association between the use of non-steroidal anti-inflammatory drugs and atrial fibrillation: a nationwide case-control study. International journal of cardiology. 2013; 168: 312e-316. https://doi.org/10.1016/j.ijcard.2012.09.058.
49. Bäck M., Yin L., Ingelsson E. Cyclooxygenase-2 inhibitors and cardiovascular risk in a nation-wide cohort study after the withdrawal of rofecoxib. European heart journal. 2012; 33: c1928-e1933. https://doi.org/10.1093/eurheartj/ehr421.
50. Krijthe B.P., Heeringa J., Hofman A., et al. Non-steroidal anti-inflammatory drugs and the risk of atrial fibrillation: a population-based follow-up study. BMJ Open 2014; 4: e004059. https://doi.org/10.1136/bmjopen-2013-004059.
51. Chuang S., Hsu P., Lin F., et al Association Between Nonsteroidal Anti-Inflammatory Drugs and Atrial Fibrillation Among a Middle-Aged Population: A Nationwide Population-Based Cohort. British journal of clinical pharmacology. 2018; 84 (6): 1290-1300. https://doi.org/10.1111/bcp.13558.
2018; 84 (6): 1290-1300. https://doi.org/10.1111/bcp.13558.
52. Cassinotti A., Massari A., Ferrara E., et al. New onset of atrial fibrillation after introduction of azathioprine in ulcerative colitis: case report and review of the literature. European journal of clinical pharmacology. 2007; 63: 875-8. https://doi.org/10.1007/s00228-007-0328-y.
53. Riccioni G., Bucciarelli V., Di Ilio E., et al. Recurrent atrial fibrillation in a patient with ulcerative colitis treated with azathioprine: case report and review of the literature. International journal of immunopathology and pharmacology. 2011; 24 (1): 247-9. https://doi.org/10.1177/039463201102400131.
54. Dodd H. J., Tatnall F. M., Sarkany I. Fast atrial fibrillation induced by treatment of psoriasis with azathioprine. British medical journal. 1985; 291: 706. https://doi.org/10.1136/bmj.291.6497.706.
55. Murphy G., Fulton R.A., Keegan D.A.J. Fast atrial fibrillation induced by azathioprine. British medical journal. 1985; 291 (6501): 1049. https://doi.org/10.1136/bmj.291.6501.1049.
1985; 291 (6501): 1049. https://doi.org/10.1136/bmj.291.6501.1049.
56. Wooten M.D., Reddy G.V., Johnson R.D. Atrial fibrillation occurring in a patient taking etanercept plus methotrexate for rheumatoid arthritis. Delaware medical journal. 2000; 72: 517-19.
57. Paolicelli D., Manni A., Direnzo V., et al. Long-term Cardiac Safety and Tolerability of Fingolimod in Multiple Sclerosis: A Postmarketing Study. Journal of clinical pharmacology. 2015; 55 (10): 1131-6. https://doi.org/10.1002/jcph.519.
58. Rolf L., Muris A., Damoiseaux J, et al. Paroxysmal atrial fibrillation after initiation of fingolimod for multiple sclerosis treatment. Neurology. 2014; 82 (11): 1008-9. https://doi.org/10.1212/WNL.0000000000000218.
59. Wallemacq P.E., Lesne M.L. Accidental massive IV administration of cyclosporine in man. Drug intelligence and clinical pharmacy. 1985; 19 (1): 29-30. https://doi.org/10.1177/106002808501900106.
60. LoVecchio F.A., Goltz H. R. Atrial fibrillation following acute overdose with oral cyclosporine. The Annals of pharmacotherapy. 2000; 34: 405. https://doi.org/10.1345/aph.19134.
The Annals of pharmacotherapy. 2000; 34: 405. https://doi.org/10.1345/aph.19134.
61. Hayashi K., Minezaki K.K., Narukawa M., et al. Atrial fibrillation and continuous 161. hypotension induced by sildenafil in an intermittent WPW syndrome patient. Japanese heart journal. 1999; 40: 827-30. https://doi.org/10.1536/jhj.40.827.
62. Awan G. M., Calderon E., Dawood G., Alpert M.A. Acute, symptomatic atrial fibrillation after sildenafil citrate therapy in a patient with hypertrophic obstructive cardiomyopathy. The American journal of the medical sciences. 2000; 320 (1): 69-71. https://doi.org/10.1097/00000441-200007000-00011.
63. Veloso H.H., de Paola A.A.V. Atrial fibrillation after vardenafil therapy. Emergency medicine journal: EMJ. 2005; 22: 823. https://doi.org/10.1136/emj.2004.015982.
64. Varkey S. Overdose of yohimbine. BMJ 1992; 304: 548. https://doi.org/10.1136/bmj.304.6826.548-a.
65. Frederiksen M.C., Toig R.M., Depp R. III. Atrial fibrillation during hexoprenaline therapy for premature labor. American journal of obstetrics and gynecology. 1983; 145: 108-9. https://doi.org/10.1016/0002-9378(83)90350-2.
American journal of obstetrics and gynecology. 1983; 145: 108-9. https://doi.org/10.1016/0002-9378(83)90350-2.
66. Pratila M.G., Pratilas V. Dysrhythmia occurring during epidural anesthesia with bupivacaine. The Mount Sinai journal of medicine, New York. 1982; 49: 130-2.
67. Ifran A., Kaptan K., Beyan C. High-dose cyclophosphamide and MESNA infusion can cause acute atrial fibrillation. American journal of hematology. 2005; 80: 247. https://doi.org/10.1002/ajh.20441.
68. Lau D.H., Stiles M.K., John B., et al. Atrial fibrillation and anabolic steroid abuse. International journal of cardiology. 2007; 117: e86-7. https://doi.org/10.1016/j.ijcard.2006.11.199.
69. Sullivan M.L., Martinez C.M., Gallagher E.J. Atrial fibrillation and anabolic steroids. The Journal of emergency medicine. 1999; 17: 851-7. https://doi.org/10.1016/s0736-4679(99)00095-5.
70. Choragudi N. L., Aronow W. S., DeLuca A. J. Nicotine gum-induced atrial fibrillation. Heart disease. 2003; 5: 100-1. https://doi.org/1010.1097/01.hdx.0000061700.11321.1a.
https://doi.org/1010.1097/01.hdx.0000061700.11321.1a.
71. Stewart P.M., Catterall J.R. Chronic nicotine ingestion and atrial fibrillation. British heart journal. 1985; 54: 222-3. https://doi.org/10.1136/hrt.54.2.222.
72. Rigotti N. A., Eagle K. A. Atrial fibrillation while chewing nicotine gum. JAMA 1986; 255: 1018.
73. Chou T.M., Benowitz N.L. Caffeine and coffee: effects on health and cardiovascular disease. Comparative biochemistry and physiology. Part C, Pharmacology, toxicology & endocrinology. 1994; 109 (2): 173-89.
74. Frost L., Vestergaard P. Caffeine and risk of atrial fibrillation or flutter: the Danish Diet, Cancer, and Health Study. The American journal of clinical nutrition. 2005; 81 (3): 578-82. https://doi.org/10.1093/ajcn/81.3.578.
75. Patanè S., Marte F., La Rosa F.C., Rocca R. Atrial Fibrillation Associated with Chocolate Intake Abuse and Chronic Salbutamol Inhalation Abuse. International journal of cardiology. 2010; 145 (2): e74-e76. https://doi.org/10.1016/j.ijcard.2008.12.159
https://doi.org/10.1016/j.ijcard.2008.12.159
76. Artin B.1., Singh M., Riche Ch., et al. Caffeine-related Atrial Fibrillation. American journal of therapeutics. 2010; 17 (5): e169-71. https://doi.org/10.1097/MJT.0b013e3181df8cf8].
77. Jennifer R., Di Rocco 1, During A., et al. Atrial Fibrillation in Healthy Adolescents After Highly Caffeinated Beverage Consumption: Two Case Reports. Journal of medical case reports. 2011; 5: 18. https://doi.org/10.1186/1752-1947-5-18.
78. Mattioli A.V., Pennella S., Manenti A., Farinetti A. Energy Drink Overconsumption Can Trigger Atrial Fibrillation. Journal of cardiovascular medicine. 2016; 17 (12): 902-904. https://doi.org/10.2459/JCM.0000000000000416.
79. Armstrong M. Atrial Fibrillation with Rapid Ventricular Response Following Use of Dietary Supplement Containing 1,3 Dimethylamylamine and Caffeine. Journal of special operations medicine: a peer reviewed journal for SOF medical professionals. 2012; 12 (4): 1-4.
80. Ciszowski K. , Biedroń W., Gomólka E. Acute Caffeine Poisoning Resulting in Atrial Fibrillation After Guarana Extract Overdose. Przeglad Lekarski. 2014; 71 (9): 495-8.
, Biedroń W., Gomólka E. Acute Caffeine Poisoning Resulting in Atrial Fibrillation After Guarana Extract Overdose. Przeglad Lekarski. 2014; 71 (9): 495-8.
81. Thyagarajan B, Alagusundaramoorthy S. S., Agrawal A. Atrial Fibrillation Due to Over The Counter Stimulant Drugs in A Young Adult. Journal of clinical and diagnostic research: JCDR. 2015; 9 (8): OD05-7. https://doi.org/10.7860/JCDR/2015/13483.6330.
Какие бывают типы APED?
Отчет об исследовании
Анаболические андрогенные стероиды , часто сокращаемые до «анаболических стероидов», «стероидов» или «андрогенов», 2,3
Эти соединения иногда используются в медицине для лечения задержки полового созревания и потери мышечной массы из-за болезни 4 , а также для лечения низкого уровня тестостерона у мужчин с сопутствующим заболеванием.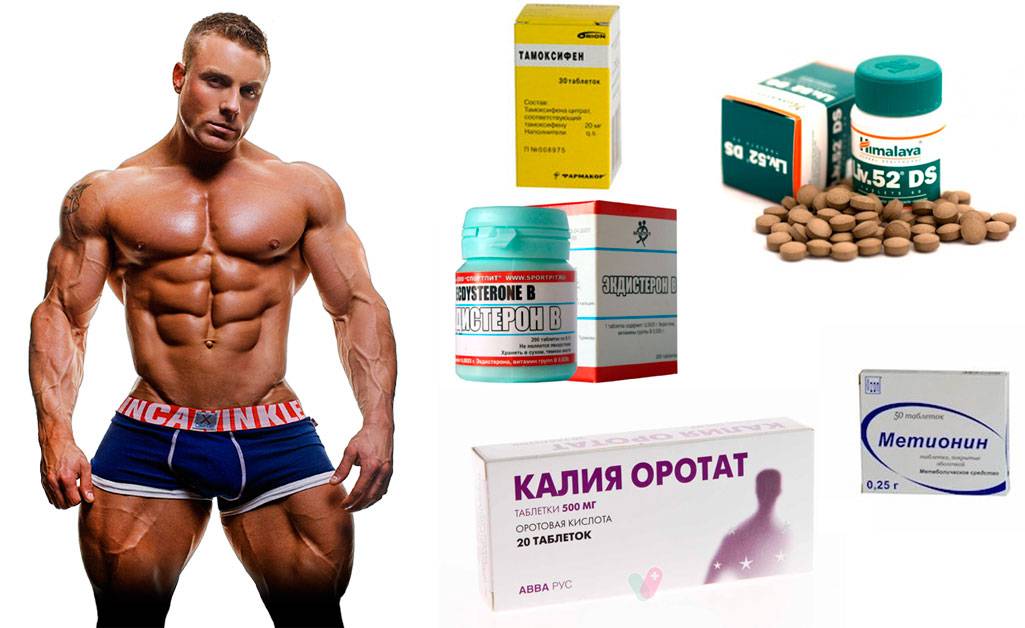 5 Анаболические андрогенные стероиды также могут улучшать самочувствие и повышать прочность костей, но они не одобрены для этих целей. Тем не менее, терапия добавками тестостерона становится все более распространенным средством лечения проблем с настроением и сексуальной активностью, связанных со старением мужчин, и ее назначают даже молодым мужчинам. 6
5 Анаболические андрогенные стероиды также могут улучшать самочувствие и повышать прочность костей, но они не одобрены для этих целей. Тем не менее, терапия добавками тестостерона становится все более распространенным средством лечения проблем с настроением и сексуальной активностью, связанных со старением мужчин, и ее назначают даже молодым мужчинам. 6
Обратите внимание, что в контексте данного отчета анаболические стероиды относятся только к непредписанному (неправильному использованию) тестостерона и тестостероноподобных веществ спортсменами и бодибилдерами, не занимающимися спортом. В этом исследовательском отчете не рассматриваются средства, улучшающие изображение, такие как кожные наполнители, ботокс или средство для загара кожи меланотан. 7
Нестероидные анаболики , включают инсулин, инсулиноподобный гормон роста (IGF) и гормон роста человека (HGH) — вещества, которые вырабатываются человеческим организмом и назначаются для законных медицинских целей, но также иногда неправильно используется для повышения производительности.
Эрго/термогеники — это соединения, используемые для уменьшения жировых отложений или повышения мышечной массы у спортсменов, занимающихся выносливостью.
- Ксантины : соединения, повышающие внимание и бодрствование и подавляющие аппетит. Примерами являются кофеин, лекарство от астмы теофиллин и теобромин — вещество, содержащееся в шоколаде, кофе и чае. 9
- Симпатомиметики : препараты, сходные по структуре и действию с адреналином и норадреналином — естественными химическими веществами в организме, которые увеличивают частоту сердечных сокращений, сужают кровеносные сосуды и повышают кровяное давление. Примером является эфедрин, который получают из растения эфедры. Эфедрин/эфедру раньше включали в пищевые добавки, которые способствовали снижению веса, увеличению энергии и улучшению спортивных результатов. 10 В 2004 году FDA запретило продажу в США пищевых добавок, содержащих эфедрин/эфедру, из-за различных возможных рисков для здоровья, включая воздействие на сердечно-сосудистую и нервную системы.
 11
11 - Гормоны щитовидной железы : вещества, которые регулируют обмен веществ путем изменения функции щитовидной железы. 12 Цитомель является примером.
Пищевые/диетические добавки – это вещества, приобретаемые на законных основаниях в магазинах пищевых продуктов или через Интернет, которые часто принимаются в сочетании с другими APEDS. Одним из распространенных примеров является креатин, повышающий работоспособность.
В Соединенных Штатах пищевые добавки, содержащие прекурсоры стероидов, такие как тетрагидрогестринон (ТГГ) и андростендион , ранее можно было приобрести на законных основаниях без рецепта. Спортсмены принимали предшественники стероидов, чтобы повысить уровень тестостерона. Меньше известно о побочных эффектах предшественников стероидов, но если большие количества этих соединений существенно повышают уровень тестостерона в организме, то они также, вероятно, будут вызывать те же побочные эффекты, что и сами анаболические стероиды. 13 Покупка этих добавок, за заметным исключением дегидроэпиандростерона (ДГЭА), стала незаконной после принятия Закона о контроле над анаболическими стероидами 2004 года, который внес поправки в Закон о контролируемых веществах. 14
13 Покупка этих добавок, за заметным исключением дегидроэпиандростерона (ДГЭА), стала незаконной после принятия Закона о контроле над анаболическими стероидами 2004 года, который внес поправки в Закон о контролируемых веществах. 14
Синтетические анаболические средства: стероиды и нестероидные селективные модуляторы андрогенных рецепторов
Обзор
. 2010;(195):99-126.
дои: 10.1007/978-3-540-79088-4_5.
Марио Тевис 1 , Вильгельм Шенцер
принадлежность
- 1 Центр профилактических допинговых исследований – Институт биохимии, Немецкий университет спорта, Кельн, Am Sportpark Müngersdorf 6, 50933, Кельн, Германия.
 [email protected]
[email protected]
- PMID: 20020362
- DOI: 10.1007/978-3-540-79088-4_5
Обзор
Марио Тевис и др. Handb Exp Pharmacol. 2010.
. 2010;(195):99-126.
doi: 10.1007/978-3-540-79088-4_5.
Авторы
Марио Тевис 1 , Вильгельм Шенцер
принадлежность
- 1 Центр профилактических допинговых исследований – Институт биохимии, Немецкий университет спорта, Кельн, Am Sportpark Müngersdorf 6, 50933, Кельн, Германия.
 [email protected]
[email protected]
- PMID: 20020362
- DOI: 10.1007/978-3-540-79088-4_5
Абстрактный
Центральная роль тестостерона в развитии мужских характеристик, а также его благотворное влияние на физическую работоспособность и рост мышц привели к поиску синтетических альтернатив с улучшенными фармакологическими свойствами. Были приготовлены сотни стероидных аналогов с превосходной биодоступностью при пероральном приеме, которые также должны обладать уменьшенными нежелательными эффектами. Однако лишь немногие вышли на фармацевтический рынок из-за серьезных токсикологических инцидентов, которые в основном объяснялись отсутствием тканевой селективности. Выдающимися представителями анаболо-андрогенных стероидов (ААС) являются, например, метилтестостерон, метандиенон и станозолол, которые обсуждаются в качестве модельных соединений в отношении общих фармакологических аспектов синтетических ААС. Недавно были разработаны нестероидные альтернативы ААС, которые избирательно активируют рецепторы андрогенов либо в мышечной ткани, либо в костях. Эти так называемые селективные модуляторы андрогенных рецепторов (SARM) в настоящее время проходят поздние клинические испытания (IIb) и будут запрещены Всемирным антидопинговым агентством с января 2008 года. Их полностью синтетические структуры почти не связаны со стероидами, но определенные функциональные группы позволяют для тканеселективной активации или ингибирования рецепторов андрогенов и, таким образом, стимуляции мышечного роста без риска серьезных нежелательных эффектов, обычно наблюдаемых при заместительной терапии стероидами. Следовательно, эти соединения обладают высоким потенциалом неправильного использования в спорте и в будущем станут предметом допинг-контроля.
Недавно были разработаны нестероидные альтернативы ААС, которые избирательно активируют рецепторы андрогенов либо в мышечной ткани, либо в костях. Эти так называемые селективные модуляторы андрогенных рецепторов (SARM) в настоящее время проходят поздние клинические испытания (IIb) и будут запрещены Всемирным антидопинговым агентством с января 2008 года. Их полностью синтетические структуры почти не связаны со стероидами, но определенные функциональные группы позволяют для тканеселективной активации или ингибирования рецепторов андрогенов и, таким образом, стимуляции мышечного роста без риска серьезных нежелательных эффектов, обычно наблюдаемых при заместительной терапии стероидами. Следовательно, эти соединения обладают высоким потенциалом неправильного использования в спорте и в будущем станут предметом допинг-контроля.
Похожие статьи
Масс-спектрометрия селективных модуляторов андрогенных рецепторов.
Тевис М., Шенцер В. Тевис М. и др. J Масс-спектр. 2008 июль; 43 (7): 865-76. doi: 10.1002/jms.1438. J Масс-спектр. 2008. PMID: 18521833 Обзор.
Структурные характеристики анаболических андрогенных стероидов, способствующие связыванию с рецептором андрогена и их анаболической и андрогенной активности. Прикладные модификации в стероидной структуре.
Фрагкаки А.Г., Ангелис Ю.С., Куппарис М., Цантили-Какулиду А., Кокотос Г., Георгакопулос К. Фрагкаки АГ и др. Стероиды. 2009 г., февраль; 74(2):172-97. doi: 10.1016/j.steroids.2008.10.016. Epub 2008 5 ноября. Стероиды. 2009. PMID: 19028512 Обзор.
Тканевая селективность и потенциальное клиническое применение тренболона (17бета-гидроксиэстра-4,9,11-триен-3-он): сильнодействующий анаболический стероид со сниженной андрогенной и эстрогенной активностью.

Ярроу JF, McCoy SC, Borst SE. Ярроу Дж. Ф. и соавт. Стероиды. 2010 июнь; 75 (6): 377-89. doi: 10.1016/j.steroids.2010.01.019. Epub 2010 4 февраля. Стероиды. 2010. PMID: 20138077 Обзор.
Анаболические агенты: современные стратегии их обнаружения и защиты от непреднамеренного приема допинга.
Гейер Х., Шенцер В., Тевис М. Гейер Х. и др. Бр Дж Спорт Мед. 2014 май; 48(10):820-6. дои: 10.1136/bjsports-2014-093526. Epub 2014, 14 марта. Бр Дж Спорт Мед. 2014. PMID: 24632537 Бесплатная статья ЧВК. Обзор.
Андрогенно-анаболические стероиды и Олимпийские игры.
Фитч К.Д. Фитч КД. Азиат Джей Андрол. 2008 май; 10(3):384-90. doi: 10.1111/j.1745-7262.2008.00377.
 x.
Азиат Джей Андрол. 2008.
PMID: 18385900
Обзор.
x.
Азиат Джей Андрол. 2008.
PMID: 18385900
Обзор.
Посмотреть все похожие статьи
Цитируется
Интеграция метаболомики с другими омиками: взгляд на понимание рака простаты.
Resurreccion EP, Фонг К.В. Resurreccion EP и др. Метаболиты. 2022 27 мая; 12 (6): 488. doi: 10.3390/metabo12060488. Метаболиты. 2022. PMID: 35736421 Бесплатная статья ЧВК. Обзор.
Селективные модуляторы андрогенных рецепторов: будущее андрогенной терапии?
Кристиансен А.Р., Липшульц Л.И., Хоталинг Дж.М., Пастушак А.В. Кристиансен А.Р. и соавт. Перевод Андрол Урол. 9 марта 2020 г. (Приложение 2): S135-S148. doi: 10.21037/tau.2019.11.02. Перевод Андрол Урол.
 2020.
PMID: 32257854
Бесплатная статья ЧВК.
Обзор.
2020.
PMID: 32257854
Бесплатная статья ЧВК.
Обзор.Роль анаболиков в колоректальном канцерогенезе: мифы и реальность (обзор).
Красанакис Т., Николузакис Т.К., Сганцос М., Мариолис-Сапсакос Т., Суглакос Дж., Спандидос Д.А., Цицимпику С., Цацакис А., Циаусис Дж. Красанакис Т. и соавт. Онкол Респ. 2019Декабрь; 42 (6): 2228-2244. doi: 10.3892/or.2019.7351. Epub 2019 3 октября. Онкол Респ. 2019. PMID: 31578582 Бесплатная статья ЧВК. Обзор.
Злоупотребление лекарствами, повышающими работоспособность, вызвало кардиомиопатию и острую травму печени у молодого бодибилдера.
Ли С, Адхикари Б.К., Гао Л., Чжан С., Лю Ц., Ван И, Сунь Дж. Ли С и др. Am J Mens Health. 2018 сен;12(5):17:00-17:04.


