Вы уверены, что вводите инсулин правильно?
Вы уверены, что вводите инсулин правильно?
- Запасы инсулина хранятся в холодильнике?
Его нужно хранить в холодильнике, он не должен замерзать.
- Инсулин не промерзал, не перегревался, был защищен от света?
Начатый флакон с инсулином хранится при комнатной температуре?
Да, он может и должен храниться именно так. Введенный холодным, инсулин действует слабее.
- Вы проверяете срок годности Вашего инсулина регулярно?
Нельзя использовать просроченные препараты. Они не только не помогают, но могут серьезно навредить.
- Не попадает ли в шприц воздух?
При попадании в шприц воздуха, Вы введете меньшее количество инсулина, чем рассчитывали
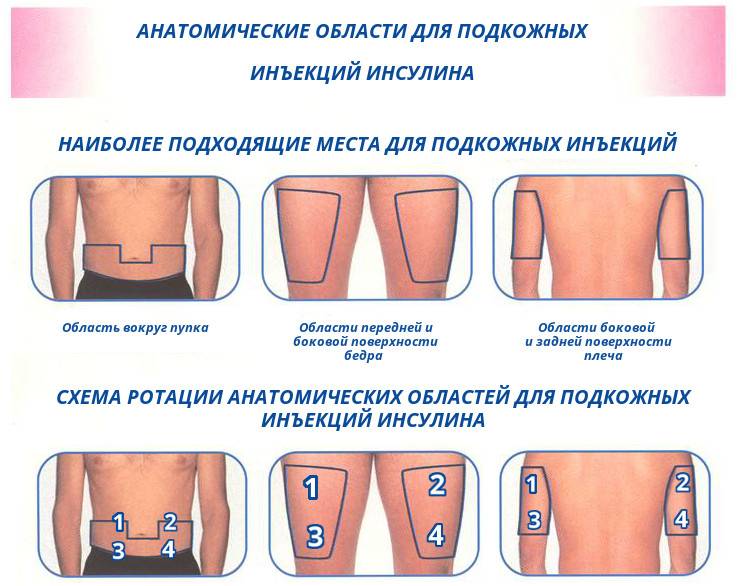
- Куда вводится инсулин?
Лучше всего инсулин действует из-под кожи живота
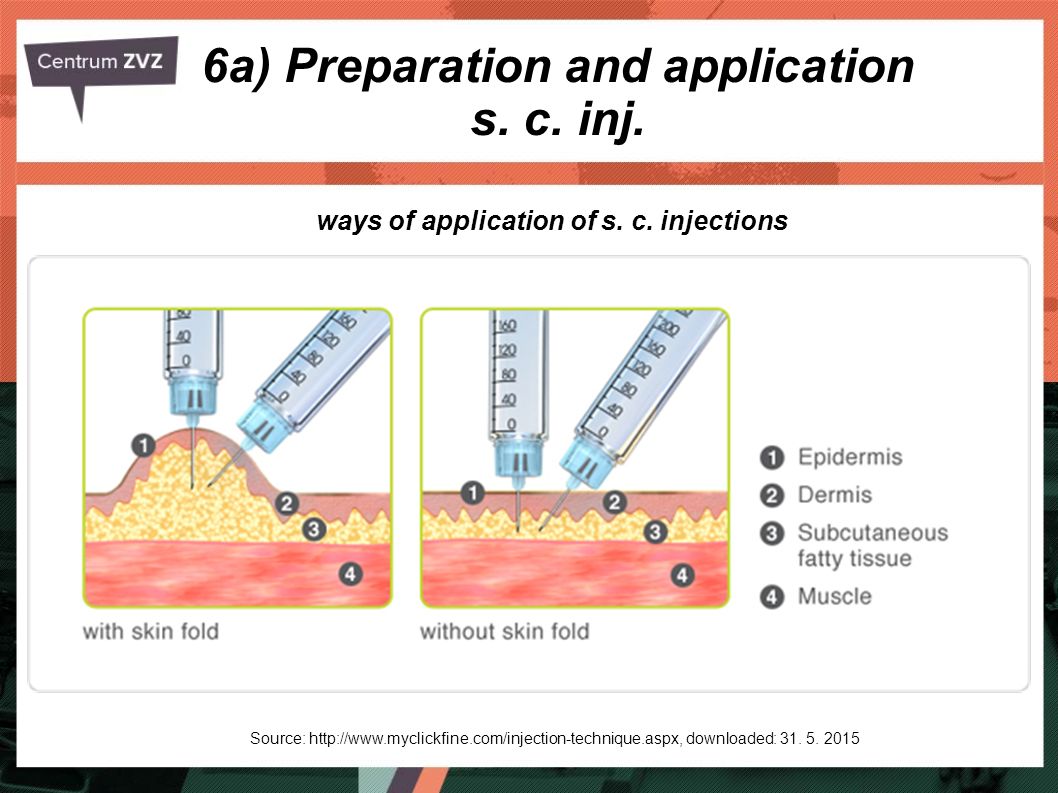
Кожную складку нельзя отпускать, пока Вы не ввели весь инсулин.
- Не протираете ли Вы перед инъекцией кожу спиртом?

- По какому принципу Вы меняете зону введения инсулина?
Существуют 2 варианта:
1. Каждый день используют все зоны по строгому плану (для каждой инъекции — своя зона). При этом инсулин короткого действия желательно вводить под кожу живота, обеспечивая более быстрое начало действия.
2. Несколько недель инсулин вводят в одну из зон (например, в живот), следующие несколько недель — в другую (например, в бедра).
- Какую часть от всей зоны (например, живота) Вы используете для инъекций?
Надо использовать всю зону, как можно шире. В область между ребрами и пупком также можно вводить инсулин. При этом на коже не будут возникать уплотнения, а болезненность инъекций будет меньше.
- Берете ли Вы перед инъекцией кожу в складку?
Если не сделать этого, инсулин может быть введен в мышцу. Он будет работать то сильнее, то слабее.
- Не попадаете ли Вы в уплотнения или “жировики” после старых инъекций?
При попадании в эти места инсулин действует слабее.
- Ожидаете ли Вы 7-10 секунд, прежде чем вынуть иглу после инъекции?
Если не сделать этого, инсулин будет вытекать обратно через место инъекции.
- Не вытекают ли капли инсулина из места введения?
В этом случае неизвестная часть инсулина не попадет в организм.
- За сколько минут до еды Вы вводите “короткий” инсулин? Всегда ли Вы соблюдаете этот интервал?
В живот – за 20 минут, в другие места – за 30. Если не соблюдать этот интервал, действие будет слишком слабым.
- Смешиваете ли Вы разные инсулины в одном шприце?
Некоторые препараты продленного инсулина (Протафан, Хумулин НПХ) можно перед инъекцией набирать в один шприц с коротким инсулином (хотя при этом требуется соблюдение специальных правил и повышается риск ошибок при наборе дозы). Другие инсулины продленного действия (Лантус, Левемир) при смешивании с коротким инсулином приводят к изменению действия этой смеси.
- Если Вы пользуетесь шприц-ручкой:
Не вытекает ли инсулин из иглы после инъекции?
Выход инсулина из шприц- ручки занимает несколько секунд.
 Вынимайте иглу через 7-10 секунд после нажатия кнопки шприц- ручки.
Вынимайте иглу через 7-10 секунд после нажатия кнопки шприц- ручки. - Как Вы перемешиваете “продленный” инсулин?
Надо 5-7 раз перевернуть ее иглой то вверх, то вниз.
- Правильно ли Вы набираете дозу инсулина? До конца ли вводите набранную дозу?
В некоторых шприц-ручках, если кнопка поршня нажата не до упора, инсулин вводится лишь частично. Если Вы не уверены, что правильно пользуетесь шприц- ручкой – попросите родственников или медицинских работников помочь Вам.
Дополнительно
Дополнительная вкладка, для размещения информации о статьях, доставке или любого другого важного контента. Поможет вам ответить на интересующие покупателя вопросы и развеять его сомнения в покупке. Используйте её по своему усмотрению.
Вы можете убрать её или вернуть обратно, изменив одну галочку в настройках компонента. Очень удобно.
Страница не найдена | Консультативно-диагностическая поликлиника №1 Приморского района
Страница не найдена | Консультативно-диагностическая поликлиника №1 Приморского районаСтраница не найдена
Страницы, на которую вы попали, либо не существует, либо она была перенесена.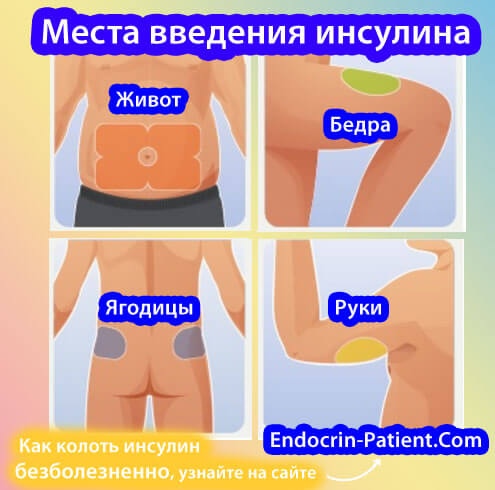 Пожалуйста, воспользуйтесь меню или формой поиска, чтобы найти то, что вы хотели.
Пожалуйста, воспользуйтесь меню или формой поиска, чтобы найти то, что вы хотели.
Поиск
Недавние записи
- День борьбы с гепатитом
- Получайте налоговые уведомления через портал ГОСУСЛУГ!
- Набор социальных услуг
- 17 – 23 июля – Неделя сохранения здоровья головного мозга (в честь Всемирного дня мозга 22 июля).
Меню
- #1442 (без названия)
- #3422 (без названия)
- #5428 (без названия)
- #4317 (без названия)
- #4899 (без названия)
- #5243 (без названия)
- #5290 (без названия)
- #332114 (без названия)
- tn
- Взаимодействие с социально ориентированными некоммерческими организациями (СОНКО) и волонтерскими организациями
- Внеочередное оказание медицинской помощи
- Всероссийская перепись населения 2021
- Всероссийский День Трезвости в 2018 году отмечается 11 сентября.
- График работы врачей оказывающих платные медицинские услуги
- Договор на оказание платных услуг
- Доступная среда
- Доступная среда Флюорографическая станция СПб ГБУЗ КДП№1
- Записаться на прием к врачу
- Инфографика COVID-19
- Информация о использовании бюджетных ассигнований
- Карта сайта
- Коронавирусная инфекция
- Лицензия организации на осуществление медицинской деятельности
- Оставьте отзыв о нашей работе.

- Ответы на часто задаваемые вопросы по COVID-19
- Отправить обращение или оставить отзыв
- Отправить отзыв
- Платные услуги
- Прейскурант платных мед.услуг (Pdf форма)
- Форма записи на платный прием
- Политика конфиденциальности
- Положение и Приказы по платным медицинским услугам
- Положение об антимонопольном комплаенсе
- Постановление Правительства РФ Об утверждении правил предоставления медицинскими организациями платных медицинских услуг
- Прейскурант платных медицинских услуг
- Прейскурант платных медицинских услуг
- Сведения о медицинских работниках участвующих в предоставлении платных медицинских услуг
- Сведения о медицинских работниках, участвующих в предоставлении платных медицинских услуг
- Сообщи, где торгуют смертью
- Социальная защита населения
- СПб ГБУЗ «Межрайонный Петроградско-Приморский противотуберкулезный диспансер №3»
- Структура
- Устав организации
- Целевая подготовка специалистов
- Электронное расписание1
- Электронное расписание2
- Электронное расписание3
- Электронное расписание4
- Главная
- Кабинеты и отделения
- Дневной стационар
- Межрайонный диабетологический центр №5 телефон 431-01-66
- Платные услуги Диабетологического центра №5
- Школы здоровья
- Клинико-диагностическая лаборатория
- Для специалистов
- Зачем сдавать анализы?
- Как подготовиться к сдаче анализов.

- Как пройти обследование?
- О лаборатории
- Список платных услуг Лаборатории
- Что может повлиять на результаты Анализа
- Центр здоровья
- Гастроэнтерологическое отделение
- Флюорографическая станция
- Центр амбулаторной онкологической помощи
- Консультативно диагностическое отделение
- Районный диабетологический центр
- Поликлиника
- Администрация
- Антинаркотическая политика
- Справочная информация
- Часто задаваемые вопросы
- Вышестоящие организации
- Фотогалерея
- График работы врачей
- Документы для ознакомления
- Нормативные документы
- Информация для ознакомления
- О рекомендациях по проведению дезинфекционных мероприятий в жилых помещениях для лиц, находящихся в домашней изоляции
- порядок возобновления получения набора социальных услуг
- Доступная среда СПб ГБУЗ КДП №1
- Противодействие коррупции
- 1.
 Нормативные правовые и иные акты в сфере противодействия коррупции
Нормативные правовые и иные акты в сфере противодействия коррупции - 2. Антикоррупционная экспертиза
- 3. Методические материалы
- 4. Формы документов, связанных с противодействием коррупции, для заполнения
- 5. Сведения о доходах, об имуществе и обязательствах имущественного характера руководителей Приморского района
- 5.1 Протоколы заседаний Комиссии по противодействию коррупции в СПБ ГБУЗ КДП №1
- 6. Комиссия по противодействию коррупции в СПБ ГБУЗ КДП №1
- 7. Обратная связь для сообщений о фактах коррупции
- 8. Меры юридической ответственности
- 9 .Информационные материалы
- Коронавирус 2019-nOcV
- 1.
- Страница профсоюза
- Виды медицинской помощи
- Новости
- Контакты
- Наши вакансии
- Ликвидация кадрового дефицита
- Отзывы
- Добавить отзыв
- Регистрационная карта обращения
- Наши вакансии
Биохакеры придумали, как сделать инсулин на 98% дешевле
Серия| Just Might Work
Биохакеры нацелены на удушение большой фармы инсулином
Смотреть на YouTube
Далее
Автор Джек Бернинг
Сто лет назад ученые начали исследовать, как сделать инсулин из поджелудочной железы собак и крупного рогатого скота. С тех пор инсулин используется для лечения людей, страдающих диабетом, но только в 80-х годах генная инженерия позволила широко распространить это жизненно важное лекарство.
В организме здорового человека инсулин представляет собой гормон, вырабатываемый поджелудочной железой, который контролирует уровень глюкозы в крови. Но организм диабетика естественным образом не вырабатывает инсулин, а это означает, что организм не может хранить глюкозу для последующего использования в качестве энергии в жировых клетках.
Из-за этого жировые клетки разрушаются и производят избыточное количество кетокислот — органических соединений, отвечающих за преобразование глюкозы в энергию, — что приводит к слишком высокому уровню кислоты, который печень не может выдержать. Если у диабетика нет доступа к инсулину, этот кислотный дисбаланс может вызвать диабетический кетоацидоз, опасное для жизни состояние. Вот почему мониторинг уровня инсулина и использование лекарств имеют решающее значение для выживания диабетиков.
Вот почему мониторинг уровня инсулина и использование лекарств имеют решающее значение для выживания диабетиков.
Сегодня более семи миллионов американцев с диабетом используют по крайней мере одну форму инсулина для лечения этого заболевания, но многие из них рискуют не получить необходимой помощи. Американская диабетическая ассоциация сообщила, что 25% пациентов начали самостоятельно нормировать свои лекарства, чтобы справиться с их постоянно растущей ценой.
Почему инсулин такой дорогой?
Стандартный процесс производства инсулина включает его выращивание в обычных бактериях, таких как кишечная палочка или дрожжи, с помощью машины для секвенирования аминокислот. Подсчитано, что производство флакона инсулина обходится фармацевтическим компаниям в пять-шесть долларов, но из-за сложной сети правил эти компании могут продавать флаконы за 180-400 долларов.
В росте цен нет ничего нового. Цены на инсулин выросли втрое с 2002 по 2013 год и удвоились в период с 2012 по 2016 год. Для сравнения: в 1996 году флакон Хумалога производства Eli Lilly стоил 21 доллар. Сегодня он стоит 324 доллара, несмотря на то, что стоимость производства остается стабильной. Для тех, кто использует несколько флаконов в месяц, расходы могут быстро исчисляться тысячами.
Для сравнения: в 1996 году флакон Хумалога производства Eli Lilly стоил 21 доллар. Сегодня он стоит 324 доллара, несмотря на то, что стоимость производства остается стабильной. Для тех, кто использует несколько флаконов в месяц, расходы могут быстро исчисляться тысячами.
В фармацевтической промышленности США 90% мирового рынка инсулина принадлежит трем компаниям: Novo Nordisk, Eli Lilly и Sanofi. Эти компании по существу имеют монополию на рынке; просто нет конкуренции, чтобы снизить цену. Кроме того, их рост цен оставался постоянным с течением времени.
Каждый человек с диабетом I типа зависит от инсулина, чтобы выжить, и многие готовы потратить все, что потребуется, чтобы получить необходимую дозу. Крупная фармацевтика явно использует в своих интересах эту уязвимую часть населения, наедая себя, взимая астрономические расходы и снижая цены для тех, кто не может позволить себе идти в ногу со временем.
Группа преданных своему делу биохакеров считает, что для того, чтобы сделать инсулин более доступным, необходимо лишить монополию трех больших фармацевтических компаний, производящих его. Поэтому они основали Open Insulin Foundation, некоммерческую организацию, планирующую разработать первую в мире модель производства инсулина с открытым исходным кодом.
Поэтому они основали Open Insulin Foundation, некоммерческую организацию, планирующую разработать первую в мире модель производства инсулина с открытым исходным кодом.
Команда состоит из десятков добровольцев во главе с основателем Энтони ДиФранко, страдающим диабетом I типа. Теперь они могут производить микроорганизмы, необходимые для инсулина, с помощью биореактора. Они также работают над созданием оборудования для очистки белков, производимых биореактором.
С помощью оборудования с открытым исходным кодом, эквивалентного патентованным биореакторам, фонд надеется предоставить лабораториям по всему миру доступ к оборудованию, необходимому для производства белка инсулина в небольших масштабах.
«Очень немногие люди действительно имеют конкретные идеи о том, как решить эти проблемы», — говорит ДиФранко. «На уровне технических основ ясно, что мы можем это сделать. И если мы можем, мы должны».
Но процесс оказался непростым. В течение шести лет команда ДиФранко пыталась реконструировать производство инсулина с помощью экспериментов под руководством добровольцев в своих общественных лабораториях в таких городах, как Окленд, Балтимор и Саннивейл, Калифорния.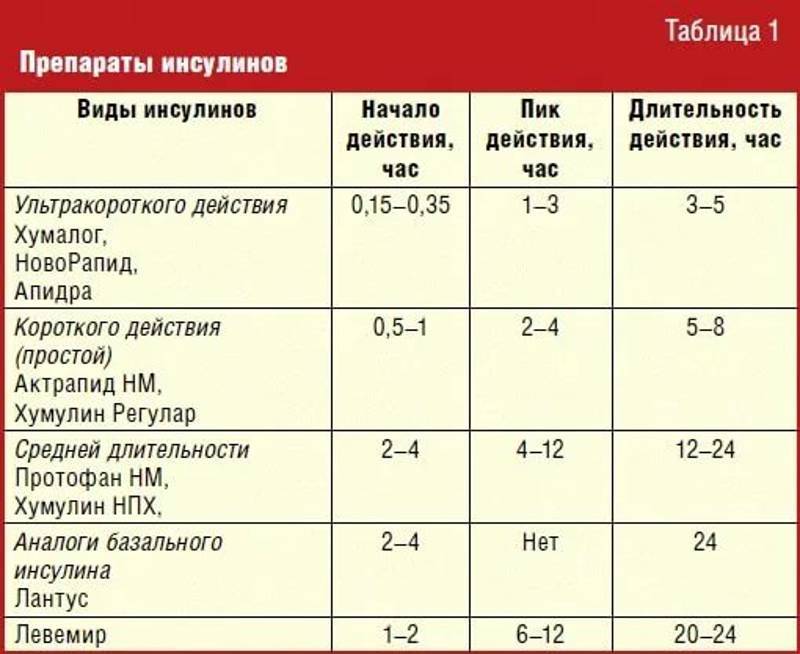
Сегодня они начинают замечать обнадеживающие признаки крупного прорыва — например, получить одобренный FDA протокол для изготовления инъекционных препаратов. По оценкам команды, затраты составят 9На 8% дешевле, чем в крупных фармацевтических компаниях, достигая цен на уровне 5-15 долларов за флакон. Лучшая часть? Они готовы раздать свои планы по производству инсулина бесплатно.
«Наш план состоит в том, чтобы иметь систему для местного производства, которая могла бы работать в любой точке мира, где в ней есть потребность», — объясняет ДиФранко. Open Insulin уже сотрудничает с общественными лабораториями, академическими учреждениями, группами защиты интересов пациентов и неправительственными организациями по всей стране и за ее пределами.
Они надеются, что их работа в конечном итоге приведет к распространению инсулина в странах, которые в настоящее время не имеют к нему доступа. «Было время злиться, — говорит ДиФранко. «Теперь, когда мы действительно можем скоро увидеть конец этому, это больше не гнев. Это просто решимость».
Это просто решимость».
Клеточные фабрики по производству инсулина
1. Cohen SN, Chang ACY, Boyer HW, Helling RB. Конструирование биологически функциональных бактериальных плазмид in vitro. Proc Natl Acad Sci U S A. 1973; 70:3240–3244. doi: 10.1073/pnas.70.11.3240. [Статья PMC бесплатно] [PubMed] [CrossRef] [Google Scholar]
2. Нильсен Дж. Производство биофармацевтических белков дрожжами. Landes Biosci Bioengineered. 2013;4(4):207–211. doi: 10.4161/bioe.22856. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
3. Гудман М., Обзор рынка Продажи биопрепаратов продемонстрируют устойчивый рост до 2013 года. Nat Rev Drug Discov. 2009; 8:837. doi: 10.1038/nrd3040. [PubMed] [CrossRef] [Google Scholar]
4. Аггарвал С. Что подпитывает биотехнологический двигатель с 2010 по 2011 год. Nat Biotechnol. 2011;29:1083–1089. doi: 10.1038/nbt.2060. [PubMed] [CrossRef] [Google Scholar]
5. Walsh G. Biopharmaceuticals: одобрения и тенденции одобрения в 2004 г. Biopharm Int. 2005; 18:58–65. [Google Scholar]
Biopharm Int. 2005; 18:58–65. [Google Scholar]
6. Уолш Г. Биофармацевтические препараты: тенденции одобрения в 2005 г. BioPharm Int. 2006;9: 58–68. [Google Scholar]
7. Уолш Г. Биофармацевтические препараты: тенденции одобрения в 2006 г. BioPharm Int. 2007; 20:40–48. [Google Scholar]
8. Walsh G. Biopharmaceuticals: тенденции одобрения в 2007 г. BioPharm Int. 2008; 21:52–65. [Google Scholar]
9. Уолш Г. Биофармацевтические препараты: тенденции одобрения в 2008 г. BioPharm Int. 2009;22(10):68–77. [Google Scholar]
10. Уолш Г. Тенденции одобрения биофармацевтических препаратов в 2009 г. BioPharm Int. 2010;23(10):30–41. [Академия Google]
11. Уолш Г. Биофармацевтические эталоны. Нац биотехнолог. 2010;28:917–924. doi: 10.1038/nbt0910-917. [PubMed] [CrossRef] [Google Scholar]
12. Уолш Г. Новые биофармацевтические препараты. БиоФарм Инт. 2012; 25:34–36. [Google Scholar]
13. Уолш Г. Тенденции одобрения биофармацевтических препаратов в 2013 году. Biopharm Int. 2013;26(4):54–56. [Google Scholar]
Biopharm Int. 2013;26(4):54–56. [Google Scholar]
14. Уолш Г. Терапевтические инсулины и их крупномасштабное производство. Приложение Microbiol Biotechnol. 2005; 67: 151–159. doi: 10.1007/s00253-004-1809-Икс. [PubMed] [CrossRef] [Google Scholar]
15. Ferrer-Miralles N, Domingo-Espin J, Corchero JL, Vazquez E, Villaverde A. Микробные фабрики для рекомбинантных фармацевтических препаратов. Факт микробной клетки. 2009; 8:17. дои: 10.1186/1475-2859-8-17. [PMC free article] [PubMed] [CrossRef] [Google Scholar]
16. Nilsson J, Jonasson P, Samuelsson E, Stahl S, Uhlen M. Интегрированное производство человеческого инсулина и его С-пептида. Дж Биотехнолог. 1996; 48: 241–250. doi: 10.1016/0168-1656(96)01514-3. [PubMed] [CrossRef] [Академия Google]
17. Thim L, Hansen MT, Norris K, Hoegh I, Boel E, Forstrom J, Ammerer G, Fiil NP. Секреция и процессинг предшественников инсулина в дрожжах. Proc Natl Acad Sci U S A. 1986; 83:6766–6770. doi: 10.1073/pnas.83.18.6766. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
18. Markussen J, Damgaard U, Diers I, Fiil N, Hansen MT, Larsen P, Norris F, Norris K, Schou O, Snel L, Thim L, Voigt HO. Биосинтез человеческого инсулина в дрожжах через одноцепочечные предшественники. Диабетология. 1986;29:568А–569А. [Google Scholar]
Markussen J, Damgaard U, Diers I, Fiil N, Hansen MT, Larsen P, Norris F, Norris K, Schou O, Snel L, Thim L, Voigt HO. Биосинтез человеческого инсулина в дрожжах через одноцепочечные предшественники. Диабетология. 1986;29:568А–569А. [Google Scholar]
19. Kjeldsen T. Секреторная экспрессия предшественников инсулина в дрожжах. Приложение Microbiol Biotechnol. 2000; 54: 277–286. doi: 10.1007/s002530000402. [PubMed] [CrossRef] [Google Scholar]
20. Холленберг С.П., Геллиссен Г. Производство рекомбинантных белков метилотрофными дрожжами. Курр Опин Биотехнолог. 1997; 8: 554–560. doi: 10.1016/S0958-1669(97)80028-6. [PubMed] [CrossRef] [Google Scholar]
21. Геллиссен Г., Холленберг С.П. Применение дрожжей в исследованиях экспрессии генов Сравнение Saccharomyces cerevisiae, Hansenula polymorpha и Kluyveromyces lactis – обзор. Ген. 1997;190:87–97. doi: 10.1016/S0378-1119(97)00020-6. [PubMed] [CrossRef] [Google Scholar]
22. Романос М. Достижения в использовании Pichia pastoris для экспрессии генов высокого уровня.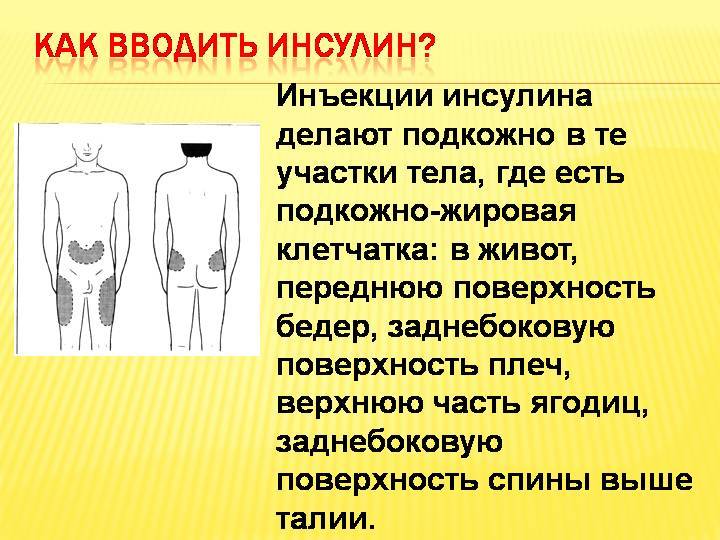 Курр Опин Биотехнолог. 1995; 6: 527–533. doi: 10.1016/0958-1669(95)80087-5. [CrossRef] [Google Scholar]
Курр Опин Биотехнолог. 1995; 6: 527–533. doi: 10.1016/0958-1669(95)80087-5. [CrossRef] [Google Scholar]
23. Weydemann U, Keup P, Piontek M, Strasser AW, Schweden J, Gellissen G, Janowicz ZA. Высокий уровень секреции гирудина Hansenula polymorpha — аутентичный процессинг трех разных препрогирудинов. Приложение Microbiol Biotechnol. 1995;44:377–385. doi: 10.1007/BF00169932. [PubMed] [CrossRef] [Google Scholar]
24. Порро Д., Зауэр М., Брандуарди П., Маттанович Д. Производство рекомбинантного белка в дрожжах. Мол Биотехнолог. 2005; 31: 245–259. дои: 10.1385/МБ:31:3:245. [PubMed] [CrossRef] [Google Scholar]
25. Yanagita M, Nakayama K, Takeuchi T. Процессинг мутантного проинсулина с сайтами четырехосновного расщепления в биоактивный инсулин в неэндокринной клеточной линии COS-7. ФЭБС лат. 1992; 311: 55–59. дои: 10.1016/0014-5793(92)81366-Т. [PubMed] [CrossRef] [Google Scholar]
26. Arakawa T, Yu J, Chong DKX, Hough J, Engen PC, Langridge WHR. Слитый белок субъединицы холерного токсина В и инсулина растительного происхождения защищает от развития аутоиммунного диабета. Нац биотехнолог. 1998; 16: 934–938. doi: 10.1038/nbt1098-934. [PubMed] [CrossRef] [Google Scholar]
Нац биотехнолог. 1998; 16: 934–938. doi: 10.1038/nbt1098-934. [PubMed] [CrossRef] [Google Scholar]
27. Nykiforuk CL, Boothe JG, Murray EW, Keon RG, Goren HJ, Markley NA, Moloney MM. Трансгенная экспрессия и выделение биологически активного рекомбинантного инсулина человека из семян Arabidopsis thaliana. Plant Biotech J. 2006; 4:77–85. doi: 10.1111/j.1467-7652.2005.00159.Икс. [PubMed] [CrossRef] [Google Scholar]
28. Boyhan D, Daniel H. Недорогое производство проинсулина в хлоропластах табака и салата для инъекций или пероральной доставки функционального инсулина и C-пептида. Plant Biotech J. 2011;9:585–598. doi: 10.1111/j.1467-7652.2010.00582.x. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
29. Wild S, Roglic G, Green A, Sicree R, King H. Глобальная распространенность диабета: оценки на 2000 год и прогнозы на 2030 год. Diabetes Care. 2004; 27:1047–1053. doi: 10.2337/diacare.27.5.1047. [PubMed] [CrossRef] [Академия Google]
30. Сахдев С., Хаттар С. К., Сайни К.С. Производство активных эукариотических белков с помощью бактериальных систем экспрессии: обзор существующих биотехнологических стратегий. Мол Селл Биохим. 2008; 307: 249–264. doi: 10.1007/s11010-007-9603-6. [PubMed] [CrossRef] [Google Scholar]
К., Сайни К.С. Производство активных эукариотических белков с помощью бактериальных систем экспрессии: обзор существующих биотехнологических стратегий. Мол Селл Биохим. 2008; 307: 249–264. doi: 10.1007/s11010-007-9603-6. [PubMed] [CrossRef] [Google Scholar]
31. Арья Р., Бхаттачарья А., Шайни К.С. Dictyostelium discoideum — многообещающая система экспрессии для продукции эукариотических белков. FASEB J. 2008; 22:4055–4066. doi: 10.1096/fj.08-110544. [PubMed] [CrossRef] [Академия Google]
32. Ferrer-Miralles N, Villaverde A. Фабрики бактериальных клеток для производства рекомбинантных белков; расширение каталога. Факт микробной клетки. 2013;12:113. дои: 10.1186/1475-2859-12-113. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
33. Kjeldsen T, Pettersson AF, Hach M. Секреторная экспрессия и характеристика инсулина у Pichia pastoris. Биотехнология Appl Biochem. 1999; 29: 79–86. [PubMed] [Google Scholar]
34. Gerngross TU. Достижения в производстве терапевтических белков человека в дрожжах и мицелиальных грибах. Нац биотехнолог. 2004;22:1409–1414. doi: 10.1038/nbt1028. [PubMed] [CrossRef] [Google Scholar]
Нац биотехнолог. 2004;22:1409–1414. doi: 10.1038/nbt1028. [PubMed] [CrossRef] [Google Scholar]
35. Mansur M, Cabello C, Hernandez L, Pais J, Varas L, Valdes J, Terrero Y, Hidalgo A, Plana L, Besada V, Garcia L, Lamazares E, Castellanos L, Martinez E. Множественное число копий гена усиливает секрецию предшественника инсулина у дрожжей Pichia pastoris . Биотехнологическая лат. 2005; 27: 339–345. doi: 10.1007/s10529-005-1007-7. [PubMed] [CrossRef] [Google Scholar]
36. Wurm FM. Производство рекомбинантных белковых терапевтических средств в культивируемых клетках млекопитающих. Нац биотехнолог. 2004; 22:1358–139.3. doi: 10.1038/nbt1026. [PubMed] [CrossRef] [Google Scholar]
37. Vajo Z, Fawcett J, Duckworth WC. Технология рекомбинантной ДНК в лечении диабета: аналоги инсулина. Endocr Rev. 2001; 22:706–717. doi: 10.1210/edrv.22.5.0442. [PubMed] [CrossRef] [Google Scholar]
38. Ахмад Б. Фармакология инсулина. Br J Диабет Vasc Dis. 2004; 4:10–14. doi: 10.1177/14746514040040010201. [CrossRef] [Google Scholar]
[CrossRef] [Google Scholar]
39. Дженкинс Н. Модификации терапевтических белков: проблемы и перспективы. Цитотехнология. 2007; 53: 121–125. doi: 10.1007/s10616-007-9075-2. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
40. Уолш Г., Джефферис Р. Посттрансляционные модификации в контексте терапевтических белков. Нац биотехнолог. 2006; 24:1241–1252. doi: 10.1038/nbt1252. [PubMed] [CrossRef] [Google Scholar]
41. Wacker M, Linton D, Hitchen PG, Nita-Lazar M, Haslam SM, North SJ, Panico M, Morris HR, Dell A, Wren BW, Aebi M. N-связанное гликозилирование в Campylobacter jejuni и его функциональный перенос в E. coli. Наука. 2002;298: 1790–1793. doi: 10.1126/science.298.5599.1790. [PubMed] [CrossRef] [Google Scholar]
42. Feldman MF, Wacker M, Hernandez M, Hitchen PG, Marolda CL, Kowarik M, Morris HR, Dell A, Valvano MA, Aebi M. Разработка N-связанного гликозилирования белка с различными структурами липополисахарида O-антигена в Escherichia coli. Proc Natl Acad Sci U S A. 2005;102:3016–3021. doi: 10.1073/pnas.0500044102. [Статья бесплатно PMC] [PubMed] [CrossRef] [Google Scholar]
2005;102:3016–3021. doi: 10.1073/pnas.0500044102. [Статья бесплатно PMC] [PubMed] [CrossRef] [Google Scholar]
43. Wacker M, Feldman MF, Callewaert N, Kowarik M, Clarke BR, Pohl NL, Hernandez M, Vines ED, Valvano MA, Whitfield C, Aebi M. Субстратная специфичность бактериальной олигосахарилтрансферазы предполагает общий механизм переноса бактериальная и эукариотическая системы. Proc Natl Acad Sci U S A. 2006; 103:7088–709.3. doi: 10.1073/pnas.0509207103. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
44. Fisher AC, Haitjema CH, Guarino C, Celik E, Endicott CE, Reading CA, Merritt JH, Ptak AC, Zhang S, DeLisa MP. Продукция секреторных и внеклеточных N-связанных гликопротеинов в Escherichia coli. Appl Environ Microbiol. 2011;77:871–881. doi: 10.1128/AEM.01901-10. [Статья бесплатно PMC] [PubMed] [CrossRef] [Google Scholar]
45. Ihssen J, Kowarik M, Dilettoso S, Tanner C, Wacker M, Thoxy-Meyer L. Производство гликопротеиновых вакцин в Escherichia coli. Факт микробной клетки. 2010;9:61. дои: 10.1186/1475-2859-9-61. [Статья бесплатно PMC] [PubMed] [CrossRef] [Google Scholar]
Факт микробной клетки. 2010;9:61. дои: 10.1186/1475-2859-9-61. [Статья бесплатно PMC] [PubMed] [CrossRef] [Google Scholar]
46. Lizak C, Fan Y, Web TC, Aebi M. N-связанное гликозилирование фрагментов антител в Escherichia coli. Биоконьюг Хим. 2011; 22: 488–496. doi: 10.1021/bc100511k. [PubMed] [CrossRef] [Google Scholar]
47. Pandhal H, Ow SY, Noirel J, Wright PC. Повышение эффективности N-гликозилирования в Escherichia coli с использованием анализа метаболической сети протеомики дробовика и селективного мониторинга реакций. Биотехнология Биоинж. 2011;108:902–912. doi: 10.1002/bit.23011. [PubMed] [CrossRef] [Google Scholar]
48. Чен Р. Бактериальные системы экспрессии для производства рекомбинантных белков: E. coli и другие. Биотехнология Adv. 2012;30:1102–1107. doi: 10.1016/j.biotechadv.2011.09.013. [PubMed] [CrossRef] [Google Scholar]
49. Makrides SC. Стратегии достижения высокого уровня экспрессии генов в Escherichia coli. Microbiol Rev. 1996;60:512–538. [Бесплатная статья PMC] [PubMed] [Google Scholar]
[Бесплатная статья PMC] [PubMed] [Google Scholar]
50. Kane JF. Влияние кластеров редких кодонов на высокий уровень экспрессии гетерологичных белков в Escherichia coli. Курр Опин Биотехнолог. 1995;6(5):494–500. doi: 10.1016/0958-1669(95)80082-4. [PubMed] [CrossRef] [Google Scholar]
51. Trundova M, Celer V. Экспрессия гена ORF2 свиного цирковируса 2 нуждается в кодон-оптимизированных клетках E.coli. Гены вирусов. 2007; 34: 199–204. doi: 10.1007/s11262-006-0043-2. [PubMed] [CrossRef] [Google Scholar]
52. Sorensen HP, Sperling-Petersen HU, Mortensen KK. Производство рекомбинантных термостабильных белков, экспрессированных в Escherichia coli: завершение синтеза белка является узким местом. J Chromatogr B Analyt Technol Biomed Life Sci. 2003; 786: 207–214. дои: 10.1016/S1570-0232(02)00689-ИКС. [PubMed] [CrossRef] [Google Scholar]
53. Bill RM, Henderson PJF, Iwata S, Kunji ERS, Michel H, Neutze R, Newstead S, Poolman B, Tate CG, Voge H. Преодоление барьеров в определении структуры мембранного белка. Нац биотехнолог. 2011;29(4):335–340. doi: 10.1038/nbt.1833. [PubMed] [CrossRef] [Google Scholar]
Нац биотехнолог. 2011;29(4):335–340. doi: 10.1038/nbt.1833. [PubMed] [CrossRef] [Google Scholar]
54. Huang CJ, Lin H, Yang X. Промышленное производство рекомбинантных терапевтических средств в Escherichia coli и его последние достижения. J Ind Microbiol Biotechnol. 2012; 39: 383–39.9. doi: 10.1007/s10295-011-1082-9. [PubMed] [CrossRef] [Google Scholar]
55. Рейли Д.Е., Янсура Д.Г. Продукция моноклональных антител в E. coli. В: Шайр С.Дж., Гомботц В., Бехтольд-Питерс К., Андья Дж., редакторы. Современные тенденции в разработке и производстве моноклональных антител. Нью-Йорк: Спрингер; 2010. С. 295–308. [Google Scholar]
56. Овертон Т.В. Продукция рекомбинантных белков в бактериях-хозяевах. Наркотиков Дисков Сегодня. 2014;19(5):590–601. doi: 10.1016/j.drudis.2013.11.008. [PubMed] [CrossRef] [Академия Google]
57. Каррио М.М., Вильяверде А. Роль молекулярных шаперонов в формировании телец включения. Фебс Летт. 2003;537(1–3):215–221. doi: 10.1016/S0014-5793(03)00126-1. [PubMed] [CrossRef] [Google Scholar]
[PubMed] [CrossRef] [Google Scholar]
58. Де Марко А. Протокол получения белков с улучшенной растворимостью путем совместной экспрессии с молекулярными шаперонами в Escherichia coli. Нат Проток. 2007;2(10):2632–2639. doi: 10.1038/nprot.2007.400. [PubMed] [CrossRef] [Google Scholar]
59. Chance R, Frank B. Исследование, разработка, производство и безопасность биосинтетического человеческого инсулина. Уход за диабетом. 1993;16(3):133–142. [PubMed] [Google Scholar]
60. Chance R, Glazer N, Wishner K. Insulin Lispro (Humalog) In: Walsh G, Murphy B, editors. Биофармацевтика, промышленная перспектива. Клювер: Дордрехт; 1999. С. 149–172. [Google Scholar]
61. Бланделл Т., Додсон Г., Ходжкин Д., Меркола Д. Инсулин: структура в кристалле и ее отражение в химии и биологии. Adv Prot Chem. 1972; 26: 279–402. doi: 10.1016/S0065-3233(08)60143-6. [CrossRef] [Google Scholar]
62. Kang S, Creagh F, Peters J, Brange J, Volund A, Owens D. Сравнение подкожного растворимого человеческого инсулина и аналогов инсулина на колебания уровня глюкозы в плазме, связанные с приемом пищи, у пациентов с диабетом 1-го типа. Уход за диабетом. 1991;14:571–577. doi: 10.2337/diacare.14.7.571. [PubMed] [CrossRef] [Google Scholar]
Уход за диабетом. 1991;14:571–577. doi: 10.2337/diacare.14.7.571. [PubMed] [CrossRef] [Google Scholar]
63. Брандж Дж., Рибель Дж., Хансен Дж.Ф., Додсон Г., Хансен М.Т., Хавелунд С., Мельберг С.Г., Норрис К., Норрис Л., Снел Л., Соренсен А.Р., Фойгт Х.О. Мономерные инсулины, полученные с помощью белковой инженерии, и их медицинские последствия. Природа. 1988; 333: 679–682. doi: 10.1038/333679a0. [PubMed] [CrossRef] [Google Scholar]
64. Brange J, Owens DR, Kang S, Volund A. Мономерные инсулины и их экспериментальное и клиническое значение. Уход за диабетом. 1990;13(9):923–954. doi: 10.2337/diacare.13.9.923. [PubMed] [CrossRef] [Google Scholar]
65. Wildt S, Gerngross TU. Гуманизация путей N-гликозилирования у дрожжей. Нат микробиол. 2005;3:119–128. doi: 10.1038/nrmicro1087. [PubMed] [CrossRef] [Google Scholar]
66. Гринна Л.С., Чопп Дж.Ф. Распределение по размерам и общие структурные особенности N-связанных олигосахаридов метилотрофных дрожжей Pichia pastoris. Дрожжи. 1989; 5: 107–115. doi: 10.1002/yea.320050206. [PubMed] [CrossRef] [Академия Google]
Дрожжи. 1989; 5: 107–115. doi: 10.1002/yea.320050206. [PubMed] [CrossRef] [Академия Google]
67. Tschopp JF, Sverlow G, Kosson R, Craig W, Grinna L. Высокий уровень секреции гликозилированной инвертазы у метилотрофных дрожжей pichia pastoris. Биотехнология. 1987; 5: 1305–1308. doi: 10.1038/nbt1287-1305. [CrossRef] [Google Scholar]
68. Ellis SB, Brust PF, Koutz PJ, Waters AF, Harpold MM, Gingeras TR. Выделение алкогольоксидазы и двух других генов, регулируемых метанолом, из дрожжей Pichia pastoris. Мол Селл Биол. 1985; 5: 1111–1121. [Бесплатная статья PMC] [PubMed] [Google Scholar]
69. Tschopp JF, Brust PF, Cregg JM, Stillman C, Gingeras TR. Экспрессия гена lacZ из двух промоторов, регулируемых метанолом, у Pichia pastoris. Нуклеиновые Кислоты Res. 1987; 15: 3859–3876. doi: 10.1093/нар/15.9.3859. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
70. Порро Д., Гассер Б., Фоссати Т., Маурер М., Брандуарди П., Зауэр М., Маттанович Д. Производство рекомбинантных белков и метаболитов в дрожжах. Приложение Microbiol Biotechnol. 2011; 89: 939–948. doi: 10.1007/s00253-010-3019-з. [PubMed] [CrossRef] [Google Scholar]
Приложение Microbiol Biotechnol. 2011; 89: 939–948. doi: 10.1007/s00253-010-3019-з. [PubMed] [CrossRef] [Google Scholar]
71. Shin CS, Hong MS, Bae CS, Lee J. Повышенная продукция человеческого мини-проинсулина в культурах с подпиткой при высокой плотности клеток Escherichia coli BL21(DE3)[pET-3aT2M2] Biotechnol Prog. 1997; 13: 249–257. doi: 10.1021/bp970018m. [PubMed] [CrossRef] [Google Scholar]
72. Mergulhao F, Taipa M, Cabral J, Monteiro G. Оценка узких мест в секреции проинсулина Escherichia coli. Дж Биотехнолог. 2004; 109:31–43. doi: 10.1016/j.jbiotec.2003.10.024. [PubMed] [CrossRef] [Академия Google]
73. Гуррамконда С., Полез С., Скоко Н., Аднан А., Гэйбл Т., Чу Д., Сваминатан С., Ханна Н., Тисминецки С., Ринас У. Применение простого метода периодической подпитки к высокоуровневому секреторному производству предшественника инсулина с использованием Pichia pastoris с последующей очисткой и преобразованием в человеческий инсулин. Факт микробной клетки. 2010;9:31. дои: 10.1186/1475-2859-9-31. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
дои: 10.1186/1475-2859-9-31. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
74. Owens DR, Vora JP, Dolben J. Человеческий инсулин и не только: обзор технологии полусинтеза и рекомбинантной ДНК. В: Pickup JC, редактор. Биотехнология инсулинотерапии. Оксфорд: Блэквелл; 1991. стр. 24–41. [Google Scholar]
75. Фрэнк Б. Манипулирование положением пролина в В-цепи привело к получению мономерных инсулинов. Диабет. 1991; 40 (Приложение 1): 423A. [Google Scholar]
76. Kurtzhals P, Havelund S, Jonassen S, Markussen J. Влияние жирных кислот и некоторых лекарств на связывание альбумина ацилированного аналога инсулина длительного действия. Дж. Фарм. 1997;86(12):1365–1368. doi: 10.1021/js9701768. [PubMed] [CrossRef] [Google Scholar]
77. Owens DR, Zinman B, Bolli G. Инсулины сегодня и в будущем. Ланцет. 2001;358:739–746. doi: 10.1016/S0140-6736(01)05842-1. [PubMed] [CrossRef] [Google Scholar]
78. Havelund S, Plum A, Ribel U, Jonassen I, Volund A, Markussen J, Kurtzhals P. Механизм пролонгации действия инсулина детемира, ацилированного аналога человеческого инсулина длительного действия. Фарм Рез. 2004;21(8):1498–1504. doi: 10.1023/B:PHAM.0000036926.54824.37. [PubMed] [CrossRef] [Google Scholar]
Механизм пролонгации действия инсулина детемира, ацилированного аналога человеческого инсулина длительного действия. Фарм Рез. 2004;21(8):1498–1504. doi: 10.1023/B:PHAM.0000036926.54824.37. [PubMed] [CrossRef] [Google Scholar]
79. Hou J, Tyo KEJ, Liu Z, Petranovic D, Nielsen J. Метаболическая инженерия секреции рекомбинантных белков Saccharomyces cerevisiae. FEMS Yeast Res. 2012;12:491–510. doi: 10.1111/j.1567-1364.2012.00810.x. [PubMed] [CrossRef] [Google Scholar]
80. Kjeldsen T, Hach M, Balschmidt P, Havelund S, Pettersson AF, Markussen J. Препролидеры, лишенные N-связанного гликозилирования для секреторной экспрессии в дрожжах Saccharomyces cerevisiae. Protein Expr Purif. 1998; 14: 309–316. doi: 10.1006/преп.1998.0977. [PubMed] [CrossRef] [Google Scholar]
81. Staub JM, Garcia B, Graves J, Hajdukiewicz PT, Hunter P, Nehra N, Paradkar V, Schlittler M, Carroll JA, Spatola L, Ward D, Ye G, Russell DA. Высокопродуктивная продукция терапевтического белка человека в хлоропластах табака.