Схема строения АТФ, основные ее функции и свойства в организме
Как устроена АТФ и каковы ее функции
Определение и строение АТФ
Что такое АТФ?
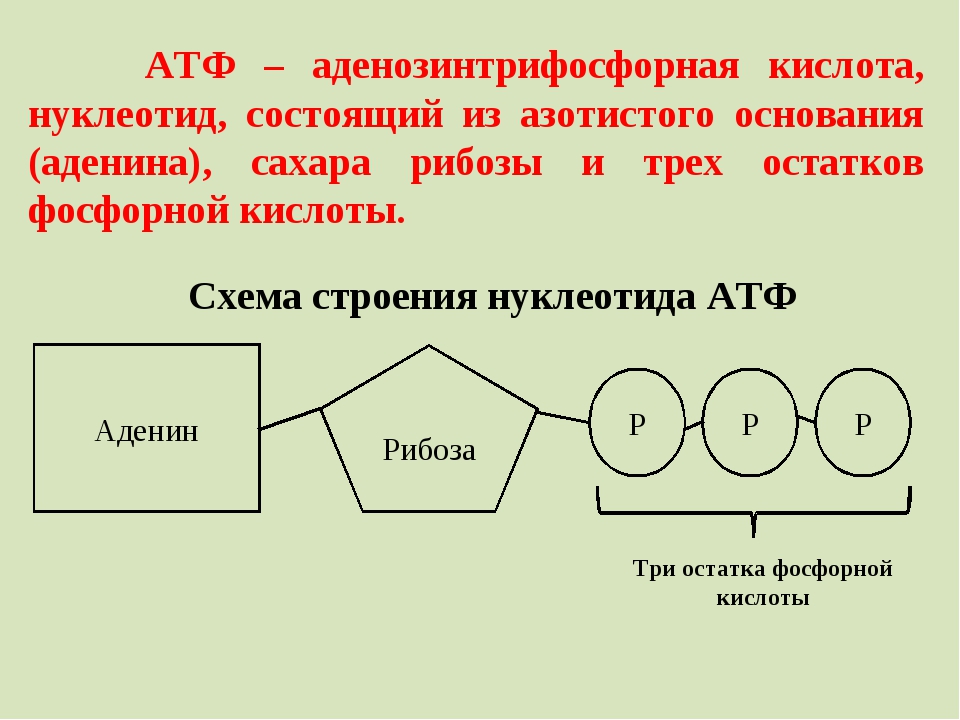
Определение 1АТФ — это аденозинтрифосфорная кислота, которая является универсальным источником энергии клеток.
АТФ — поставщик энергии для всех биохимических процессов, происходящих внутри живых систем. В частности, это неотъемлемая часть образования ферментов. Открытие вещества произошло в 1929 году в Гарвардской медицинской школе.
Химическая структура АТФ представляет собой оригинальное соединение эфира аденозина, а также оригинальных производных рибозы и аденина. Соединение азотистого основания пурина с углеродом рибозы происходит при помощи гликозидной связи. К другому углероду рибозы присоединяется фосфорная кислота (в составе 3-молекул). Они обозначаются буквами ɑ, β и γ.
АТФ также относят к соединениям с высокой степенью энергетической емкости. Вещество содержит связи, высвобождающие максимальное количество энергии. Гидролиз макроэргической связи в молекуле АТФ происходит с параллельным отщеплением 1-2 остатков фосфорной кислоты, которые способствуют выработке до 60 кДж/моль энергетических молекул.
Гидролиз макроэргической связи в молекуле АТФ происходит с параллельным отщеплением 1-2 остатков фосфорной кислоты, которые способствуют выработке до 60 кДж/моль энергетических молекул.
Энергия, полученная в результате, задействуется в различных процессах, требующих энергетических затрат.
Функции АТФ
В организме АТФ отводится несколько важных функций:
- поставляет энергию в организм, с помощью которой протекают различные химические реакции;
- переносит две богатые энергией химические связи, которые обеспечивают биохимические и физиологические процессы;
- переносит биологические мембраны. Одна из целей такого переноса — формирование определенного энергетического потенциала между несколькими мембранами;
- осуществление мышечного сокращения.
Кроме этого, АТФ может выступать:
- в качестве исходного продукта для создания разнообразных нуклеиновых кислот;
- как пусковой механизм для нескольких ферментов в случае присоединения к их активным центрам;
- в качестве субстрата для запуска циклического процесса вторичного посредника, который отвечает за транспортировку сигналов от гормонов в клетку;
- как медиатор в синапсах и сигнальное вещество в пуринэргической передаче сигнала.
Основные свойства АТФ
Синтез АТФ может происходить путем фосфорилирования АДФ. Есть 3 способа:
- Окислительное фосфорилирование.
- Фотофосфорилирование. Оно осуществляется в процессе фотосинтеза в хлоропластах растений.
- Субстратное фосфорилирование.
Первый вариант — путь метаболизма, суть которого заключается в непрерывном потоке энергии, образующейся при окислении различных питательных веществ.
Второй вариант — процесс синтеза АТФ из АДФ при помощи энергии света.
Замечание 2Оба способа реализуются в случае окисления веществ.
Большая часть АТФ формируется на мембранах митохондрий в процессе окислительного фосфорилирования. В случае субстратного фосфорилирования АДФ не подразумевает участия мембранных ферментов. Этот процесс протекает в цитоплазме в ходе гликолиза, а также при переносе фосфатной группы с различных макроэргических соединений.
Как источники энергии, реакции фосфорилирования АТФ и АДФ формируют циклический процесс — он представляет собой суть энергетического обмена. АТФ как источник энергии в организме человека запускает циклический процесс — он является сутью энергетического обмена. Можно сделать вывод, что АТФ является конечной точкой циклов энергетического обмена.
АТФ как источник энергии в организме человека запускает циклический процесс — он является сутью энергетического обмена. Можно сделать вывод, что АТФ является конечной точкой циклов энергетического обмена.
Отмечается, что АТФ — наиболее часто обновляемое вещество. Молекула АТФ живет менее 60 секунд. В течение суток одна молекула АТФ проходит 2-3 тысячи ресинтезов.
В день человеческий организм способен синтезировать до 40 кг АТФ. Это значит, что запасы АТФ в организме не откладываются, что вынуждает для нормальной жизнедеятельности постоянно синтезировать новые молекулы АТФ.
Синтез АТФ происходит в процессе дыхания с помощью химической энергии, которая высвобождается при окислении таких органических веществ как глюкоза, а также во время фотосинтеза — с помощью солнечной энергии. Накопление АТФ осуществляется в складках внутренней мембраны митохондрий внутри крист.
Все сбои, происходящие в организме, нужно анализировать с точки зрения наличия определенного количества АТФ в клетках. Если наблюдается дисбаланс энергии, стоит делать клеточный анализ и оценку структур развития организма с точки зрения комплексного подхода.
Если наблюдается дисбаланс энергии, стоит делать клеточный анализ и оценку структур развития организма с точки зрения комплексного подхода.
Функции, строение и процесс накопления тесно связаны с мембранами крист в присутствии кислорода. Образованная в результате бескислородного расщепления глюкозы пировиноградная кислота, окисляется до конечных продуктов СО₂ и НО₂.
Этот многоступенчатый ферментативный процесс получил название цикла Кребса и цикла трикарбоновых кислот.
Важно отметить:
- при распаде 2-х молекул пировиноградной кислоты происходит образование 36 молекул АТФ;
- 2 молекулы АТФ запасаются в процессе бескислородного расщепления каждой молекулы;
- в результате окислительного фосфорилирования происходит образование энергии АТФ в 18 раз больше, чем в процессе гликолиза.
Особенность процесса накопления АТФ в клетке — понимание ее как энергетического носителя, а не как депо клетки.
Чтобы энергия была сохранена на длительное время, нужно наличие в клетке определенных веществ: жиров и гликогена. Клетки организма имеют чувствительность к изменениям уровня АТФ. При возрастании скорости использования этой молекулы, процесс дыхания становится более интенсивным.
Клетки организма имеют чувствительность к изменениям уровня АТФ. При возрастании скорости использования этой молекулы, процесс дыхания становится более интенсивным.
Роль АТФ как связующего звена между клеточным дыханием и требующими затрат энергии процессами видна на схеме строения АТФ.
Так как в АТФ нуждаются все клетки, то она считается универсальным носителем энергии. С помощью АТФ происходит поставка энергии для различных процессов: мышечного сокращения, передачи нервных импульсов, активного транспорта и синтеза белков, других типов клеточной активности. Все, что необходимо от вещества — быть подключенным к соответствующей части аппарата клетки.
АТФ есть во всех живых клетках, он доставляет энергию к каждой части клетки и к любому процессу, который нуждается в энергообеспечении.
Строение и функции АТФ — Строение и функции АТФ
Комментарии преподавателяКак вы помните, нуклеиновые кислотысостоят из нуклеотидов. Оказалось, что в клетке нуклеотиды могут находиться в связанном состоянии или в свободном состоянии. В свободном состоянии они выполняют ряд важных для жизнедеятельности организма функций.
Оказалось, что в клетке нуклеотиды могут находиться в связанном состоянии или в свободном состоянии. В свободном состоянии они выполняют ряд важных для жизнедеятельности организма функций.
К таким свободным нуклеотидам относится молекула АТФ или аденозинтрифосфорная кислота (аденозинтрифосфат). Как и все нуклеотиды, АТФ состоит из пятиуглеродного сахара – рибозы, азотистого основания – аденина, и, в отличие от нуклеотидов ДНК и РНК, трех остатков фосфорной кислоты
fs.nashaucheba.ru
Важнейшая функция АТФ состоит в том, что она является универсальным хранителем и переносчиком энергии в клетке.
Все биохимические реакции в клетке, которые требуют затрат энергии, в качестве ее источника используют АТФ.
При отделении одного остатка фосфорной кислоты, АТФ переходит в АДФ (аденозиндифосфат). Если отделяется ещё один остаток фосфорной кислоты (что случается в особых случаях), АДФ переходит в АМФ (аденозинмонофосфат)
fs.nashaucheba.ru
При отделении второго и третьего остатков фосфорной кислоты освобождается большое количество энергии, до 40 кДж. Именно поэтому связь между этими остатками фосфорной кислоты называют макроэргической и обозначают соответственным символом.
При гидролизе обычной связи выделяется (или поглощается) небольшое количество энергии, а при гидролизе макроэргической связи выделяется намного больше энергии (40 кДж). Связь между рибозой и первым остатком фосфорной кислоты не является макроэргической, при её гидролизе выделяется всего 14 кДж энергии.
Макроэргические соединения могут образовываться и на основе других нуклеотидов, например ГТФ (гуанозинтрифосфат) используется как источник энергии в биосинтезе белка, принимает участие в реакциях передачи сигнала, является субстратом для синтеза РНК в процессе транскрипции, но именно АТФ является наиболее распространенным и универсальным источником энергии в клетке.
АТФ содержится как в цитоплазме, так и в ядре, митохондриях и хлоропластах.
Таким образом, мы вспомнили, что такое АТФ, каковы её функции, и что такое макроэргическая связь.
Витамины – биологически активные органические соединения, которые в малых количествах необходимы для подержания процессов жизнедеятельности в клетке.
Они не являются структурными компонентами живой материи, и не используются в качестве источника энергии.
Большинство витаминов не синтезируются в организме человека и животных, а поступают в него с пищей, некоторые синтезируются в небольших количествах микрофлорой кишечника и тканями (витамин D синтезируется кожей).
Потребность человека и животных в витаминах не одинакова и зависит от таких факторов как пол, возраст, физиологическое состояние и условия среды обитания. Некоторые витамины нужны не всем животным.
Например, аскорбиновая кислота, или витамин С, необходим человеку и другим приматам. Вместе с тем, он синтезируется в организме рептилий (моряки брали в плавания черепах, для борьбы с цингой – авитаминозом витамина С).
Витамины были открыты в конце XIX века благодаря работам русских ученых Н. И. Лунина и В. Пашутина, которые показали, что для полноценного питания необходимо не только наличие белков, жиров и углеводов, но и ещё каких-то других, на тот момент неизвестных, веществ.
В 1912 году польский ученый К. Функ (Рис. 3), изучая компоненты шелухи риса, предохраняющей от болезни Бери-Бери (авитаминоз витамина В), предположил, что в состав этих веществ обязательно должны входить аминные группировки. Именно он предложили назвать эти вещества витаминами, то есть аминами жизни.
В дальнейшем было установлено, что многие из этих веществ аминогрупп не содержат, но термин витамины хорошо прижился в языке науки и практики.
По мере открытия отдельных витаминов, их обозначали латинскими буквами и называли в зависимости от выполняемых функций. Например, витамин Е назвали токоферол (от др.-греч. τόκος – «деторождение», и φέρειν – «приносить»).
Сегодня витамины делят по их способности растворяться в воде или в жирах.
К водорастворимым витаминам относят витамины H, C, P, В.
К жирорастворимым витаминам относят A, D, E, K(можно запомнить, как слово: кеда).
Как уже было отмечено, потребность в витаминах зависит от возраста, пола, физиологического состояния организма и среды обитания. В молодом возрасте отмечена явная нужда в витаминах. Ослабленный организм тоже требует больших доз этих веществ. С возрастом способность усваивать витамины падает.
Потребность в витаминах также определяется способностью организма их утилизировать.
В 1912 году польский ученый Казимир Функ получил из шелухи риса частично очищенный витамин B1 – тиамин. Ещё 15 лет понадобилось для получения этого вещества в кристаллическом состоянии.
Кристаллический витамин B1 бесцветен, обладает горьковатым вкусом и хорошо растворим в воде. Тиамин найден как в растительных, так и микробных клетках. Особенно много его в зерновых культурах и дрожжах
Тиамин найден как в растительных, так и микробных клетках. Особенно много его в зерновых культурах и дрожжах
Тиамин в виде таблеток и в продуктах питания — fibromyalgialiving.today
Термическая обработка пищевых продуктов и различные добавки разрушают тиамин. При авитаминозе наблюдаются патологии нервной, сердечно-сосудистой и пищеварительной систем. Авитаминоз приводит к нарушению водного обмена и функции кроветворения. Один из ярких примеров авитаминоза тиамина – это развитие болезни Бери-Бери
Витамин В1 широко применяется в медицинской практике для лечения различных нервных заболеваний, сердечно-сосудистых расстройств.
В хлебопечении тиамин вместе с другим витаминами – рибофлавином и никотиновой кислотой используется для витаминизации хлебобулочных изделий.
В 1922 году Г. Эванс и А. Бишо открыли жирорастворимый витамин, названный ими токоферолом или витамином Е (дословно: «способствующий родам»).
Бишо открыли жирорастворимый витамин, названный ими токоферолом или витамином Е (дословно: «способствующий родам»).
Витамин Е в чистом виде – маслянистая жидкость. Он широко распространен в злаковых культурах, например в пшенице. Его много в растительных, животных жирах
Много витамина E в моркови, в яйцах и молоке. Витамин E является антиоксидантом, то есть защищает клетки от патологического окисления, которое приводит их к старению и гибели. Он является «витамином молодости». Огромно значение витамина для половой системы, поэтому его часто называют витамином размножения.
Вследствие этого, дефицит витамина Е, в первую очередь, приводит к нарушению эмбриогенеза и работы репродуктивных органов.
Производство витамина Е основано на выделении его из зародышей пшеницы – методом спиртовой экстракции и отгонки растворителей при низких температурах.
В медицинской практике используют как природные, так и синтетические препараты – токоферолаацетат в растительном масле, заключенный в капсулу (знаменитый «рыбий жир»).
Препараты витамина Е используются как антиоксиданты при облучениях и других патологических состояниях, связанных с повышенным содержанием в организме ионизированных частиц и активных форм кислорода.
Кроме того, витамин Е назначают беременным женщинам, а также используют в комплексной терапии лечения бесплодия, при мышечной дистрофии и некоторых заболеваниях печени.
Витамин А был открыт Н. Друммондом в 1916 году.
Этому открытию предшествовали наблюдения за наличием жирорастворимого фактора в пище, необходимого для полноценного развития сельскохозяйственных животных.
Витамин А недаром занимает первое место в витамином алфавите.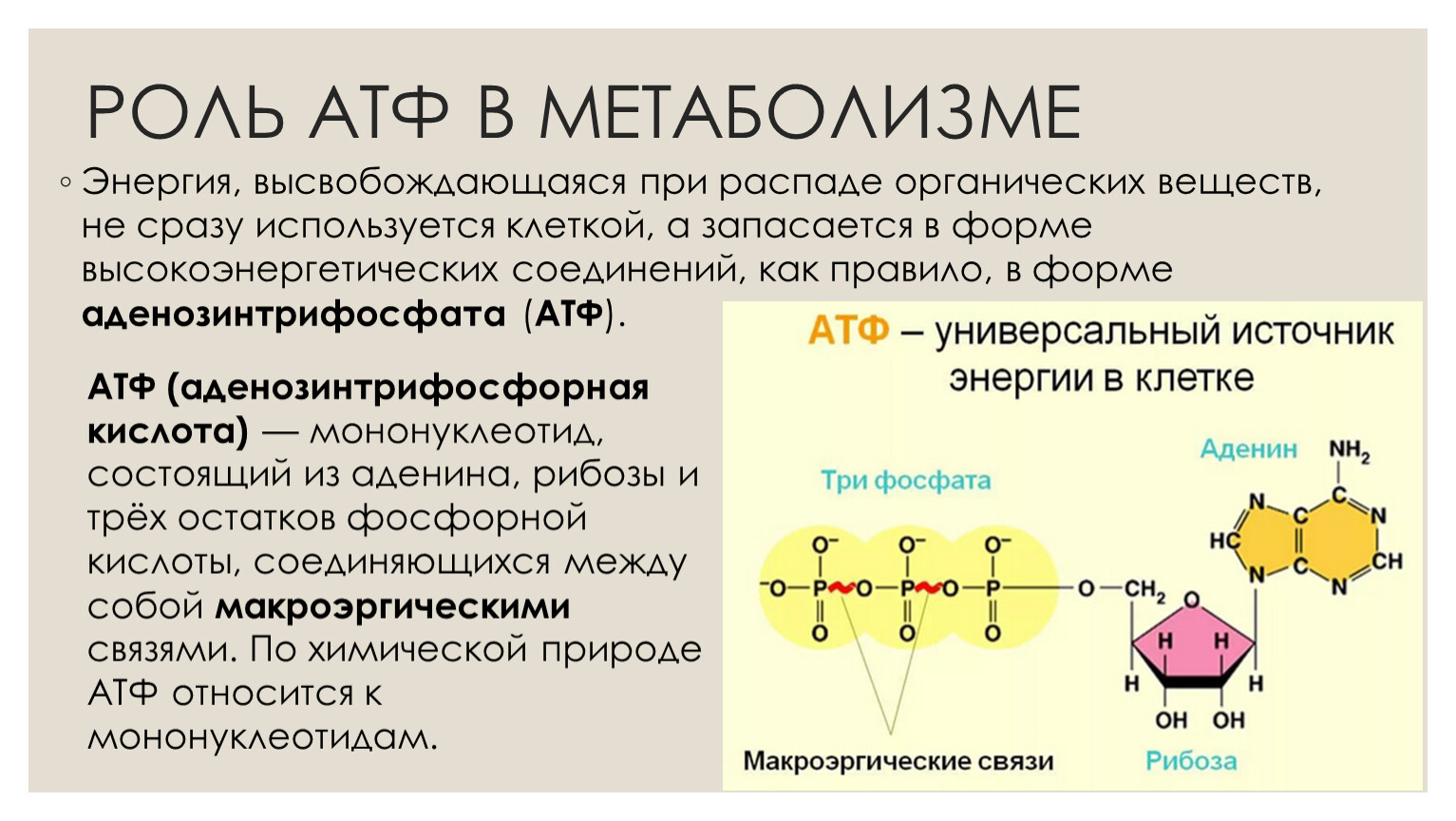 Он участвует практически во всех процессах жизнедеятельности. Этот витамин необходим для восстановления и сохранения хорошего зрения.
Он участвует практически во всех процессах жизнедеятельности. Этот витамин необходим для восстановления и сохранения хорошего зрения.
Он также помогает вырабатывать иммунитет ко многим заболеваниям, в том числе и простудным.
Без витамина А невозможно здоровое состояние эпителия кожи. Если у вас «гусиная кожа», которая чаще всего появляется на локтях, бедрах, коленях, голенях, если появилась сухость кожи на руках или возникают другие подобные явления, это означает, что вам недостает витамина А.
Витамин А, как и витамин Е, необходим для нормального функционирования половых желез (гонад). При гиповитаминозе витамина А отмечено повреждение репродуктивной системы и органов дыхания.
Одним из специфических последствий недостатка витамина А является нарушение процесса зрения, в частности снижение способности глаз к темновой адаптации – куриная слепота. Авитаминоз приводит к возникновению ксерофтальмии и разрушению роговицы. Последний процесс необратим, и характеризуется полной потерей зрения. Гипервитаминоз приводит к воспалению глаз и нарушению волосяного покрова, потери аппетита и полному истощению организма.
Авитаминоз приводит к возникновению ксерофтальмии и разрушению роговицы. Последний процесс необратим, и характеризуется полной потерей зрения. Гипервитаминоз приводит к воспалению глаз и нарушению волосяного покрова, потери аппетита и полному истощению организма.
Витамины группы А, в первую очередь, содержатся в продуктах животного происхождения: в печени, в рыбьем жире, в масле, в яйцах
infourok.ru
В продуктах растительного происхождения содержатся каротиноиды, которые в организме человека под действием фермента каротиназы переходят в витамин А.
Таким образом, Вы познакомились сегодня со структурой и функциями АТФ, а также вспомнили о значении витаминов и выяснили, как некоторые из них участвуют в процессах жизнедеятельности.
При недостаточном поступлении витаминов в организм развивается первичный авитаминоз. Разные продукты содержат разное количество витаминов.
Разные продукты содержат разное количество витаминов.
Например, морковь содержит много провитамина А (каротина), капуста содержит витамин С и т. д. Отсюда проистекает необходимость сбалансированной диеты, включающей в себя разнообразные продукты растительного и животного происхождения.
Авитаминоз при нормальных условиях питания встречается очень редко, гораздо чаще встречаются гиповитаминозы, которые связаны с недостаточным поступлением с пищей витаминов.
Гиповитаминоз может возникать не только в результате несбалансированного питания, но и как следствие различных патологий со стороны желудочно-кишечного тракта или печени, или в результате различных эндокринных или инфекционных заболеваний, которые приводят к нарушению всасывания витаминов в организме.
Некоторые витамины вырабатываются кишечной микрофлорой (микробиотой кишечника). Подавление биосинтетических процессов в результате действия антибиотиков может также привести к развитию гиповитаминоза, как следствия дисбактериоза.
Чрезмерное употребление пищевых витаминных добавок, а также лекарственных средств, содержащих витамины, приводит к возникновению патологического состояния – гипервитаминоза. Особенно это характерно для жирорастворимых витаминов, таких как A, D, E, K.
источник конспекта — http://interneturok.ru/ru/school/biology/10-klass/bosnovy-citologii-b/stroenie-i-funktsii-atf?seconds=0&chapter_id=98
источник видео — http://www.youtube.com/watch?v=XLwiY5dkoY8
источник виедо — http://www. youtube.com/watch?v=aExflgKux3o
youtube.com/watch?v=aExflgKux3o
источник видео — http://www.youtube.com/watch?v=RaWqk7FSPpE
источник видео — http://www.youtube.com/watch?v=Wx-t6t01PuQ
источник видео — http://www.youtube.com/watch?v=YX3631pv1Wk
источник видео — http://www.youtube.com/watch?v=SIKsIW2HVyY
источник видео — http://www.youtube.com/watch?v=BeSyX2QU6x4
источник видео — http://www.youtube.com/watch?v=j1Zq5HFKXCE
источник презентации — http://www.myshared.ru/slide/download/
АТФ – определение, структура, производство, синтез, функции
АТФ (аденозинтрифосфат) представляет собой молекулу пирофосфата, которая обеспечивает энергию для проведения метаболических процессов, т. е. поддержания жизни клетки.
Комплексное органическое высокоэнергетическое соединение, дающее энергию для проведения метаболических процессов. Он упоминается как «молекулярная единица валюты » внутриклеточной передачи энергии или «энергетическая валюта клетки 9». 0004» или « единица энергии ячейки ». Это основной источник энергии для использования и хранения внутри каждой клетки.
0004» или « единица энергии ячейки ». Это основной источник энергии для использования и хранения внутри каждой клетки.
Это сложная органическая молекула, состоящая из фрагментов аденина, рибозы и трифосфата. Энергия, высвобождаемая при клеточном дыхании, улавливается в виде двух фосфодиэфирных связей в молекуле АТФ. Во время гидролиза этих высокоэнергетических фосфодиэфирных связей в молекулах АТФ высвобождается энергия, которая затем используется для клеточной деятельности.
Название IUPAC : Аденозин 5′-(тетрагидрогентрифосфат)
Молекулярная формула: C 10 H 16 N 5 O 13 90 024 P 3
Молекулярный вес : 507,18 г/ моль
Плотность: 1,04 г/см 3
Растворимость : Водорастворимый
Содержание
Структура АТФ Структура АТФ Состоит из аденина, рибозы и трифосфатный фрагмент. Аденозин присоединяется к 9-атом азота к 1-атому углерода рибозы, которая, в свою очередь, присоединена к 5-углеродному атому сахара к трифосфатной группе. Три фосфатные группы образуют трифосфатную группу. Их называют альфа (α), бета (β) и гамма (γ) фосфатными группами. Есть три фосфодиэфирные связи; один между фосфатными группами, второй между фосфатными группами и третий между фосфатом и сахаром рибозы. Первые два представляют собой высокоэнергетическую фосфодиэфирную связь и выделяют энергию при гидролизе. Следовательно, гидролиз АТФ до АДФ (аденозиндифосфата) и снова до АМФ (аденозинмонофосфата) дает энергию, но разрыв фосфодиэфирной связи между рибозой и фосфатом требует энергии.
Аденозин присоединяется к 9-атом азота к 1-атому углерода рибозы, которая, в свою очередь, присоединена к 5-углеродному атому сахара к трифосфатной группе. Три фосфатные группы образуют трифосфатную группу. Их называют альфа (α), бета (β) и гамма (γ) фосфатными группами. Есть три фосфодиэфирные связи; один между фосфатными группами, второй между фосфатными группами и третий между фосфатом и сахаром рибозы. Первые два представляют собой высокоэнергетическую фосфодиэфирную связь и выделяют энергию при гидролизе. Следовательно, гидролиз АТФ до АДФ (аденозиндифосфата) и снова до АМФ (аденозинмонофосфата) дает энергию, но разрыв фосфодиэфирной связи между рибозой и фосфатом требует энергии.
АТФ представляет собой богатое энергией соединение, в основном синтезируемое в процессе клеточного дыхания в аэробных и анаэробных клетках. Окисление глюкозы, липидов (жиров) и аминокислот приводит к образованию молекул АТФ внутри клеток. Энергия, высвобождаемая при окислении этих питательных веществ, улавливается в форме высокоэнергетической фосфодиэфирной связи в молекуле АТФ.
Углеводы являются основным источником энергии. Углеводы, потребляемые в различных формах (крахмал, сахароза, декстроза, лактоза, фруктоза и т. д.), в основном расщепляются до моносахаридной формы «глюкозы». Затем глюкоза подвергается метаболическим реакциям, гликолизу, циклу Кребса и окислительному фосфорилированию и окисляется до высвобождать энергию. Эта высвободившаяся энергия улавливается и сохраняется в виде АТФ.
Точно так же метаболизм белков и липидов также производит простые конечные продукты, такие как ацетил-КоА, сукцинил-КоА, кетокислоты, аммиак и т. д., которые затем подвергаются циклу Кребса и окислительному фосфорилированию с образованием молекул АТФ.
Механизмы синтеза АТФ Синтез АТФ происходит во время нескольких клеточных процессов, включая реакции фосфорилирования. Это может происходить как в аэробных, так и в анаэробных условиях. Важными способами производства АТФ являются; клеточное дыхание (окислительное фосфорилирование, фосфорилирование на уровне субстрата), бета-окисление и катаболизм липидов, катаболизм белков, фотофосфорилирование и ферментация.
Это процесс, при котором глюкоза катаболизируется в ацетил-КоА и подвергается окислительному фосфорилированию для синтеза АТФ. Это основной механизм синтеза большей части АТФ, необходимой клетке. Производство АТФ посредством клеточного дыхания происходит в два разных этапа;
а. Фосфорилирование на уровне субстратаПроизводство АТФ происходит непосредственно во время гликолиза. В гликолитическом пути окисление G-3-P ферментом G-3-P-дегидрогеназой добавляет высокоэнергетическую фосфатную группу, которая переносится на АДФ в следующей реакции с образованием молекулы АТФ.
В другой реакции энергия, высвобождаемая при дегидратации 2-фосфоглицерата, преобразует низкоэнергетическую фосфатную связь в высокоэнергетическую фосфатную связь, которая передается АДФ в следующей реакции с образованием молекулы АТФ.
Затем пируват окисляется до молекулы ацетил-КоА с помощью комплексов пируватдегидрогеназы. Образовавшийся таким образом ацетил-КоА затем подвергается циклу Кребса, где он окисляется с образованием одного эквивалента АТФ, то есть молекулы ГТФ, трех молекул НАДН и одной молекулы ФАДН 9.0023 2 . Эти молекулы NADH и FADH 2 являются переносчиками электронов, которые войдут в ЭТЦ (цепь переноса электронов) и произведут молекулы АТФ.
Образовавшийся таким образом ацетил-КоА затем подвергается циклу Кребса, где он окисляется с образованием одного эквивалента АТФ, то есть молекулы ГТФ, трех молекул НАДН и одной молекулы ФАДН 9.0023 2 . Эти молекулы NADH и FADH 2 являются переносчиками электронов, которые войдут в ЭТЦ (цепь переноса электронов) и произведут молекулы АТФ.
Промежуточные соединения, такие как НАДН и ФАДН 2 , образующиеся во время гликолиза, декарбоксилирования пирувата и цикла Кребса, используются в качестве переносчиков электронов и подвергаются в качестве субстрата цепи переноса электронов (ЭТЦ), генерирующей протонный градиент. Протонный градиент сочетается с хемиосмосом, при котором фермент АТФ-синтаза синтезирует АТФ.
2. ФотофосфорилированиеЭто процесс, при котором энергия света используется для фосфорилирования АДФ в АТФ внутри хлорофиллсодержащих клеток. Общая реакция фотофосфорилирования может быть выражена как:
АДФ + световая энергия + Pi → АТФ
Она бывает двух типов; циклическое и нециклическое фотофосфорилирование.
Это процесс фотофосфорилирования, при котором электроны, высвобождаемые пигментом P700 Фотосистемы-I, возвращаются обратно в Фотосистему-I. Высвобожденный электрон подвергается воздействию ЭТЦ, который создает протонный градиент, который используется для производства АТФ с помощью АТФ-синтазы в процессе, называемом хемиосмосом. Преимущественно это происходит в бактериальных клетках.
б. Нециклическое фотофосфорилирование Это процесс фотофосфорилирования, при котором высвобожденные электроны не возвращаются обратно в фотосистему, которая их производит. В этом механизме обе фотосистемы-I и –II возбуждаются одновременно. Электроны, высвобождаемые P680 фотосистемы-II, проходят через ETC, генерируя АТФ, путем фосфорилирования АДФ ферментом АТФ-синтазой при хемиосмосе. Затем электроны используются для замены электронов, потерянных P700 фотосистемы-II во время фотовозбуждения. Затем электроны, высвобождаемые фотосистемой-II, используются для восстановления НАДФ+ до НАДФН. Это преимущественно происходит в растительных клетках и вызывает высвобождение одного O 2 молекулы на каждом этапе.
Это преимущественно происходит в растительных клетках и вызывает высвобождение одного O 2 молекулы на каждом этапе.
Это катаболическая реакция, при которой жирные кислоты окисляются до ацетил-КоА, которые затем подвергаются циклу Кребса и ЭТС одновременно для образования АТФ. В каждом цикле бета-окисления образуется один ацетил – КоА, НАДН и ФАДН 2 . Эти промежуточные продукты затем дополнительно метаболизируются с высвобождением АТФ в цикле Кребса и в процессах окислительного фосфорилирования.
4. Ферментация Это процесс производства органической кислоты или спирта путем восстановления пирувата, образующегося при гликолизе сахара (глюкозы). Это происходит в процессе анаэробного дыхания. Это процесс фосфорилирования на уровне субстрата, при котором 2 молекулы АТФ образуются из одной молекулы глюкозы. Конечным продуктом является либо молочная кислота, либо этанол. Эти продукты не могут вступать в окислительное фосфорилирование из-за недостатка кислорода. Следовательно, больше молекул АТФ не образуется. Следовательно, он менее эффективен, чем процесс аэробного дыхания в образовании АТФ.
Следовательно, больше молекул АТФ не образуется. Следовательно, он менее эффективен, чем процесс аэробного дыхания в образовании АТФ.
Это процесс катаболической реакции, при котором богатые энергией фосфодиэфирные связи молекул АТФ разрушаются (гидролизуются) с высвобождением энергии и молекул неорганического фосфата в присутствии воды и фермента АТФазы. Это экзергоническая реакция, при которой высвобождается энергия, накопленная в фосфодиэфирной связи во время образования АТФ. Эта высвобождаемая энергия используется клеткой для выполнения нескольких клеточных действий и реакций.
АТФ сначала гидролизуется, разрывая одну богатую энергией фосфодиэфирную связь с образованием АДФ. Молекула АДФ может далее гидролизоваться, разрывая другую богатую энергией фосфодиэфирную связь с образованием АМФ. Расщепление фосфодиэфирной связи катализируется ферментом АТФ-гидролазой (АТФазой) в присутствии воды. Гидролиз АТФ является обратимой реакцией, т. е. АДФ и АМФ могут рефосфорилироваться из молекулы АТФ.
е. АДФ и АМФ могут рефосфорилироваться из молекулы АТФ.
При гидролизе АТФ до АДФ выделяется 7,3 ккал/моль энергии. Его можно выразить следующим образом:
Гидролиз АТФ в АДФГде ∆G= свободная энергия Гиббса = – 7,3 ккал/моль энергии
Дальнейший гидролиз АДФ в АМФ высвобождает 7,5 ккал/моль энергии. Это может быть выражено как:
Гидролиз АДФ до АМФГде ∆G= Свободная энергия Гиббса = – 7,5 ккал/моль энергии
Общая реакция может быть резюмирована как:
Гидролиз АТФ Функции АТФ- АТФ играет важную роль в анаболических реакциях, обеспечивая энергию для формирования или разрушения костей. Это основной источник энергии для клеточных реакций и процессов. Энергия хранится и транспортируется в виде АТФ внутри живых клеток. Все другие формы химической энергии в клетке перед использованием преобразуются в АТФ.
- Жизненно важные процессы, такие как сокращение-расслабление мышц, движение клеток, передача импульсов, работа сердца, кровообращение и т.
 д., требуют гидролиза АТФ в качестве топлива.
д., требуют гидролиза АТФ в качестве топлива. - АТФ используется в качестве источника энергии для транспорта молекул в клетку и из нее во время активных транспортных механизмов.
- АТФ действует как внутриклеточный резервный источник энергии.
- АТФ участвует во внутриклеточных сигнальных процессах. Они служат субстратом для киназ переноса фосфата, ферментов аденилатциклазы и др. АТФ превращается в цАМФ (циклический АМФ), который действует как вторичные сигнальные молекулы во время внутриклеточных сигнальных процессов.
- АТФ также участвует во внеклеточной передаче сигналов и нейротрансмиссии. Во время процесса пуринергической передачи сигналов АТФ используется для связи между клетками. Он также служит нейротрансмиттером в нескольких нейронных сигнальных процессах.
- АТФ требуется для биосинтеза молекул ДНК и РНК. ДНК-гираза прокариот или ДНК-топоизомераза II требует АТФ в форме дАТФ (дезоксирибонуклеотид-аденозинтрифосфат).
- Он также участвует в реакциях синтеза белка, активируя ферменты аминоацил-тРНК-синтетазы.

- В клеточных мембранах присутствует несколько кассетных транспортеров, связывающих АТФ (транспортеры ABC), которые используют энергию связывания и гидролиза АТФ для клеточного транспорта, такого как поглощение витаминов, ионов металлов, предшественников биосинтеза и т. д., а также отток липидов, остатков лекарств, стеролов и т. д. .
- Инъекционные АТФ используются в качестве диагностических и терапевтических препаратов при некоторых заболеваниях сердца (сердечные брадиаритмии). Установлено, что
- АТФ действует как биологический гидротроп. АТФ может препятствовать термической агрегации белков и растворимости белков.
- АТФ также изучается на предмет его омолаживающих свойств и используется в препаратах против старения.
- Нельсон Д.Л. и Кокс М.М. (2017). Принципы биохимии Ленингера (7-е изд.). В.Х. Фриман.
- Сатьянараяна, У. (2013). Биохимия . Эльзевир Науки о здоровье.
 https://books.google.com.np/books?id=Bd9XAwAAQBAJ
https://books.google.com.np/books?id=Bd9XAwAAQBAJ - Данн Дж., Гридер М.Х. Физиология, Аденозинтрифосфат. [Обновлено 17 февраля 2022 г.]. В: StatPearls [Интернет]. Остров сокровищ (Флорида): StatPearls Publishing; 2022 янв. Доступно по адресу: https://www.ncbi.nlm.nih.gov/books/NBK553175/9.0176
- Национальный центр биотехнологической информации (2022 г.). Сводка соединений PubChem для CID 5957, аденозин-5′-трифосфат. Получено 2 апреля 2022 г. с сайта https://pubchem.ncbi.nlm.nih.gov/compound/Adenosine-5_-triphosphate.
- АТФ – энергетическая валюта клетки – структура и ее функции (byjus.com)
- Аденозинтрифосфат (АТФ) – определение, структура и функция (biologydictionary.net)
- Что такое АТФ – биология мудрая
- Синтез АТФ – NEET Biology Notes (byjus.com)
- СПС | Биология I (lumenlearning.com)
- Фотофосфорилирование: определение и типы – исследование QS
- Циклическое фотофосфорилирование и нециклическое фотофосфорилирование (byjus.
 com)
com) - Фотофосфорилирование | Биониндзя
- Фотофосфорилирование – обзор | Темы ScienceDirect
- Бета-окисление – определение, этапы и тест | Биологический словарь
- Бета-окисление жирных кислот: этапы и примеры — Online Biology Notes
- Ферментация | Общая биология в BCC (cuny.edu)
- Что такое гидролиз АТФ? (с картинками) (thehealthboard.com)
- blobs.org — Гидролиз АТФ
- Гидролиз и синтез АТФ (1.6.2) | Примечания к редакции AQA A Level Biology 2017 | Сохранить мои экзамены
- » Сколько энергии выделяется при гидролизе АТФ? (bionumbers.org)
- СПС | Структура, синтез, гидролиз, функции и резюме (alevelbiology.co.uk)
- Хах, Б.С., и Бернсток, Г. (2009 г.). Двойная жизнь АТФ. Scientific American , 301 (6), 84–92. https://doi.org/10.1038/scientificamerican1209-84
- Пеллег А., Куталек С.
 П., Фламманг Д. и др. ATPace™: аденозин-5′-трифосфат для инъекций. Пуринергическая сигнализация 8, 57–60 (2012). https://doi.org/10.1007/s11302-011-9268-1
П., Фламманг Д. и др. ATPace™: аденозин-5′-трифосфат для инъекций. Пуринергическая сигнализация 8, 57–60 (2012). https://doi.org/10.1007/s11302-011-9268-1 - Чу, Х.Ю., Ван, Г., и Чжан, Х.Ю. (2021). АТФ как антивозрастной агент: за пределами энергетического резервуара. Открытие лекарств сегодня , 26 (12), 2783–2785. https://doi.org/10.1016/j.drudis.2021.09.022
- Хопфнер, К.-П., Карчер, А., Шин, Д.С., Крейг, Л., Артур, Л.М., Карни, Дж.П., и Тайнер, Дж.А. (2000). Структурная биология АТФазы Rad50: управляемый АТФ конформационный контроль при репарации двухцепочечных разрывов ДНК и суперсемейство ABC-АТФаз. Сотовый , 101 (7), 789–800. https://doi.org/10.1016/S0092-8674(00)80890-9
- Йоханнес Мерингер, Туан-Минь До, Дидье Туро, Макс Хоэншуц, Али Хошсима, Доминик Хоринек, Вернер Кунц, Хофмайстер против Нойберга: действительно ли АТФ является биологическим гидротропом?, Cell Reports Physical Science, Volume 2, Issue 2, 2021, 100343 , ISSN 2666-3864, https://doi.
 org/10.1016/j.xcrp.2021.100343
org/10.1016/j.xcrp.2021.100343
Образование и роль АТФ, креатининфосфата и BMR: Pharmaguideline
Конденсация АДФ с неорганическим фосфатом с образованием АТФ является сильно эндотермической.Образование АТФ
Конденсация АДФ с неорганическим фосфатом с образованием АТФ является сильно эндотермической. В первичных частицах имеется АТФ-синтетаза, расположенная на внутренней поверхности кристовой мембраны. АТФ гидролизуется первичными частицами до фосфата и АДФ.
АТФ-синтетаза содержит три эквивалентных каталитических центра в своей многосубъединичной структуре.
В любой конкретный момент каждый центр реакции находится в различном состоянии:
- Фосфат и АДФ связаны с одним центром
- АДФ и фосфат катализируются с образованием АДФ и фосфата, а вода выделяется в виде -продукт
- АТФ выгружается с одного участка, готов к поступлению АДФ и фосфата

Доступность АДФ контролирует транспорт электронов и окисление субстрата
Стебель первичной частицы может быть не в состоянии пересечь стебель АДФ, если в пустом месте нет АДФ для связывания. Следовательно, центральная часть АТФ-синтетазы не может вращаться. Результатом является накопление протонов в кристальном пространстве, что, в свою очередь, препятствует дальнейшему обмену протонами в цепи переноса электронов, что приводит к прекращению транспорта электронов (и, таким образом, окислению субстрата).
Функции и роль АТФ
Различные молекулы транспортируются через клеточные мембраны с помощью АТФ, который выполняет множество функций внутри клетки. Помимо обеспечения энергией для сокращения мышц, АТФ также поставляет энергию для кровообращения, передвижения и других функций организма. Помимо производства энергии, АТФ необходима для синтеза тысяч типов макромолекул, необходимых для выживания клетки. Аденозинтрифосфат работает как переключатель для управления химическими реакциями и отправки сообщений.
Метаболические процессы зависят от молекул АТФ
- Молекулы АТФ можно рециркулировать после каждой реакции.
- Экзергонические и эндергонические процессы приводятся в действие молекулами АТФ.
- Нейротрансмиттер и внеклеточная сигнальная молекула, АТФ используется как центральной нервной системой, так и периферической нервной системой.
- В отличие от других источников энергии, он может быть непосредственно использован в различных метаболических процессах. Энергия из других химических источников должна быть преобразована в АТФ, прежде чем ее можно будет использовать.
- В метаболизме участвуют ферментативные реакции, фотосинтез, фотофосфорилирование, деление клеток, синтез белка, эндоцитоз, аэробное дыхание, экзоцитоз и подвижность.
Образование креатинфосфата
Аденозиндифосфат (АДФ) превращается в аденозинтрифосфат (АТФ) из креатинфосфата (КФ), фосфорилированной формы креатина. Упражнения расщепляют АТФ на АДФ, но на ранних стадиях он рефосфорилируется. Таким образом, креатинфосфат можно рассматривать как источник топлива для работающих мышц. Хотя этот запас обычно довольно мал, короткие тренировки требуют его как единственного топлива для создания АТФ. Помимо печени и поджелудочной железы, почки и поджелудочная железа также синтезируют креатин. Метильная группа S-аденозилметионина присоединяется к глициновой группе аргинина и гуанидиногруппе глицина. Он транспортируется через мембраны мышечных и нервных клеток с помощью специфической транспортной системы. Фермент креатинкиназа фосфорилирует креатин до креатинфосфата. Мышцы (преимущественно скелетные) содержат около 95% запаса креатин-КП. Соотношение между креатином и креатином составляет 2:1. CP и креатин разрушают креатинин, вещество, выделяемое с мочой. Организм должен синтезировать или потреблять около 2 граммов креатина, чтобы восполнить эту потерю. Креатин в основном содержится в мясе, но его также можно найти в молоке и рыбе.
Таким образом, креатинфосфат можно рассматривать как источник топлива для работающих мышц. Хотя этот запас обычно довольно мал, короткие тренировки требуют его как единственного топлива для создания АТФ. Помимо печени и поджелудочной железы, почки и поджелудочная железа также синтезируют креатин. Метильная группа S-аденозилметионина присоединяется к глициновой группе аргинина и гуанидиногруппе глицина. Он транспортируется через мембраны мышечных и нервных клеток с помощью специфической транспортной системы. Фермент креатинкиназа фосфорилирует креатин до креатинфосфата. Мышцы (преимущественно скелетные) содержат около 95% запаса креатин-КП. Соотношение между креатином и креатином составляет 2:1. CP и креатин разрушают креатинин, вещество, выделяемое с мочой. Организм должен синтезировать или потреблять около 2 граммов креатина, чтобы восполнить эту потерю. Креатин в основном содержится в мясе, но его также можно найти в молоке и рыбе.Роль креатинфосфата
Мышечные клетки хранят фосфат в креатинфосфате, основной молекуле, хранящей фосфат. В покоящихся мышцах преобладает креатинфосфат, концентрация которого в пять раз превышает концентрацию АТФ. Во время острой потребности в энергии креатинкиназа фосфорилирует АДФ в АТФ с использованием креатинфосфата. В дополнение к сперматозоидам и фоторецепторным клеткам, креатинфосфат имеет решающее значение для глаз. Фосфаты мозга могут служить не менее важным источником стабилизирующей энергии. Давно известно, что высокоэнергетические фосфаты способствуют поддержанию мембранных потенциалов, высвобождению нейротрансмиттеров, поддержанию кальциевого гомеостаза, апоптозу, миграции и выживанию нейронов. Кофакторы, такие как креатин, необходимы ферментам, таким как аденилаткиназа.
В покоящихся мышцах преобладает креатинфосфат, концентрация которого в пять раз превышает концентрацию АТФ. Во время острой потребности в энергии креатинкиназа фосфорилирует АДФ в АТФ с использованием креатинфосфата. В дополнение к сперматозоидам и фоторецепторным клеткам, креатинфосфат имеет решающее значение для глаз. Фосфаты мозга могут служить не менее важным источником стабилизирующей энергии. Давно известно, что высокоэнергетические фосфаты способствуют поддержанию мембранных потенциалов, высвобождению нейротрансмиттеров, поддержанию кальциевого гомеостаза, апоптозу, миграции и выживанию нейронов. Кофакторы, такие как креатин, необходимы ферментам, таким как аденилаткиназа.BMR
В состоянии покоя скорость основного обмена эндотермического животного (BMR) показывает количество энергии, которое оно расходует в единицу времени. Это измеряется в единицах энергии в единицу времени, таких как ватты (джоули в секунду) и миллилитры кислорода в минуту или джоули на килограмм в час (ч•кг). Для обеспечения надлежащего измерения необходимо соблюдать ряд строгих критериев. Физически невозмущенный, в термически нейтральной среде и без активного переваривания пищи — требования для соответствующих постабсорбционных состояний. Животные с брадиметаболической скоростью метаболизма, такие как рыбы и рептилии, называются стандартной скоростью метаболизма (SMR). Скорость метаболизма измеряется при той же температуре, что и BMR, но требуется документальное подтверждение температуры. 9Таким образом, 0005
Для обеспечения надлежащего измерения необходимо соблюдать ряд строгих критериев. Физически невозмущенный, в термически нейтральной среде и без активного переваривания пищи — требования для соответствующих постабсорбционных состояний. Животные с брадиметаболической скоростью метаболизма, такие как рыбы и рептилии, называются стандартной скоростью метаболизма (SMR). Скорость метаболизма измеряется при той же температуре, что и BMR, но требуется документальное подтверждение температуры. 9Таким образом, 0005 BMR представляет собой вариант стандартных измерений скорости метаболизма, в котором не учитывается информация о температуре, что вызывает проблемы с определением «стандартной» скорости метаболизма для многих млекопитающих. Метаболизм тела состоит из процессов, необходимых для функционирования. В состоянии покоя организму человека требуется определенное количество энергии для функционирования. Это называется основной скоростью метаболизма. Тело проходит через несколько процессов, чтобы дышать, циркулировать кровь, регулировать температуру тела, производить клетки и функционировать мозг и нервы. Скорость основного обмена человека определяет, сколько калорий он сжигает каждый день и поддерживает ли он вес, набирает или теряет. От 60 до 75 процентов ежедневного расхода калорий человека приходится на его базовый уровень метаболизма. На это влияет несколько факторов. Когда человеку исполняется 20 лет, масса его тела обычно уменьшается на 1–2 % за десятилетие. Однако индивидуальные различия могут быть значительными.
Скорость основного обмена человека определяет, сколько калорий он сжигает каждый день и поддерживает ли он вес, набирает или теряет. От 60 до 75 процентов ежедневного расхода калорий человека приходится на его базовый уровень метаболизма. На это влияет несколько факторов. Когда человеку исполняется 20 лет, масса его тела обычно уменьшается на 1–2 % за десятилетие. Однако индивидуальные различия могут быть значительными.
Производство тепла телом называется термогенезом, и количество затрачиваемой им энергии можно измерить. Когда человек становится старше, и по мере того, как мышечная масса тела уменьшается (как это происходит при старении), скорость метаболизма тела (BMR) снижается. Рост мышц увеличивает BMR. Было обнаружено, что при поправке на безжировую массу тела уровень аэробной подготовленности не связан с BMR. Хотя уровень аэробной подготовки зависит от сердечно-сосудистых упражнений, он не влияет на BMR. Несмотря на это, анаэробные упражнения действительно увеличивают расход энергии в состоянии покоя (см. «Аэробные и анаэробные упражнения»). Болезни, ранее потребляемые продукты и напитки, температура окружающей среды и уровень стресса также могут влиять на общий расход энергии и уровень основного обмена.
«Аэробные и анаэробные упражнения»). Болезни, ранее потребляемые продукты и напитки, температура окружающей среды и уровень стресса также могут влиять на общий расход энергии и уровень основного обмена.
Когда человек бодрствует, BMR измеряется в очень ограниченных условиях. Измерения BMR требуют, чтобы симпатическая нервная система человека не стимулировалась, а это означает, что они должны быть полностью беспокойными. Более распространенным измерением является скорость метаболизма в покое (RMR), поскольку строгих критериев меньше. Непрямая калориметрия может использоваться для измерения BMR, а прямая калориметрия может использоваться для его непосредственного измерения. Оцените возраст, рост и вес, используя уравнение, основанное на факторах пола, веса и роста. Исследователи, изучающие энергетический обмен, подтвердили правильность дыхательного коэффициента (RQ), одного из показателей, измеряющих состав углеводов, жиров и белков, а также их преобразование в энергетические субстраты, которые могут быть использованы организмом.

