Метаболизм прокариот. Катаболизм и анаболизм. Брожение : Farmf
МЕТАБОЛИЗМ ПРОКАРИОТ
ПРОЦЕССЫ КАТАБОЛИЗМА И АНАБОЛИЗМА
Метаболизм прокариот, так же как и эукариот, складывается из двух противоположно направленных процессов — катаболизма и анаболизма.
Катаболизм — это совокупность реакций окисления различных восстановленных органических и неорганических соединений, сопровождающихся выделением энергии, аккумулируемой клеткой л-форме фосфатных связей (АТФ).
Анаболизм — это совокупность реакций биосинтеза конституционных и запасных компонентов клетки за счет веществ питательного субстрата и промежуточных продуктов, образующихся при катаболизме. Анаболизм осуществляется за счет энергии, аккумулированной в фосфатных связях в форме АТФ или других богатых энергией соединений.
Процессы катаболизма и анаболизма в клетке протекают одновременно и тесно взаимосвязаны между собой. Совокупность последовательных ферментативных реакций обоих процессов можно подразделить на 3 этапа.
Начальный этап предусматривает ферментативное превращение веществ исходного субстрата и носит название периферического метаболизма (СО2).
Промежуточный этап объединяет ферментативные реакции, сопровождающиеся образованием промежуточных продуктов, нередко одинаковых для процессов катаболизма и анаболизма (ПВК).
Конечный этап характеризуется образованием конечных продуктов анаболизма, идущих на построение структурных элементов клетки, и конечных продуктов катаболизма, выделяемых клеткой в среду.
ФЕРМЕНТЫ ПРОКАРИОТНОЙ КЛЕТКИ
Ферменты – это белки, биологические катализаторы всех биохимических реакций.
Свойства ферментов:
- Ферменты – это белки,
- Ферменты участвуют в реакциях в небольших количествах.
- Ферменты не входят в состав конечных продуктов реакции,
- Ферменты катализируют много реакций,
- Ферменты обладают специфичностью,
Ф могут быть простые (состоят из Б), и сложные ( Б+ небелковая часть). Небелковая часть может быть прочно связана – простетическая группа, и непрочно связаны – кофермент.
Небелковая часть может быть прочно связана – простетическая группа, и непрочно связаны – кофермент.
По времени образования ферменты прокариотной клетки можно подразделить на 2 группы.
Конститутивные ферменты, синтез которых идет с достоянной скоростью независимо от веществ субстрата; в клетке они находятся в более или менее постоянной концентрации. Примером конститутивных ферментов могут служить гликолитические ферменты.
Индуцибельные ферменты, скорость синтеза которых в клетке резко возрастает в ответ на появление в среде субстрата-индуктора. К индуцибельным ферментам относится большинство гидролаз.
Ключевые позиции в процессах метаболизма занимают алло-стерические
Виды ферментов:
- оксидоредуктазы – О-В,
- Лигазы – катализируют соединение молекул,
- гидролазы – катализируют расщепление между атомами С и О2, N,S. И катализируют присоединение молекул воды.,
- лиазы – катализируют отсоединение атомов от одних веществ и присоединение к другим.,
- Изомеразы – катализируют внутирмолекулярный перенос.
- Эндоферменты – все вышеуказанные Ф,
- Экзоферменты – выделяются из прокариотной клетки в окружающую среду.
АНАБОЛИЗМ ПРОКАРИОТ
Биосинтез углеводов.
- Для прокариот-автотрофов исходным продуктом для синтеза углеводов является СО 2. Фотосинтезирующие автотрофные микроорганизмы фиксируют СО2 и осуществляют биосинтез углеводов так же, как растения при фотосинтезе, через цикл Кальвина.
- Сначала идет синтез триозофосфатов по циклу Кальвина, а затем на их основании синтезируются другие углеводы.
Прокариоты-гетеротрофы получают сахара с пищей.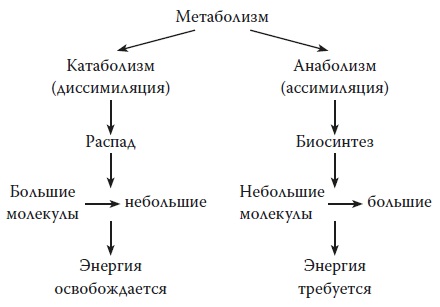
- На основании этих сахаров идет реакция полимеризации.
- Синтез идет путем реакции карбоксилирования:
СО2 + ПВК — ЩУК.
Биосинтез Белков.
Большинство прокариот способны синтезировать все аминокислоты, входящие в состав их клеточных белков. Предшественниками для синтеза аминокислот служат промежуточные продукты метаболизма, такие, как а-кетоглутаровая, щавелевоуксусная, пировиноградная, Источником азота обычно является аммиак или нитраты, нитриты, молекулярный азот.
Биосинтез аминокислот происходит различными путями.
Наиболее простой путь — прямое аминирование кетокислот аммиаком. Образуется 3 а/к
ПВК + Nh4—аланин,
ЩУК+ Nh4— аспорагиновая ,
А-кетоглутаровая+ Nh4— глутаминовая.
Остальные а/к образуются в результате переаминирования. Донором амино-групп является глутаминовая а/к.
У гетеротрофов – а/к получают с пищей и из них синтезируют Б.
Биосинтез нуклеотидов.
Нуклеотиды являются исходным материалом для биосинтеза нуклеиновых кислот н многих коферментов.
По химической природе нуклеотиды — сложные соединения, состоящие из азотистых оснований — производных пурина или пиримидина, углеводов типа пентоз и фосфорной кислоты. Однако, несмотря на сложность химической природы, большинство прокариот способны синтезировать нуклеотиды, используя низкомолекулярные предшественники.
Основным звеном биосинтеза нуклеотидов считается синтез пуриновых и пиримидиновых азотистых оснований.
- Начальной стадией синтеза пуриновых нуклеотидов является взаимодействие фосфорибозил-1-пирофосфата с глутамином с образованием фосфорибозиламина. Затем в реакцию включаются другие соединения-предшественники и. ряд последовательных ферментативных реакций завершается образованием инозиновой кислоты — пуриновото нуклеотида. Она служит исходным продуктом для синтеза других нуклеотидов — адениловой и гуаниловой кислот, необходимых для синтеза РНК.
2. Первым пиримидиновым нуклеотидом, синтезируемым из низкомолекулярных соединений, является
1- оротидиловая кислота – СО2= уридиловая кислоты.
2 — уридиловая кислота + Nh4 —цитидиловая кислота — нуклеотид, содержащий цитозич.
3. цитидиловая кислота путем ферментативного метилирования — тимидиловая кислота — нуклеотид, содержащий тимин.
Биосинтез липидов.
Липиды в клетке прокариот представлены химическими соединениями различной природы (триглицериды, фосфолипиды, гликолипиды, воска), выполняющими разные функции. Они входят в состав клеточных мембран, являются компонентами пигментных систем и транспорта электронов, выполняют роль запасных веществ.
Исходными продуктами для биосинтеза липидов служат жирные кислоты, спирты, углеводы, фосфаты. Пути биосинтеза липидов сложны и протекают с затратой значительного количества энергии при участии многочисленных ферментов. Наиболее важны для жизнедеятельности клетки триглицериды и фосфолипиды.
1. Биосинтез жирных кислот с четным числом атомов углерода происходит в результате последовательного присоединения к молекуле ацетил-KnA двууглеродного остатка от малонил-КоА.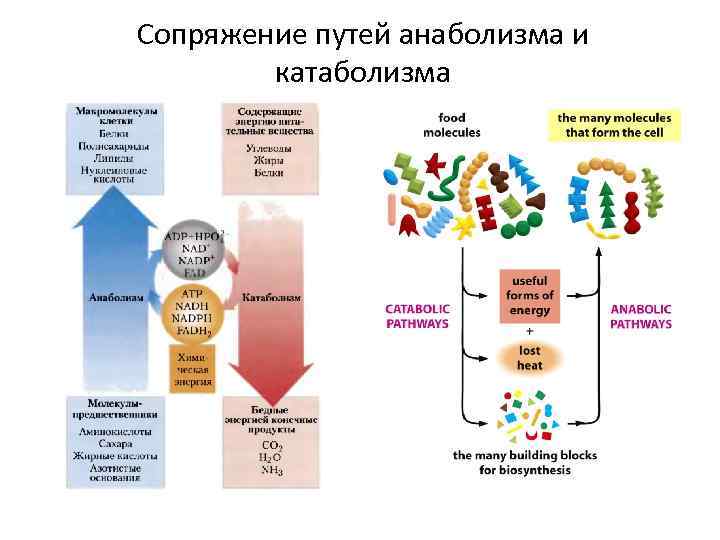
Важную роль в реакциях биосинтеза жирных кислот играет ацилпереносящий белок (АПБ) — переносчик ацильных групп. Последовательное наращивание двууглеродных остатков через ряд промежуточных продуктов приводит к образованию C16 — С18-соединений.
В клетках прокариот компонентами липидов могут являться ненасыщенные жирные кислоты, содержащие одну двойную связь. Образование двойной связи у аэробных микроорганизмов происходит при участии кислорода и специфического фермента десатуразы.
Исходным субстратом для синтеза фосфолипидов служит фосфодиоксиацетон — промежуточное соединение гликолитического цикла. Восстановление его приводит к образованию З-фосфоглицерина, который, соединяясь с двумя остатками жирных кислот, продуцирует фосфатидную кислоту. Присоединение к ее фосфатной группе серина, инозита, этаноламина, холина заканчивается синтезом фосфатидилсерина, фосфатидилинозита, фосфатидилэтано-ламина- (кефалина) и фосфатиДилхолина (лецитина).
КАТАБОЛИЗМ ПРОКАРИОТ
Для прокариот характерны весьма различные способы получения энергии. Так, наиболее древняя группа анаэробных прокариот довольствуется химической энергией процессов брожения. Большинство прокариот получают энергию в реакциях аэробного окисления самых различных органических соединений. Однако среди них имеются факультативные анаэробы, способные переходить от аэробного окисления органических веществ субстрата к анаэробному нитратному или сульфатному дыханию.
Энергия, получаемая прокариотами, аккумулируется клеткой в высокоэнергетических соединениях с фосфатной связью: производные фосфорной кислоты — аденозинтрифосфат (АТФ),
При отщеплении одного из остатков фосфорной кислоты от молекулы АТФ с образованием АДФ освобождается значительное количество энергии.
И наоборот, присоединение фосфорной кислоты к АДФ в реакциях фосфорилирования с образованием АТФ (АДФ + Фн = АТФ) сопровождается аккумуляцией энергии.
Энергия, аккумулированная в АТФ, расходуется клеткой на биосинтез веществ, связанный с активным ростом культуры. Часть энергии постоянно потребляется на поддержание жизнедеятельности организма — на активный транспорт питательного субстрата в клетку, на обновление клеточного материала (белки ферментов, иРНК, вещества клеточной стенки и цитоплазматической мембраны), на движение организма и т. д.
Часть энергии постоянно потребляется на поддержание жизнедеятельности организма — на активный транспорт питательного субстрата в клетку, на обновление клеточного материала (белки ферментов, иРНК, вещества клеточной стенки и цитоплазматической мембраны), на движение организма и т. д.
Ферменты цепи переноса электронов.
Отщепление и перенос водорода или электронов от окисляемого субстрата на конечный акцептор осуществляется через последовательную цепь дыхательных ферментов, получившую название
Общая характеристика процессов брожения.
Брожение — эволюционно наиболее древний и примитивный способ получения энергии, характерный для некоторых групп прокариот. Основные типы брожений — спиртовое, молочнокислое и маслянокислое — открыты
Л. Пастером в 1861 г., хотя продукты брожений были известны
человеку с незапамятных времен.
Процессы брожения протекают в анаэробных условиях без участия молекулярного кислорода за счет окислительно-восстановительных превращений органических соединений субстрата и сопровождаются выделением незначительного количества энергии. . По выходу основного конечного продукта выделяют различные типы брожений: молочнокислое, спиртовое, маслянокислое, пропионо-вокислое и др.
. По выходу основного конечного продукта выделяют различные типы брожений: молочнокислое, спиртовое, маслянокислое, пропионо-вокислое и др.
В любом процессе брожения можно выделить две стадии: окислительную и восстановительную.
Первая, окислительная стадия большинства процессов брожения заключается в серии последовательных реакций, ведущих к образованию пировиноградной кислоты из углевода. У различных групп микроорганизмов установлены три пути превращения глюкозы в пировиноградную кислоту. Первый, наиболее распространенный путь, характерный для дрожжей и многих бактерий, получил название гликолиза.
Второй, пентозофосфатный путь также показан для многих бактерий.
Гликолиз
включает ряд реакций, каждая из которых катализируется специфическим ферментом. Исходными продуктами гликолиза служат моносахариды или дисахариды, которые ферментативным путем расщепляются до моносахаридов.
В реакциях гликолиза из одной молекулы глюкозы образуются 2 молекулы пировиноградной кислоты, 2 молекулы НАД ■ Н2 и 4 молекулы АТФ, из которых 2 синтезируются при окислении двух молекул 3-ФГА и 2 при дегидратации двух молекул 2-ФГК. Из четырех синтезированных молекул АТФ 2 молекулы АТФ затрачиваются на фосфорилирование глюкозы во фруктозо-1,6-дифосфат. Поэтому общий энергетический эффект реакций гликолиза составляет 2 молекулы АТФ на 1 молекулу сброженной глюкозы.
Из четырех синтезированных молекул АТФ 2 молекулы АТФ затрачиваются на фосфорилирование глюкозы во фруктозо-1,6-дифосфат. Поэтому общий энергетический эффект реакций гликолиза составляет 2 молекулы АТФ на 1 молекулу сброженной глюкозы.
Пентозофосфатный путь растщепления углеводов,
Конечными продуктами сбраживания гексоз в пентозофосфатном цикле являются рибозо-5-фосфат и 3-ФГА. Последний гликолитическим путем превращается в пировиноградную кислоту и гексозофосфаты, которые снова включаются в цикл (рис. 25).
Эволюционное значение возникновения пентозофосфатного пути сбраживания углеводов заключается прежде всего в обеспечении прокариотной клетки пентозами как исходными веществами для процессов биосинтеза. В частности, образующаяся рибоза является предшественником иуклеотидов, нуклеиновых
С энергетической стороны этот путь сбраживания углеводов в два раза менее эффективен, чем гликолитический, так как на 1 молекулу глюкозы образуется только 1 молекула АТФ.
Молочнокислое брожение.
Молочнокислое брожение считается эволюционно одним из самых древних и примитивных типов брожения. По характеру самого процесса и образующимся конечным продуктам различают гомо- и гетероферментативное молочнокислое брожение.
1. В основе гомоферментативного молочнокислого брожения лежит гликолитический цикл сбраживания гексозы с образованием двух молекул пировиноградной кислоты. Последняя, выступая конечным акцептором водорода, восстанавливается до единственного продукта — молочной кислоты.
1. Глюкоза—-2 ПВК,
2. ПВК+НАДН2—С3Н6О3
Энергетической выход гомоферментатипного молочнокислого брожения всего 2 молекулы АТФ на 1 молекулу сброженной глюкозы.
Процесс ведут гомоферментативные молочнокислые бактерии. Морфологически они представлены кокками, спор не образуют, неподвижны. 2- В основе гетероферментативного молочнокислого брожения лежит пентозофосфатный путь сбраживания гексоз или пентоз с образованием молочной кислоты и ряда других продуктов — уксусной кислоты, этилового спирта, глицерина и углекислого газа.
По морфологическим, культуральным и многим физиологическим признакам гетероферментативные молочнокислые бактерии близки к гомоферментативньтм. Различные виды молочнокислых бактерий способны развиваться в широких температурных пределах от 7—10 до 40—42 °С, имея оптимум 25—30 «С.
Значение молочнокислого брожения
1. С незапамятных времен молочнокислые бактерии находят применение в различных отраслях хозяйственной деятельности человека — для приготовления кисломолочных продуктов, сливочного масла, сыра, квашения овощей, в хлебопекарном производстве для заквасок ржаного и пшеничного хлеба, в сельском хозяйстве для силосования кормов.
2. Для производства кисломолочных продуктов в разных географических широтах используют различные виды молочнокислых бактерий.
3. Молочнокислые бактерии играют важную роль в приготовлении сыров. В основе сыроварения лежит коагуляция казеина молока под действием сычужного фермента, получаемого из желудка жвачных животных.
4. Многие молочнокислые бактерии способны синтезировать вещества, обладающие антибиотическими свойствами (лактолин, низин, бревин, диплококкцин и др.). На этом свойстве молочнокислых бактерий основано их антагонистическое действие на гнилостные и болезнетворные микроорганизмы в кишечнике человека и животных.
Спиртовое брожение.
этапы
1— Окислительный этап. Процесс спиртового брожения проходит по гликолитическому пути до образования пировиноградной кислоты.
Глюкоза—-2 ПВК,
2- Восстановительный этап. Далее при участии ключевого фермента спиртового брожения — пируватдекарбоксилазы — происходит декарбоксилирование пировиноградной кислоты. В результате образуются ацетальдегид и углекислый газ
3. Образовавшийся ацетлъдегид выступает конечным акцептором водорода и под действием~~НАд-зависимой алкогольдегидрогеназы восстанавливается до этилового спирта. Донором водорода, как и при молочнокислом брожении, служит 3-фосфоглицерино-вый альдегид
Энергетический выход процесса составляют 2 молекулы АТФ на I молекулу сброженной глюкозы. Отличие спиртового брожения от молочнокислого заключается в различной природе конечного акцептора водорода.
Отличие спиртового брожения от молочнокислого заключается в различной природе конечного акцептора водорода.
Значение
Спиртовое брожение лежит в основе ряда промышленных производств — виноделия, получения спирта, пивоварения, хлебопечения.
Возбудители
- -дрожжи – аэробы, клетки округлой формы, неподвижны
- бактерии — сарцины
Маслянокислое брожение.
Маслянокислое брожение проходит в строго анаэробных условиях и ведут его облигатно-анаэробные бактерии рода Clostridium.
Характерной особенностью маслянокислого брожения является реакция конденсации с образованием C4-соединения (масляной кислоты). В результате ряда последовательных реакций из пировиноградной кислоты образуются уксусный альдегид, муравьиная и уксусная кислоты, нередко этиловый спирт. Муравьиная кислота почти тотчас же распадается до СО2 и Н2, а реакция конденсации ацетальдегида приводит к образованию масляной кислоты. Суммарно процесс маслянокислого брожения можно выразить следующим уравнением:
Суммарно процесс маслянокислого брожения можно выразить следующим уравнением:
Энергетический выход данного процесса составляет 3,3 молекулы АТФ на 1 молекулу сброженной глюкозы. Это наибольший выход энергии, получаемый во всех вышерассмотренных типах брожений,
Маслянокислые бактерии рода Clostridium многочисленны и ге-терогенпы. Морфологически они представлены крупными палочками. В молодой культуре палочки подвижны, тип жгутикования перитрихиальный. По мере старения клетки формируют эндоспоры.
Масляно-кислое брожение
1 этап – окисление (гликолиз)
2этап – восстановление
Значение
Положительное:
- минерализуют органическое вещество
- молочно-кислые бактерии фиксируют атм азот.
- Используются для получения парфюмерного масла.
Отрицательное
1 –вызывают порчу кисломолочных продуктов
2- являются возбудителями заболеваний
Ввозбудители столбняка проникают через поврежденные покровы.
Аэробное окисление органического и неорганического субстрата.
Большая часть аэробных прокариотных организмов потребляет в качестве источника энергии различные органические соединения, окисляя их до конечных продуктов СО2 и Н2О. Аэробное окисление органических веществ в прокариотной клетке проходит подобно аэробному дыханию эукариот. В основе его лежит окисление пировиноградной кислоты по циклу трикарбоновых кислот (ЦТК—цикл Кребса).
Собственно цикл Кребса начинается с реакции конденсации ацетил-КоА с молекулой щавелевоуксусной кислоты (ЩУК). В результате реакции образуются свободный KоA и лимонная кислота.
Лимонная кислота под действием фермента аконитазы превращается в цис-аконитовую и далее в изолимонную кислоту. Последняя подвергается дегидрированию, в результате которого образуется щавелево-янтарная кислота и НАД-Н2. Щавелевоянтарная кислота, легко декарбоксилируется и превращается в а-кетоглутаровую кислоту. Далее а-кетоглутаратдегидрогеназный комплекс катализирует реакцию окислительного декарбоксилирования а-кетоглутаровой кислоты, в результате чего образуется сукцинил-КоА, содержащий высокоэнергетическую тиоэфирную связь.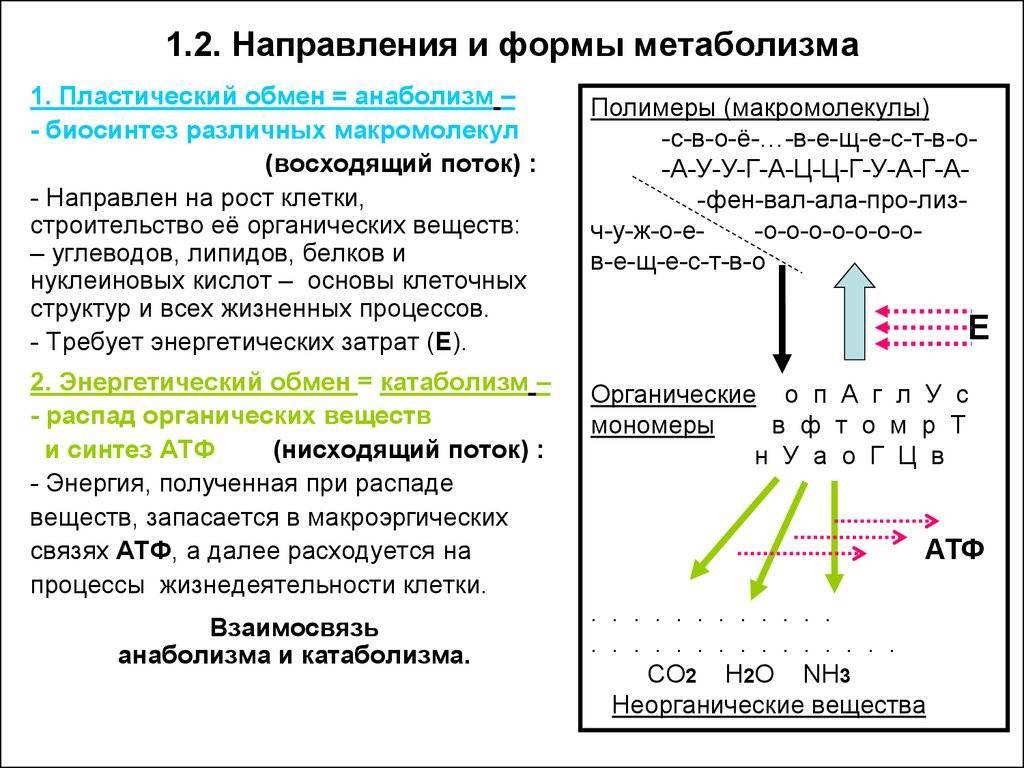 Это единственная необратимая реакция цикла Кребса.
Это единственная необратимая реакция цикла Кребса.
При участии фермента сукцинилтиокиназы из сукцинил-КоА образуется янтарная кислота. Освобождающаяся при разрыве тиоэфирной связи энергия запасается в фосфатной связи АТФ. Янтарная кислота окисляется в фумаровую, которая далее гидратируется с образованием яблочной кислоты. Последующее дегидрирование яблочной кислоты завершает цикл трикарбоновых кислот, образуя щавелевоуксусную кислоту.
Цикл Кребса выполняет две важные функции для клетки.
В реакциях этого цикла осуществляется полное окисление органического субстрата с отщеплением водорода и переходом его на
фермент,
Исходным субстратом служат – углеводы, жирные кислоты, аминокислоты.
Цикл Кребса сопряжен с дыхательной цепью.
В целом энергетический выход аэробного окисления прокариотных организмов значительно выше энергетического эффекта процессов брожения. На одну молекулу глюкозы, окисленной до конечных продуктов CO2 и Н2О, образуется 38 молекул АТФ.
Метаболизм,катаболизм,анаболизм
Федеральное государственное бюджетное образовательное учреждение
высшего профессионального образования
Санкт-Петербургский государственный университет
сервиса и экономики
Реферат
по дисциплине «Биохимия»
на тему: “Метаболизм,катаболизм,
Выполнил: Студент 2-го курса
заочного отделения ИТиРБ
специальности 260.800.62 сокр.
Тимохин Артём Константинович.
Проверил (а): Мирзоев А.М.
Санкт-Петербург
2014г.
Содержание:
1.Метаболизм,катаболизм,
Список литературы……………..…………………..…………
1 Метаболизм, катаболизм, анаболизм.
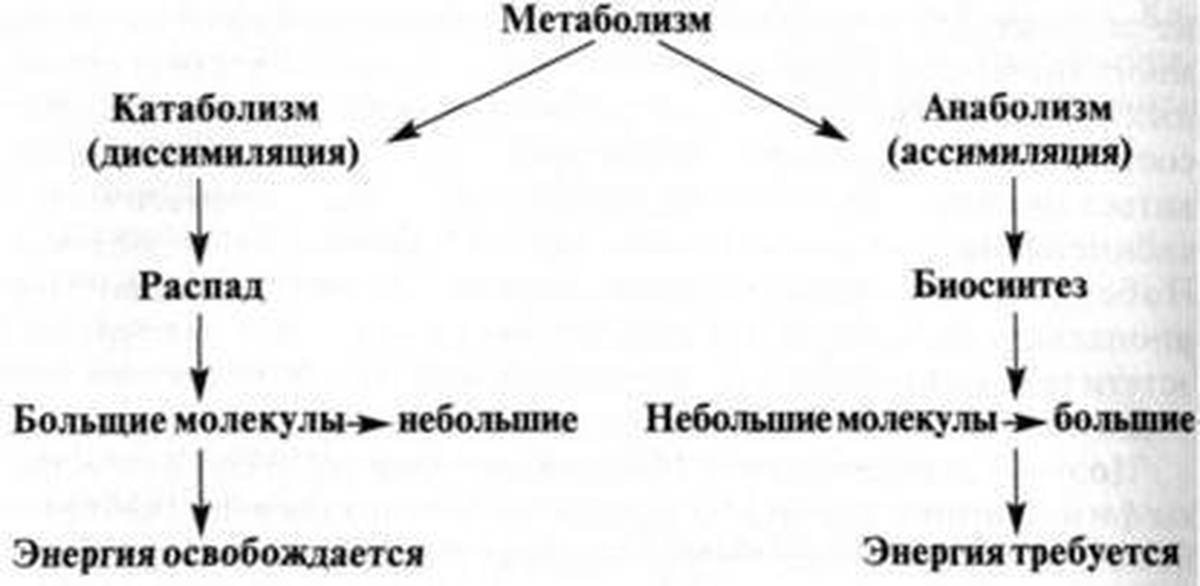
Обмен веществ (метаболизм) клетки складывается в из двух потоков реакций — катаболических и анаболических.

Катаболические пути — это процессы деградации, диссимиляции. К ним относятся различные реакции расщепления (гидролиз, фосфоролиз) и окисления. Крупные органические молекулы расщепляются до простых веществ с выделением содержащейся в них свободной химической энергии. Энергия запасается организмом в форме АТФ и в других соединениях, а затем используется на процессы жизнедеятельности.
Анаболические пути — процессы синтеза, ассимиляции. При этом из простых молекул строятся сложные органические соединения. Такие пути часто включают в себя восстановительные реакции и осуществляются с затратой энергии.
Из-за разной локализации ферментов катаболизма и анаболизма такие противоположные метаболические процессы протекают в клетке одновременно. Их связывают центральные, или амфиболические, процессы (рис. 2).
Рис. 2. Связь катаболических и анаболических путей: Фн — ортофосфорная кислота, ФФН — пирофосфорная кислота.
Связь между анаболизмом и катаболизмом проявляется на трех уровнях.

Уровнь источников углерода: продукты катаболизма могут быть исходными субстратами анаболических реакций.
Энергетический уровне: в процессе катаболизма образуются АТФ и другие высокоэнергетические соединения; анаболические процессы протекают с их потреблением.
Уровнь восстановительных эквивалентов: реакции катаболизма являются в основном окислительными; процессы анаболизма, наоборот, потребляют восстановительные эквиваленты.
Основные биохимические реакции, их последовательность сходна у всех живых форм. Возникли на ранних этапах эволюции, и к моменту, когда началось видообразование, достигли совершенства. Сходны центральные метаболические пути.
В процессе метаболизма осуществляются четыре специфические функции.
Извлечение энергии из окружающей среды (в форме энергии органических веществ или в форме энергии солнечного света).
Превращение экзогенных веществ в «строительные блоки», т. е. в предшественники биополимеров.
Сборка белков, нуклеиновых кислот, липидов, полисахаридов и других клеточных компонентов из этих строительных блоков.
Разрушение «устаревших» биомолекул, уже выполнивших в клетке свои функции.
С химической точки зрения, метаболизм представляет собой совокупность огромного числа разнообразных реакций: окисления, восстановления, расщепления, объединения молекул, межмолекулярного переноса групп и т. д. Специфичным для обмена веществ живого организма является скоординированность отдельных реакций во времени и пространстве. Протоплазма клетки обладает сложной внутренней организацией, структурой. Биохимические процессы локализованы в определенных участках клетки, органеллах, мембранных образованиях. Синтез белка происходит в рибосомах, получение энергии в легко используемой форме — в митохондриях, анаэробная фаза дыхания, гликолиз — в цитоплазме, фотосинтез растений — в хлоропластах и т. д. Мембраны делят клетку на отделы, отсеки, компартменты (от англ.
 compartment),
поэтому разнообразные биохимические
реакции, зачастую противоположного характера,
идут в клетке одновременно, не мешая друг
другу, вследствие пространственного
разделения — компартментализации. В
этом и выражается пространственная скоординированность
биохимических реакций.
compartment),
поэтому разнообразные биохимические
реакции, зачастую противоположного характера,
идут в клетке одновременно, не мешая друг
другу, вследствие пространственного
разделения — компартментализации. В
этом и выражается пространственная скоординированность
биохимических реакций.В клетке отдельные биохимические реакции протекают в строго определенной временной последовательности, образуя длинные цепи взаимосвязанных реакций. Например, гликолиз углеводов протекает в 11 реакций, строго следующих одна за другой, при этом каждая предыдущая создает условия для осуществления следующей. Эта пространственная и временная скоординированность, гармоничность биохимических реакций направлены на достижение одной цели: самовозобновление, самосохранение данной живой системы — организма, клетки. Это характерно для любого живого организма, даже микроскопического.
Поглощая питательные вещества из внешней среды, живые организмы получают энергию, и строительный материал; конечные продукты обмена веществ выводятся в среду.
 Такие системы, в которых непрерывно происходит
поступление и удаление веществ и обмен
со энергией средой, называются открытыми
системами. Их характерная особенность
заключается в отсутствии равновесия
с внешней средой.
Такие системы, в которых непрерывно происходит
поступление и удаление веществ и обмен
со энергией средой, называются открытыми
системами. Их характерная особенность
заключается в отсутствии равновесия
с внешней средой.При термодинамическом равновесии системы все параметры постоянны во времени, нет никаких стационарных потоков за счет действия внешних источников. Энтропия термодинамического равновесия максимальна, свободная энергия равна нулю. В отличие от термодинамического равновесия в биосистемах существует стационарное состояние, при котором скорость переноса вещества и энергии из среды в систему точно соответствует скорости переноса вещества и энергии из системы. Один из ведущих специалистов в области биоэнергетики А. Ленинджер называл живую клетку «неравновесной открытой системой, машиной для извлечения из внешней среды свободной энергии; в результате чего происходит возрастание энтропии среды». В живой клетке как открытой системы в стационарном состоянии отражается важнейшее свойство всего живого — постоянный обмен веществ с окружающей средой.
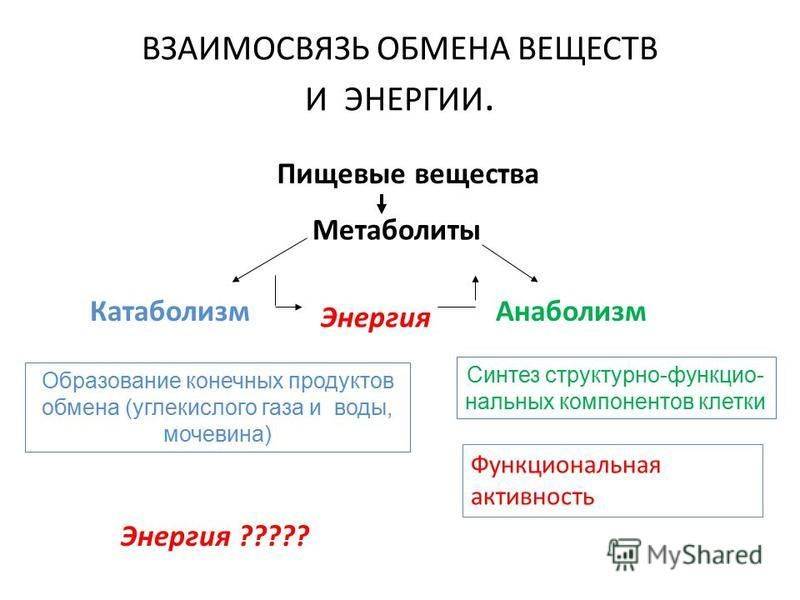
Живой организм как открытая стационарная система хорошо объясняет явление гомеостаза — постоянства состава внутренней среды организма, устойчивость и стабильность биохимических параметров.
Живая клетка не только потребляет вещества, но и экскретирует продукты распада, является открытой системой. Между поступлением питательных веществ в организм и выделением отработанных продуктов существует сложная, часто разветвленная система промежуточных реакций. Если скорости образования и распада промежуточных продуктов равны, устанавливается стационарное состояние. Но в окружающей среде содержание некоторых питательных веществ может резко увеличиться или уменьшиться, вследствие этого изменится скорость их поступления в клетку. Под влияием различных факторов может увеличиваться или уменьшаться скорость той или иной промежуточной реакции, скорость выведения веществ из клетки. В связи с этим значительно изменяются стационарные концентрации компонентов системы.

Как в живой клетке, так и в организме есть многочисленные чувствительные механизмы, которые «выявляют» сдвиги концентраций и компенсируют их, возвращая к норме. При изменении условий стационарного состояния в открытой системе развиваются процессы, направленные на сохранение свойств системы, — динамическая стабилизация стационарного состояния. В большинстве случаев эти механизмы функционируют по принципу обратной связи. При снижении содержания глюкозы в крови (например, вследствие голодания) происходит возбуждение определенного центра в головном мозгу, в результате чего начинает действовать сложный гормонально-ферментативный механизм расщепления запасного углевода гликогена в печени до глюкозы, которая поступает в кровь. Как только ее содержание в крови поднимается до нормы, соответствующий центр головного мозга перестает возбуждаться, механизм расщепления гликогена выключается. Это один из многочисленных примеров функционирования живого организма как саморегулирующейся системы.

Таким образом, относительное постоянство биохимических параметров живого организма не статическое, пассивное, а активное, динамическое. В организм непрерывно поступают вещества из среды, они ассимилируются, из них образуются вещества самого организма, вместе с тем постепенно «стареют» молекулы ранее имевшихся в организме соединений, идут реакции катаболизма, диссимиляции, продукты расщепления удаляются. Эти реакции находятся под контролем генетического аппарата организма, поэтому вновь образующиеся в нем вещества соответствуют признакам наследственности.
За короткое время внешние признаки организма могут не измениться, а его вещества существенно обновятся. Методом меченых атомов установлено, что половина всех белков обновляется за 80 дней, а полное обновление воды происходит за 30 дней. Виднейший английский исследователь и прогрессивный общественный деятель Дж. Бернал писал: «Молекулы в нашем теле и во всяком организме находятся в состоянии непрерывного восстановления, и атомы протекают через него почти непрерывным потоком.
 Вероятно, что никто из нас не
сохранил больше чем несколько атомов,
с которыми мы начали свою жизнь и что,
будучи взрослыми, мы меняем большую часть
материала нашего тела всего за несколько
месяцев». Коротко эту мысль так выразил
Гераклит: «Наши тела текут как ручьи,
вещество в них возобновляется как вода
в потоке». В постоянном обновлении веществ
живого организма проявляется диалектический
закон отрицания: новое отрицает старое,
затем оно само становится старым и тоже
отрицается новым.
Вероятно, что никто из нас не
сохранил больше чем несколько атомов,
с которыми мы начали свою жизнь и что,
будучи взрослыми, мы меняем большую часть
материала нашего тела всего за несколько
месяцев». Коротко эту мысль так выразил
Гераклит: «Наши тела текут как ручьи,
вещество в них возобновляется как вода
в потоке». В постоянном обновлении веществ
живого организма проявляется диалектический
закон отрицания: новое отрицает старое,
затем оно само становится старым и тоже
отрицается новым.Особенностью всех биохимических реакций является их большая скорость, обусловленная присутствием ферментов — биологических катализаторов. Те же реакции вне организма при участии химических катализаторов обладают скоростью на несколько порядков меньше: Ферменты как катализаторы значительно более совершенны, чем химические катализаторы.
Для метаболических процессов характерны ступенчатость и сопряженность. Многие реакции в клетке идут через ряд промежуточных этапов, ступеней.
 Например,
окисление углеводов (клетчатка, крахмал
и т. д.) в процессе сгорания вне организма
протекает одноэтапно — присоединяется
кислород и сразу образуются конечные
продукты окисления углекислый газ и вода.
Например,
окисление углеводов (клетчатка, крахмал
и т. д.) в процессе сгорания вне организма
протекает одноэтапно — присоединяется
кислород и сразу образуются конечные
продукты окисления углекислый газ и вода.В живом организме окисление углеводов в процессе дыхания до С02 и Н20 происходит ступенчато, более чем через 20 промежуточных реакций. Часто проявляется сопряженность отдельных реакций, взаимозависимость друг от друга. Так, многие реакции биосинтеза, являясь энергопотребляющими, сопряжены обычно с экзэргоническими, в процессе которых свободная энергия выделяется в легко используемой форме. Сопряженность хорошо выражена и в многоэтапных цепных процессах, где продукты каждой предыдущей реакции являются исходными соединениями для последующей.
В жидкокристаллическом состоянии вещество единовременно имеет свойства и жидкости (способность течь, образовывать капли), и твердого тела (строгая упорядоченность кристаллической структуры). Вместе с тем у жидких кристаллов есть свойства, характерные только для них: способность образовывать монокристаллы во внешнем электромагнитном поле, крайне большая оптическая активность и др.
 . Для понимания
биохимических явлений очень важна чрезвычайная
чувствительность жидких кристаллов ко
многим внешним воздействиям. Жидкие кристаллы,
для которых характерна одно- или двумерная
упорядоченность, способны к самоорганизации,
спонтанному образованию упорядоченной
структуры и ее воспроизведению. Что представляет
большой интерес при исследовании и объяснении
структурообразования в живых клетках.
. Для понимания
биохимических явлений очень важна чрезвычайная
чувствительность жидких кристаллов ко
многим внешним воздействиям. Жидкие кристаллы,
для которых характерна одно- или двумерная
упорядоченность, способны к самоорганизации,
спонтанному образованию упорядоченной
структуры и ее воспроизведению. Что представляет
большой интерес при исследовании и объяснении
структурообразования в живых клетках.Ни одна из перечисленных особенностей метаболических процессов не может являеться единственным фактором, придающим системе свойство живого. Жизнь как самая сложная форма движения материи может быть понята и объяснена с позиций совокупного рассмотрения всех особенностей этой формы существования белковых тел с ее постоянным обменом веществ с окружающей средой.
Список литературы:
Анисимов А.
 А., Основы биохимии.
– М.Высш. шк., 1986-551 с.
А., Основы биохимии.
– М.Высш. шк., 1986-551 с.Брухман Э.Э., Прикладная биохимия. — М. 1981-296с.
Васильева С.В., Конопатов Ю.В. – СПбГАВМ, 2009г.
Березов Т.Т., Коровкин Б.Ф. Биологическая химия.-М.: Медицина, 1983.-749с.
Биологический
Бохински Р. Современные воззрения в биохимии: Пер. с англ.- М.: Мир, 1987.-543с.
Бышевский А.Ш., Терсенов О.А. Биохимия для врача.- Екатеринбург, Издательско- полиграфическое предприятие «Уральский рабочий», 1994.-383 с.
Грин С., Стаут У., Тейлор Д., Биология в 3-х томах: Пер с англ., под ред. Сопер Р.- М.: Мир, 1993г.-Т. 1- 367с.-Т. 2-326с.- Т. 3- 373с.
Васильева С.В., Конопатов Ю.В. – СПбГАВМ, 2009г.
Диксон М., Уэбб Э. Ферменты: в трех томах. Пер. с англ.- М.: Мир, 1982.-Т. 1-398с. 1982.- Т.2-806с. 1982-.Т. 3-1117с.
Дузу П. Криобиохимия: Пер.с англ.,под ред. Сергеева Г.Б.- М.: Мир, 1980.
 -283с.
-283с.Калоус В., Павличек З. Биофизическая химия: Пер. с чешск.-М.: Мир, 1985.- 446с.
Королев А. П., Гридина С. Б. Основы биохимии. – Учебное пособие, в 3-х частях, РИО КемТИПП, Кемерово, 1999 – 2002гг..
Кретович В. Л. Биохимия растений. – М.: Высшая школа, 1980. – 445 с.
Кнорре Д.Г., Биологическая химия. – М. Высш. шк. 1992-416 с.
Малер г., Кордекс Ю. Основы биологической химии: Пер. с англ.- М.: Мир, 1970.
Плешков Б. П. Биохимия сельскохозяйственных растений. – М.: Агропромиздат,
Что такое метаболизм? | Elysium Health
Ключевые выводы:
Метаболизм — это сумма всех химических реакций, происходящих в организме и зависящих от различных факторов, таких как возраст, гены, уровень стресса, сон и физические упражнения.
Поддержание баланса в обмене веществ имеет важное значение , учитывая постоянно меняющуюся физиологическую среду.
 Колебания в типе и количестве съеденной пищи, уровень физической активности и старение могут повлиять на этот баланс.
Колебания в типе и количестве съеденной пищи, уровень физической активности и старение могут повлиять на этот баланс.Митохондрии играют центральную роль в метаболизме , производя почти 95% энергии клетки. Однако функция митохондрий снижается с возрастом.
Поддержание здорового уровня NAD+ помогает поддерживать митохондриальное и метаболическое здоровье.
Связанный продукт:
Сигнал : Содержит предшественник NAD+ NMN для повышения уровня NAD+ . Signal также содержит хонокиол и виниферин, которые работают вместе с NAD+ для активации SIRT3, ключевого митохондриального фермента, необходимого для поддержания митохондриального и метаболического здоровья.
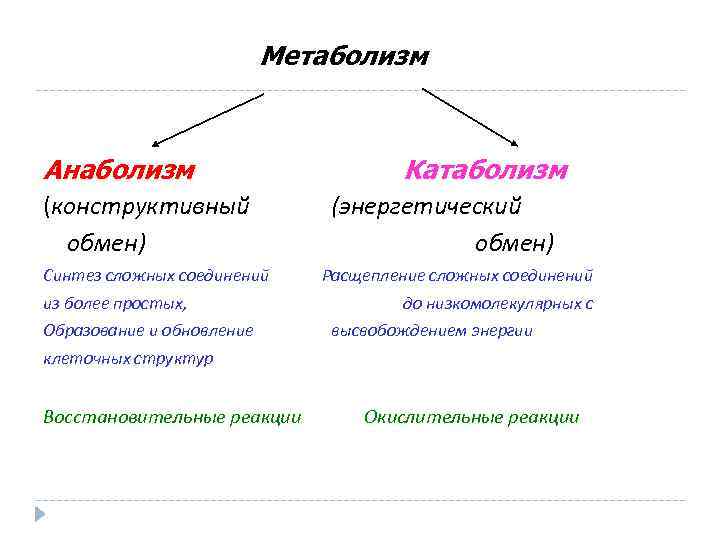
Метаболизм – это сумма всех химических реакций, происходящих внутри организма. Ученые понимают метаболизм как сумму процессов разрушения, известного как катаболизм , и наращивания, или анаболизм , который поддерживает жизнь. На метаболизм влияет множество факторов, включая возраст, гены, уровень стресса, сон и физические упражнения.
На метаболизм влияет множество факторов, включая возраст, гены, уровень стресса, сон и физические упражнения.
Популярные представления о метаболизме не приносят нам пользы. Предположение, содержащееся в большинстве статей (поиск в Google: «как работает метаболизм»), что обмен веществ неразрывно связан с набором и похудением, не является неверным. Но за деревьями не хватает леса. Метаболизм — это сумма всех химических реакций, происходящих внутри тела, огромная сеть взаимодействий на молекулярном уровне, направленная на поддержание организма (вас) в том, что биологи называют гомеостазом: состоянием равновесия, лучше всего иллюстрируемым почти постоянной температурой нашего тела, которая сохраняется даже в самых разных обстоятельствах.
Ученые классифицируют большинство химических реакций, составляющих обмен веществ, на два процесса, которые происходят одновременно и постоянно. При катаболизме большие молекулы (многие из пищи) расщепляются для извлечения энергии и формирования более мелких молекулярных строительных блоков.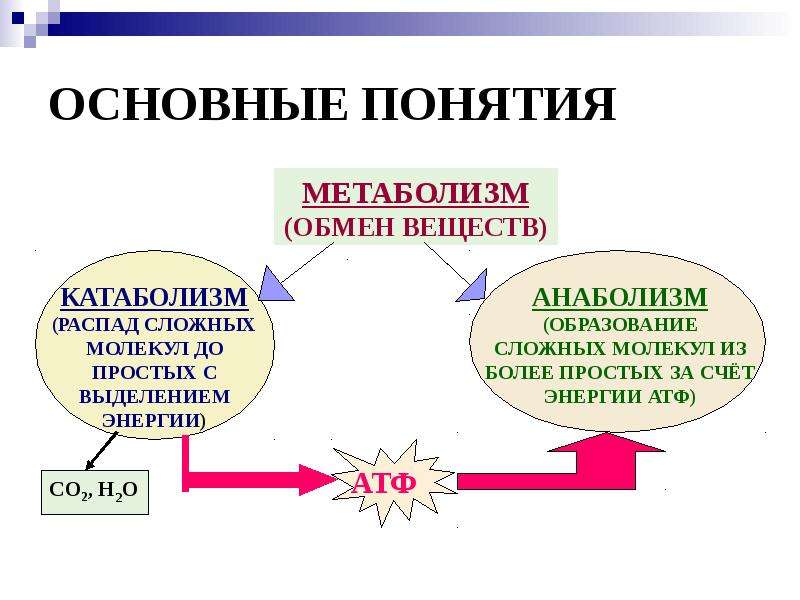 При анаболизме полученная энергия используется для сборки этих строительных блоков в более крупные комплексы, которые можно использовать для построения клеток, тканей и органов.
При анаболизме полученная энергия используется для сборки этих строительных блоков в более крупные комплексы, которые можно использовать для построения клеток, тканей и органов.
Это деликатный баланс и постоянное усилие вашего тела, чтобы производить нужное количество энергии и нужное сырье для выживания. Наряду с вашими генами метаболизм и факторы, влияющие на него, делают вас тем, кто вы есть. Хотя это не звучит так знакомо, как «вы — это то, что вы едите», «вы — это ваш метаболизм» может быть ближе к истине.
Что такое катаболизм и анаболизм? Пищеварение на самом деле является важным первым шагом, который ведет вас от пережевывания пищи к поглощению ценных молекул в кишечнике. Катаболизм начинается внутри клетки, когда большие молекулы (также называемые макромолекулами), такие как углеводы, жиры и белки — основные компоненты пищи — расщепляются на строительные блоки. Они называются мономерами и включают жирные кислоты, аминокислоты, нуклеотиды и моносахариды.
Все это происходит в цепочках химических реакций, называемых метаболическими путями, где ферменты реагируют с молекулой, а затем передают ее другому ферменту для следующей реакции, подобно конвейеру сборки (или конвейеру разборки, в случае катаболизма). Ферменты — это белки, которые ускоряют каждую реакцию (например, катализатор), и многим из этих ферментов требуются коферменты или вспомогательные молекулы, такие как НАД +, чтобы помочь им функционировать. Эта серия реакций продолжается до тех пор, пока молекула не преобразуется в форму, которую можно использовать немедленно или сохранить для последующего использования. Во время многих из этих реакций энергия высвобождается как побочный продукт в виде аденозинтрифосфата или АТФ. АТФ является основным источником энергии для большинства биологических процессов в организме. Конечным результатом является набор молекулярных строительных блоков пищи, которую вы съели, плюс АТФ, которые используются в другой половине метаболизма: анаболизме.
Анаболизм использует многие (но не все) те же ферменты и метаболические пути, что и катаболизм. Это означает, что многие части катаболизма и анаболизма происходят одновременно в одной и той же клетке. Во время анаболизма ферменты используют энергию АТФ, высвободившуюся во время катаболизма, для объединения мономеров обратно в более крупные макромолекулы. Затем эти более крупные молекулы используются в организме в качестве материалов для восстановления и построения клеток, тканей органов, костей и мышц.
Важно помнить, что метаболические пути являются частью очень сложной системы, целью которой является поддержание баланса. Поддержание баланса нетривиально, учитывая постоянно меняющуюся физиологическую среду. Колебания в типе и количестве пищи, которую вы едите, количество упражнений и многие другие факторы, такие как старение, влияют на этот баланс.
Еще один способ представить реакции на молекулярном уровне — сравнить их с собственным поведением на поверхностном уровне. Когда вам становится холодно, вы надеваете еще один слой; когда вы идете на пробежку, вы чувствуете жажду и пьете воду. Точно так же химические реакции, из которых состоит метаболизм, реагируют на их условия на клеточном уровне, чтобы вы продолжали напевать.
Когда вам становится холодно, вы надеваете еще один слой; когда вы идете на пробежку, вы чувствуете жажду и пьете воду. Точно так же химические реакции, из которых состоит метаболизм, реагируют на их условия на клеточном уровне, чтобы вы продолжали напевать.
Во-первых, нам нужно понять, где происходит большинство этих реакций. Митохондрии — это важные органеллы внутри вашей клетки, которые действуют как центр многих метаболических реакций и играют центральную роль в обмене веществ. На самом деле, почти 95% АТФ клетки вырабатывается внутри митохондрий. НАД+, кофермент, упомянутый ранее, является важной молекулой для митохондриальной функции, как и сиртуины, класс НАД-зависимых ферментов, которые действуют как молекулярные сенсоры клеточного энергетического баланса и играют важную роль в регуляции метаболизма.
Мы можем помочь поддержать наши митохондрии, а также ферменты и метаболические реакции внутри них, поддерживая здоровый уровень NAD+ и обеспечивая питательными веществами, которые помогают поддерживать функцию митохондрий. Это особенно важно, потому что уровни NAD+ и функция митохондрий снижаются как нормальная часть старения. Один из способов сохранить наш NAD+ и поддержать функцию митохондрий — использовать наш продукт Signal.
Это особенно важно, потому что уровни NAD+ и функция митохондрий снижаются как нормальная часть старения. Один из способов сохранить наш NAD+ и поддержать функцию митохондрий — использовать наш продукт Signal.
Signal содержит молекулу-предшественник NAD+, называемую NMN (никотинамидный нуклеотид), которая эффективно преобразуется клеткой в NAD+, а также комплекс активации SIRT3 — хонокиол, выделенный из коры Magnolia officinalis , и виниферин, полученный из виноградной лозы. Этот комплекс работает вместе с NAD+ для активации SIRT3 и помогает поддерживать общее митохондриальное и метаболическое здоровье.
Точно так же сон, физические упражнения и образ жизни в соответствии с нашими естественными циркадными ритмами (подумайте: получать солнечный свет утром и избегать яркого света после наступления темноты) поддерживают обмен веществ. Напротив, диета с высоким содержанием рафинированного сахара, прием пищи поздно ночью, малоподвижный образ жизни и сон в неположенное время могут создать нагрузку на метаболическую систему.
Получайте новости Elysium, предложения продуктов только для подписчиков и ежемесячный дайджест новых исследований в области старения. Подпишитесь на нашу рассылку новостей .
Глоссарий научных терминов
Набор терминов, обычно используемых в исследованиях старения.
Старение 10110 лучших научных книг для чтения в 2023 году
От крупнейшего в мире исследования счастья до мастерского исследования клеточной биологии — вот десять наших любимых научных книг, которые стоит прочитать в 2023 году.
Старение 101Преимущества добавки NMN: от 1 дня до 6 месяцев
Клинически доказано, что пероральные добавки с NMN повышают уровень NAD+. Вот временной курс преимуществ, которые вы можете ожидать от добавок NMN, от поддержки митохондрий до улучшения здоровой функции мышц.
Старение 101Метаболизм – Общественный колледж Маунт-Худ, биология 101
Перейти к содержимому Метаболизм организма – это сумма всех химических реакций, протекающих в организме. Эти химические реакции делятся на две основные категории:
Эти химические реакции делятся на две основные категории:
- Анаболизм: строительные полимеры (крупные молекулы, необходимые клетке).
- Катаболизм: расщепление полимеров с выделением энергии.
Это означает, что метаболизм состоит из синтеза (анаболизма) и деградации (катаболизма) ( Рисунок 1 ).
Рисунок 1 Катаболические пути – это те, которые генерируют энергию за счет расщепления более крупных молекул. Анаболические пути — это те, которые требуют энергии для синтеза более крупных молекул. Оба типа путей необходимы для поддержания энергетического баланса клетки.Важно знать, что химические реакции метаболических путей не происходят сами по себе. Каждый этап реакции облегчается или катализируется белком, называемым ферментом . Ферменты играют важную роль в катализе всех типов биологических реакций — как тех, которые требуют энергии, так и тех, которые высвобождают энергию.
Рассмотрим метаболизм сахара. Это классический пример одного из многих клеточных процессов, использующих и производящих энергию. Живые существа потребляют сахара в качестве основного источника энергии, потому что молекулы сахара имеют большое количество энергии, хранящейся в их связях. По большей части фотосинтезирующие организмы, такие как растения, производят эти сахара. Во время фотосинтеза растения используют энергию (первоначально солнечного света) для преобразования углекислого газа (CO 2 ) на молекулы сахара (например, глюкоза: C 6 H 12 O 6 ). Они потребляют углекислый газ и производят кислород в качестве побочного продукта. Эта реакция резюмируется как:
Это классический пример одного из многих клеточных процессов, использующих и производящих энергию. Живые существа потребляют сахара в качестве основного источника энергии, потому что молекулы сахара имеют большое количество энергии, хранящейся в их связях. По большей части фотосинтезирующие организмы, такие как растения, производят эти сахара. Во время фотосинтеза растения используют энергию (первоначально солнечного света) для преобразования углекислого газа (CO 2 ) на молекулы сахара (например, глюкоза: C 6 H 12 O 6 ). Они потребляют углекислый газ и производят кислород в качестве побочного продукта. Эта реакция резюмируется как:
6 CO 2 + 6 H 2 O -> C 6 H 12 O 6 + 6 O 2
Процесс получения глюкозы из углекислого газа и воды требует затраты энергии, потому что глюкоза содержит больше энергии в своих молекулярных связях, чем углекислый газ. Это означает, что этот процесс требует затрат энергии для продолжения. Вы, наверное, уже знаете, что энергия для питания фотосинтеза исходит от солнечного света.
Это означает, что этот процесс требует затрат энергии для продолжения. Вы, наверное, уже знаете, что энергия для питания фотосинтеза исходит от солнечного света.
Напротив, молекулы-аккумуляторы энергии, такие как глюкоза, потребляются для расщепления, чтобы использовать их энергию. Реакция, которая собирает энергию молекулы сахара в клетках, нуждающихся в кислороде для выживания, может быть обобщена как реакция, обратная фотосинтезу. В этой реакции потребляется кислород, а в качестве побочного продукта выделяется углекислый газ. Реакция резюмируется как:
C 6 H 12 O 6 + 6 O 2 -> 6 CO 2 + 6 Н 2 О
Обе эти реакции включают много стадий.
Процессы создания и расщепления молекул сахара иллюстрируют два примера метаболических путей. Метаболический путь – это серия химических реакций, в ходе которых исходная молекула шаг за шагом модифицируется посредством ряда метаболических промежуточных продуктов, что в конечном итоге приводит к получению конечного продукта.

